题目内容
某中学化学兴趣小组为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量的10%的稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水)。有关实验数据如下表:
| 反应前 | 反应后 | ||
| 实验 数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 134.4 g | 10 g | 141.1 g |
请计算(写出计算过程):
(1)该石灰石中碳酸钙的质量分数;
(2)参加反应10%的盐酸的质量。
(1)二氧化碳的质量=134.4g +10g - 141.1g = 3.g …… ……1分
……1分
(2)解:设10g石灰石中碳酸钙的质量为x,参加反应的HCl质量为y
CaCO3 + 2HCl = CaCl2 + H2O + CO2↑ …………1分
100 73 44
x y 3.3 g
100:x = 44:3.3g …………1分
x =7..5g
73:y = 44:3.3g …………1分
y=5.475g
CaCO3% =7.5g ÷10g ×100% = 75% ……… 1分
盐酸的质量=5.475g÷10%= 54.75 g ……… 1分
答:略。

 阅读快车系列答案
阅读快车系列答案实验室里有一瓶标签残缺的试剂瓶,标签中只剩下“Na”和“10%”字样(如下图所示),某兴趣小组对其组成进行如下探究。
 【提出问题】这瓶试剂可能是什么溶液呢?
【提出问题】这瓶试剂可能是什么溶液呢?
【查阅资料】
Ⅰ.初中化学中常见含钠的化合物有:NaCl、NaOH、Na2CO3、NaHCO3,其中一 种物质的类别有别于其它三种物质,该物质是 ⒀ 。
Ⅱ. NaHCO3的水溶液呈碱性。
Ⅲ.室温(20℃)时,四种物质的溶解度数据如下:
| 物质 | NaHCO3 | NaCl | NaOH | Na2CO3 |
| 溶解度g/100g水 | 9.6 | 36 | 109 | 215 |
【资料分析】
依据上述资料分析该瓶试剂不可能是碳酸氢钠的原因是 ⒁ 。
【实验探究】
实验1:
实验测得该溶液的pH>7,则这瓶试剂也不可能是氯化钠。
实验2:
为了检验该溶液是NaOH溶液还是Na2CO3溶液,又进行了如下实验:
取少量溶液于试管中,滴加足量的盐酸,有气泡产生,得出结论,该溶液是Na2CO3溶液。写出上述反应的化学方程式: ⒂ 。
有同学对上述结论提出质疑,他认为该溶液可能由 ⒃ 组成,并设计如下实验。
实验3:
另取样,加入过量的CaCl2溶液(呈中性),观察到有白色沉淀产生,设计这一步骤的目的是 ⒄ ;静置后,取上层清液,滴入酚酞试液,溶液呈红色;得出结论,该同学的假设成立。
上述实验中,证明所加氯化钙溶液是过量的方法是 ⒅ 。
按下表进行实验,有关说法及分析错误的是( )
| 向少量NaOH溶液中滴加CuSO4溶液 | 向少量BaCl2溶液中滴加CuSO4溶液 | |
| 现象 | ① | 白色沉淀 |
| 化学方程式 | CuSO4+2Na(OH)2↓+Na2SO4 | ② |
|
| A. | ①有蓝色沉淀 |
|
| B. | ②反应的化学方程式为:CuSO4+BaCl2=BaSO4↓+CuCl2 |
|
| C. | 两个反应都属于复分解反应 |
|
| D. | 只要有沉淀生成的反应就属于复分解反应 |
甲烷和水反应可以制备水煤气(混和气体),其反应的微观示意图如图所示:

根据以上微观示意图得出的结论中,正确的是( )
|
| A. | 水煤气的成分是一氧化碳和氧气 |
|
| B. | 反应中含氢元素的化合物有三种 |
|
| C. | 反应前后碳元素的化合价没有发生变化 |
|
| D. | 反应中甲和丙的质量之比为4:7 |
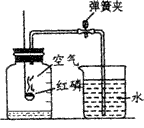
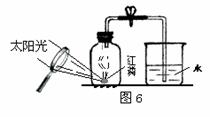
 ____ 、 _。
____ 、 _。 主要是利用了铁的 ;铁在潮湿的空气中容易锈蚀,喷漆可以延缓汽车钢铁外壳的锈蚀,起防锈原理是隔绝 ,喷漆前需将铁制品放入稀盐酸中除锈(铁锈主要成分是Fe2O3),观察到溶液变黄,有无色气泡逸出,写出其中涉及到的一个化学方程式: 。
主要是利用了铁的 ;铁在潮湿的空气中容易锈蚀,喷漆可以延缓汽车钢铁外壳的锈蚀,起防锈原理是隔绝 ,喷漆前需将铁制品放入稀盐酸中除锈(铁锈主要成分是Fe2O3),观察到溶液变黄,有无色气泡逸出,写出其中涉及到的一个化学方程式: 。 (2)化学实验室要从含少量铜粉的银、锰(Mn)混合金属粉末中分离出贵金属,并获得一种盐晶体,将有关三种金属随意编号为:A、B、C,并设计了如下流程:
(2)化学实验室要从含少量铜粉的银、锰(Mn)混合金属粉末中分离出贵金属,并获得一种盐晶体,将有关三种金属随意编号为:A、B、C,并设计了如下流程:

