题目内容
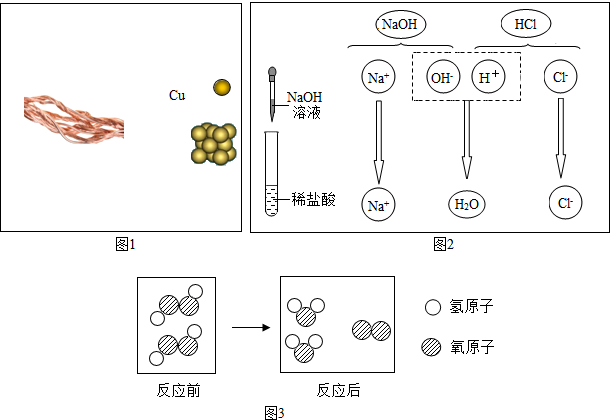
13.已知:A是红色粉末,B、C是氧化物,D、I是常见金属,E为胃酸的主要成分,G为单质.它们之间的转化关系如下:
请回答:
(1)写出下列物质的化学式:AFe2O3,CCO2.
(2)上述转化①②③中,属于置换反应的有②③(填序号).
(3)为了安全,点燃G气体之前要检验纯度.
(4)写出与上述转化①、③有关反应的化学方程式:①Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;③Fe+CuCl2═FeCl2+Cu.
分析 由反应①可知,该反应是冶炼金属的反应,B气体具有还原性,是一氧化碳,A是红色粉末,根据学过的知识,可知A是氧化铁,生成的C是二氧化碳,D是铁,E为胃酸的主要成分说明是盐酸,所以G为氢气;H是氯化亚铁;F是蓝色溶液,能与铁反应生成氯化亚铁,故F事氯化铜,I是铜,根据置换反应的定义来判断:一种单质和一种化合物反应生成另一种单质和另一种化合物;据此解答.
解答 解:由反应①可知,该反应是冶炼金属的反应,B气体具有还原性,是一氧化碳,A是红色粉末,根据学过的知识,可知A是氧化铁,生成的C是二氧化碳,D是铁,E为胃酸的主要成分说明是盐酸,所以G为氢气;H是氯化亚铁;F是蓝色溶液,能与铁反应生成氯化亚铁,故F事氯化铜,I是铜,带入框图,推断合理;
(1)A是Fe2O3、C是CO2,故填:Fe2O3,CO2;
(2)因为E为HCl、D是Fe、G为氢气、H为FeCl2所以②反应是置换反应,由D是Fe、F是CuCl2、H为FeCl2、I是Cu.所以③反应也是置换反应;故填:②③;
(3)氢气是可燃气,不纯时点燃或加热会产生爆炸,故点燃前要检验纯度,故填:检验纯度;
(4)反应①使一氧化碳和氧化铁高温反应生成铁和二氧化碳,反应③是铁与氯化铜反应生成氯化亚铁和铜,故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;Fe+CuCl2═FeCl2+Cu.
点评 根据图表中提供的信息再结合已学过的知识解这类题目,先找出突破口再依此类推,熟记置换反应的定义.

练习册系列答案
相关题目
3.化学实验涉及到很多物质的检验,下列检验中,错误的是( )
| A. |  检验装置气密性 | B. | 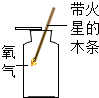 验满氧气 | C. | 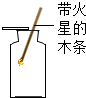 检验二氧化碳 | D. |  氢气验纯 |
1.如表是氯化钠和硝酸钾在不同温度时的溶解度,根据此表回答
(1)60℃时,氯化钠的溶解度为37.3g.
(2)在30℃时,100g水中加入50g硝酸钾,充分搅拌后得到的溶液质量为145.8g.
(3)欲从海水中获得氯化钠晶体,应采取蒸发溶剂方法.
(4)由表中数据分析可知,硝酸钾和氯化钠在某一温度时具有相同的溶解度x,则x的取值范围是36.0<x<36.3g.
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
(2)在30℃时,100g水中加入50g硝酸钾,充分搅拌后得到的溶液质量为145.8g.
(3)欲从海水中获得氯化钠晶体,应采取蒸发溶剂方法.
(4)由表中数据分析可知,硝酸钾和氯化钠在某一温度时具有相同的溶解度x,则x的取值范围是36.0<x<36.3g.
8.下列做法错误的是( )
| A. | 除去CO中的CO2通入足量的氢氧化钠溶液后干燥 | |
| B. | 用稀硫酸除去氯化钠中混有的碳酸钠 | |
| C. | 用水鉴别NH4NO3、NaOH、NaCl三种固体 | |
| D. | 按溶解、过滤、蒸发的主要操作顺序分离氯酸钾和二氧化锰混合制取氧气后的剩余固体 |
18.下列做法不符合绿色设计理念的是( )
| A. | 化石燃料的直接利用 | B. | 用布袋替代塑料购物袋 | ||
| C. | 回收废弃的金属制品 | D. | 工业废水处理达标后排放 |
2.规范的实验操作是化学实验成功的关键,下列操作中正确的是( )
| A. |  稀释浓硫酸 | B. |  闻气体气味 | C. |  取用液体试剂 | D. |  量9.5mL液体 |
 A、B、C是三种不同类别的含有氧元素的化合物,物质间相互反应的关系如图所示(图中“-”表示相连的两种物质能在溶液中发生反应).若B为纯碱,A的浓溶液在实验室常用于做气体干燥剂,A、C间的反应为复分解反应,回答下列问题:
A、B、C是三种不同类别的含有氧元素的化合物,物质间相互反应的关系如图所示(图中“-”表示相连的两种物质能在溶液中发生反应).若B为纯碱,A的浓溶液在实验室常用于做气体干燥剂,A、C间的反应为复分解反应,回答下列问题: