题目内容
6.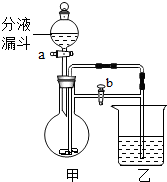 化学小组同学利用如图装置进行相关实验.
化学小组同学利用如图装置进行相关实验.(1)若甲中放入块状大理石,乙中放入澄清石灰水,打开b,将分液漏斗中过量的盐酸注入,关闭a,此时乙中反应的化学方程式是CO2+Ca(OH)2═CaCO3↓+H2O,一段时间后,关闭b,观察到乙中液体变澄清,产生此现象的原因是关闭b,生成的二氧化碳使甲中的压强增大,将稀盐酸压入乙试管,稀盐酸与碳酸钙反应生成氯化钙.
(2)若甲中放入氢氧化钠固体,乙中放入水,关闭b,将分液漏斗中的盐酸注入,关闭a.观察到甲中导管内液面上升至一定高度,一段时间后液面下降且最终高于烧瓶中的液面.甲中反应的化学方程式是HCl+NaOH═NaCl+H2O.同学们解释“甲中导管内液面上升”的原因有氢氧化钠与盐酸反应放出热量、氢氧化钠固体溶于水放热、滴加稀盐酸挤压空气等.
分析 (1)根据碳酸钙与稀盐酸反应生成氯化钙、水、二氧化碳,二氧化碳和石灰水反应产生碳酸钙沉淀;一段时间后,关闭b,生成的二氧化碳使甲中的压强增大,将稀盐酸压入乙试管,稀盐酸与碳酸钙反应生成氯化钙据此分析;
(2)氢氧化钠固体溶于水放热,氢氧化钠和盐酸发生酸碱中和反应也放热,据此分析出现的现象.
解答 解:(1)甲中放入块状大理石,乙中放入澄清石灰水,打开b,将分液漏斗中过量的盐酸注入,关闭a,这时碳酸钙与稀盐酸反应生成氯化钙、水、二氧化碳,二氧化碳进入乙中,和石灰水反应产生碳酸钙沉淀,反应的方程式为:CO2+Ca(OH)2═CaCO3↓+H2O;一段时间后,关闭b,生成的二氧化碳使甲中的压强增大,将稀盐酸压入乙试管,稀盐酸与碳酸钙反应生成氯化钙,因此液体变澄清;故答案为:CO2+Ca(OH)2═CaCO3↓+H2O;关闭b,生成的二氧化碳使甲中的压强增大,将稀盐酸压入乙试管,稀盐酸与碳酸钙反应生成氯化钙;
(2)甲中是氢氧化钠和盐酸反应产生氯化钠和水,反应的方程式为:HCl+NaOH═NaCl+H2O;甲中导管内液面上升,说明甲中的气压增大,由于氢氧化钠溶于水放热、酸碱中和放热,另外滴加液体会使甲中的空气被压缩等都会使导管内的液面上升;故答案为:HCl+NaOH═NaCl+H2O;氢氧化钠固体溶于水放热、滴加稀盐酸挤压空气.
点评 本题考查了常见物质的性质,合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
9.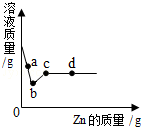 向一定量的AgNO3和Cu(N03)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法不正确的是( )
向一定量的AgNO3和Cu(N03)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法不正确的是( )
 向一定量的AgNO3和Cu(N03)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法不正确的是( )
向一定量的AgNO3和Cu(N03)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法不正确的是( )| A. | a点对应溶液中的溶质有3种 | |
| B. | c点对应溶液中溶质为为Zn(NO3)2 | |
| C. | b~c段对应溶液中一定含有AgNO3 | |
| D. | 取d点对应的固体,加入稀盐酸,有气泡产生 |
10.下列关于化学反应类型的判断不正确的是( )
| A. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 (置换反应) | |
| B. | Na2CO3+Ca(OH)2═CaCO3↓+2NaOH (复分解反应) | |
| C. | 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 (化合反应) | |
| D. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ (分解反应) |
1.下列实验操作正确的是( )
| A. | 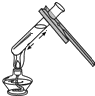 加热液体 | B. | 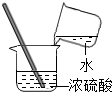 稀释浓硫酸 | C. |  检验气密性 | D. |  熄灭酒精灯 |
11.下列是人体中几种体液的正常pH,酸性最强的是( )
| A. | 胆汁(7.1~7.3) | B. | 胃液(0.9~1.5) | C. | 血浆(7.35~7.45) | D. | 唾液(6.6~7.1) |
18.下列说法中正确的是( )
| A. | 催化剂一定能加快化学反应速率 | |
| B. | 生成盐和水的反应一定是中和反应 | |
| C. | 稀溶液一定是不饱和溶液,浓溶液不一定是饱和溶液 | |
| D. | 碱溶液使酚酞变红,使酚酞变红的溶液不一定是碱溶液 |
15.油、盐、酱、醋是家庭中常用的调味品,下列物质与水充分混合不能形成溶液的是( )
| A. | 食盐 | B. | 苏打 | C. | 芝麻油 | D. | 食醋 |
16.下列实验方法正确的是( )
| A. | 用带火星木条鉴别氮气和空气 | |
| B. | 用紫色石蕊溶液鉴别二氧化碳和一氧化碳 | |
| C. | 用稀硫酸除去铁粉中混有的少量铜粉 | |
| D. | 用稀盐酸除去氧化钙中混有的少量碳酸钙 |