题目内容
15.气体的制取是重要的化学实验活动.请根据给出的装置回答下列问题: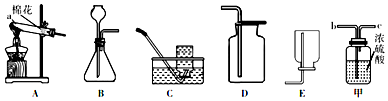
(1)请写出图A中仪器a的名称:试管.
(2)用高锰酸钾制取并收集较纯的氧气,应选择的装置是AC(选填字母).
(3)在实验室中选用B装置制取氧气的反应原理是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑(用化学方程式表示);用这种方法制得的氧气常含有少量水蒸气,若用甲图所示装置除去水蒸气,气体应从b(选填“b”或“c”)端进入.
(4)实验室制取二氧化碳时,可将燃着的木条放到集气瓶口来判断是否已集满二氧化碳气体:实验室不适宜用排水法收集二氧化碳的理由是二氧化碳溶于水且与水反应.
(5)实验室利用B装置和置换反应的原理制取一种气体.该气体是H2(写化学式),该反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑.
分析 试管是常用的反应容器,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了.实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集.
解答 解:(1)试管是常用的反应容器,故答案为:试管;
(2)如果用高锰酸钾制氧气就需要加热,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净;故答案为:AC;
(3)如果用双氧水和二氧化锰制氧气就不需要加热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;若用甲图所示装置除去水蒸气,气体应从长管进入,因为干燥要长进短出;故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;b;
(4)实验室制取二氧化碳时,可将燃着的木条放到集气瓶口来判断是否已集满二氧化碳气体:实验室不适宜用排水法收集二氧化碳的理由是:二氧化碳溶于水且与水反应,故答案为:燃着的木条;二氧化碳溶于水且与水反应;
(5)锌和硫酸反应生成硫酸锌和氢气,本反应属于置换反应,故答案为:H2;Zn+H2SO4=ZnSO4+H2↑;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的干燥和验满等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| A. | 食物腐败 | B. | 蜡烛燃烧 | C. | 石蜡熔化 | D. | 钢铁生锈 |
 有一包固体粉末可能含有BaCO3、NaNO3、NaOH、Cu(OH)2、BaCl2和NaCl中的一种或几种,为确定其成分,设计如下实验方案:
有一包固体粉末可能含有BaCO3、NaNO3、NaOH、Cu(OH)2、BaCl2和NaCl中的一种或几种,为确定其成分,设计如下实验方案:下列说法中,正确的是( )
| A. | 蓝色溶液B中溶质只有CuCl2 | |
| B. | 无色溶液A中一定含有NaOH | |
| C. | 产生白色沉淀B发生的化学变化为CO2+BaCl2+H2O═BaCO3↓+2HCl | |
| D. | 固体粉末中一定含有BaCO3、NaOH、BaCl2、NaCl和Cu(OH)2,可能含有NaNO3 |
(1)“辣味”属于氢氧化锂的(填“物理”或“化学”)物理性质.
(2)载人航天飞船中通常用LiOH代替NaOH来吸收航天员呼吸产生的CO2,则LiOH与CO2反应的化学方程式为CO2+2LiOH=Li2CO3+H2O.
(3)下表是部分物质的溶解性表,运用此溶解性表并结合你对复分解反应发生条件的理解,从表中选出一种盐,该盐能和LiOH发生复分解反应,请你写出该盐的化学式:Cu(NO3)2或CuSO4.
| OH- | CO32- | SO42- | NO3- | |
| Ba2+ | 溶 | 不 | 不 | 溶 |
| Cu2+ | 不 | 不 | 溶 | 溶 |
| Li+ | 溶 | 微溶 | 溶 | 溶 |
| A. |  pH-13的NaOH溶液中加水稀释 | |
| B. |  用适量的KClO3和MnO2混合物加热制O2 | |
| C. |  向一定量的稀盐酸和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量 | |
| D. |  向一定质量的稀盐酸中加入铁粉至过量 |