题目内容
20.实验是科学探究的重要途径,请根据如图所示的实验回答有关问题: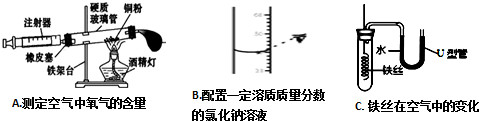
(1)某同学用A装置测定空气中氧气的含量,其化学反应方程式是4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.通过水量法测得硬质玻璃管的容积为32.0mL,为保证实验效果,注射器内至少预留7ml空气,若最终得到的实验数据小于21%,可能的原因是装置漏气(写出一点).
(2)在B实验中的其它实验操作均正确的前提下,该操作将导致所配溶液溶质质量分数偏大(填“偏大”、“偏小”或“不变”).
(3)表面光亮的细铁丝放入C中,一段时间后C中的现象为铁丝生锈,U形管左高右低.
分析 (1)根据反应、物生成物和条件,写方程式;如果反应物不足,或装置漏气等,都能够导致测定的氧气体积分数偏小;
(2)根据溶液的配制方法来完成解答;
(3)根据铁生锈的条件分析解答.
解答 解:
(1)红磷燃烧的化学方程式:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;通过水量法测得硬质玻璃管的容积为32.0mL,为保证实验效果,注射器内至少预留32.0mL×$\frac{1}{5}$=6.4 mL
如果铜粉不足,不能把装置中的氧气耗尽,如果装置漏气,则外面的气体会进入装置中,这些都能够导致实验测得的结果偏小;
(2)俯视读数读数偏大,而实际量取的液体的体积偏少,所以会导致配制的溶液的质量分数偏大;
(3)表面光亮的细铁丝放入C中,一段时间后C中的现象为铁丝生锈,氧气被消耗,试管内压强变小,U形管左高右低.
答案:
(1)4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;7;装置漏气;
(2)偏大;
(3)铁丝生锈,U形管左高右低.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
10.向硝酸银、硝酸铜、硝酸镁的混合溶液中加入一些锌粉,待完全反应后,再过滤.下列情况不可能的是( )
| A. | 滤纸上有Ag、Cu,滤液中有Zn(NO3)2、Mg(NO3)2 | |
| B. | 滤纸上有Ag、Cu、Zn,滤液中有Zn(NO3)2、Mg(NO3)2 | |
| C. | 滤纸上有Ag、Cu,滤液中有AgNO3、Zn(NO3)2、Mg(NO3)2 | |
| D. | 滤纸上有Ag,滤液中有AgNO3、Cu(NO3)2、Zn(NO3)2、Mg(NO3)2 |
5.工业酒精中常含有甲醇(CH3OH),误食后会使人眼睛失明,甚至死亡.下列有关甲醇的说法中不正确的是( )
| A. | 甲醇由碳、氢、氧三种元素组成 | |
| B. | 甲醇中碳、氢、氧三种元素的质量比为3:2:1 | |
| C. | 甲醇由甲醇分子构成 | |
| D. | 一个甲醇分子中共有5个原子 |
12.图为M、N两种固体物质溶解度随温度(t)变化的曲线.下列说法正确的是( )


| A. | 40gM放入150g水中形成不饱和溶液 | |
| B. | t℃时,M的饱和溶液中溶质与溶剂的质量比为2:5 | |
| C. | 80gN放入150g水中全部溶解,此时溶液的温度一定低于t℃ | |
| D. | 200gN的溶液,蒸发60g水、冷却至t℃后得到40g晶体,原溶液溶质的质量分数为40% |
 小科以化合价为纵坐标、以物质类别为横坐标绘制了如图,每种物质中都有一种元素的化合价与纵坐标的数值对应,图中字母均表示初中科学中的常见物质,其中“→”表示物质间的转化关系.已知A为硫的氧化物且氧元素的质量分数为60%,C、D、E、F均含有铜元素.请回答:
小科以化合价为纵坐标、以物质类别为横坐标绘制了如图,每种物质中都有一种元素的化合价与纵坐标的数值对应,图中字母均表示初中科学中的常见物质,其中“→”表示物质间的转化关系.已知A为硫的氧化物且氧元素的质量分数为60%,C、D、E、F均含有铜元素.请回答: 现有一瓶葡萄糖(C6H12O6)溶液,部分标签如图所示,请列式计算,无需答
现有一瓶葡萄糖(C6H12O6)溶液,部分标签如图所示,请列式计算,无需答 