3. (09全国卷Ⅱ6) 物质的量之比为2:5的锌与稀硝酸反应,若硝酸被还原的产物为N2O,
(09全国卷Ⅱ6) 物质的量之比为2:5的锌与稀硝酸反应,若硝酸被还原的产物为N2O,
反应结束后锌没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是
A. 1:4 B.1:5 C. 2:3 D.2:5
答案:A
解析:设2molZn参与反应,因Zn无剩余,则最终生成了2molZn(NO3)2,显然含有4molNO3- ,这部分是没有参与氧化还原反应的HNO3,根据得失电子守恒有:2×n(Zn)=n(HNO3)×4,则n(HNO3)=1mol,即有1molHNO3被还原。
4.(09全国卷Ⅱ13) 含有a mol FeBr2的溶液中,通入x mol Cl2。下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是
 A.x=0.4a,2Fe2++Cl2=2Fe3++2Cl-
A.x=0.4a,2Fe2++Cl2=2Fe3++2Cl-
 B.x=0.6a,2Br-+ Cl2=Br2+2Cl-
B.x=0.6a,2Br-+ Cl2=Br2+2Cl-
 C.x=a,2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl-
C.x=a,2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl-
 D.x=1.5a,2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl-
D.x=1.5a,2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl-
 答案:B
答案:B
 解析:由于Fe2+的还原性强于Br-,故根据氧化还原反应的先后顺序知,Cl2先氧化Fe2+,然后再氧化Br-。2Fe2+ + Cl2
解析:由于Fe2+的还原性强于Br-,故根据氧化还原反应的先后顺序知,Cl2先氧化Fe2+,然后再氧化Br-。2Fe2+ + Cl2  2Fe3+ +
2Cl-,2Br- + Cl2
2Fe3+ +
2Cl-,2Br- + Cl2  Br2 + 2Cl-,2FeBr2 + 3Cl2
Br2 + 2Cl-,2FeBr2 + 3Cl2  2FeCl3 + 2Br2 。当x/a ≤0.5时,Cl2仅氧化Fe2+,故A项正确。
2FeCl3 + 2Br2 。当x/a ≤0.5时,Cl2仅氧化Fe2+,故A项正确。
 当x/a ≥1.5时,Fe2+和Br-合部被氧化,D项正确;
当x/a ≥1.5时,Fe2+和Br-合部被氧化,D项正确;
 当介于两者之间时,则要分步书写方程式,然后进行叠加得总反应。如B项,当x=0.5a时,Cl2刚好把Fe2+全部氧化,而当x=0.6a,显然Cl2还要氧化Br-,而选项中没有表示,故错。
当介于两者之间时,则要分步书写方程式,然后进行叠加得总反应。如B项,当x=0.5a时,Cl2刚好把Fe2+全部氧化,而当x=0.6a,显然Cl2还要氧化Br-,而选项中没有表示,故错。
 5.(09江苏卷
5.(09江苏卷 3)下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
3)下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
|
|
a |
b |
c |
|
A |
Al |
AlCl3 |
Al(OH)3 |
|
B |
HNO3 |
NO |
NO2 |
|
C |
Si |
SiO2 |
H2SiO3 |
|
D |
CH2=CH2 |
CH3CH2OH |
CH3CHO |
答案:B.
 解析:
解析:
 A项:
A项: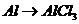
 (
(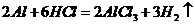 或者
或者 ,
,

 (
(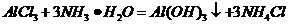 ),
),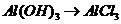 (
(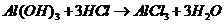 ),
),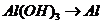 的转化必须经过
的转化必须经过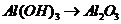 (反应方程式为:
(反应方程式为: )和
)和 (
(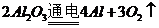 )这两步,所以A项不选;
)这两步,所以A项不选;
 B项:
B项: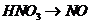 (
(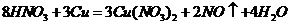 ),
),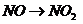 (
(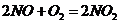 ),
),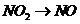 (
(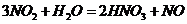 ),
),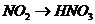 (
(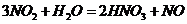 ),所以B项正确;
),所以B项正确;
 C项:
C项: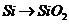 (
(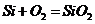 ),
),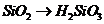 必须经过两步(
必须经过两步(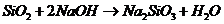 、
、 ),
),
 D项:
D项: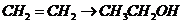 (
( ),
), (
(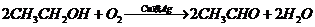 ),
),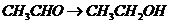 (
( ),
),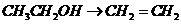 就必须经过两步(
就必须经过两步( 和
和 )
)
 6.(09广东理科基础25)钢铁生锈过程发生如下反应:
6.(09广东理科基础25)钢铁生锈过程发生如下反应:
 ①2Fe+O2+2H2O=2Fe(OH)2;
①2Fe+O2+2H2O=2Fe(OH)2;
 ②4Fe(OH)2+O2+2H2O=4Fe(OH)3;
②4Fe(OH)2+O2+2H2O=4Fe(OH)3;
 ③2Fe(OH)3=Fe2O3+3H2O。
③2Fe(OH)3=Fe2O3+3H2O。
 下列说法正确的是
下列说法正确的是
 A.反应①、②中电子转移数目相等
A.反应①、②中电子转移数目相等
 B.反应①中氧化剂是氧气和水
B.反应①中氧化剂是氧气和水
 C.与铜质水龙头连接处的钢质水管不易发生腐蚀
C.与铜质水龙头连接处的钢质水管不易发生腐蚀
 D.钢铁在潮湿的空气中不能发生电化学腐蚀
D.钢铁在潮湿的空气中不能发生电化学腐蚀
 答案:A
答案:A
 解析:.
解析:.
 ①②反应中消耗O2的量相等,两个反应也仅有O2作为氧化剂,故转移电子数是相等的,A项正确。①中H2O的H、O两元素的化合价没有变,故不作氧化剂,B项错;铜和钢构成原电池,腐蚀速度加快,C项错;钢铁是铁和碳的混合物,在潮湿的空气的中易发生吸氧腐蚀,属于电化学腐蚀,故D项错。
①②反应中消耗O2的量相等,两个反应也仅有O2作为氧化剂,故转移电子数是相等的,A项正确。①中H2O的H、O两元素的化合价没有变,故不作氧化剂,B项错;铜和钢构成原电池,腐蚀速度加快,C项错;钢铁是铁和碳的混合物,在潮湿的空气的中易发生吸氧腐蚀,属于电化学腐蚀,故D项错。
 7.(09福建卷6) 下列类型的反应,一定发生电子转移的是
7.(09福建卷6) 下列类型的反应,一定发生电子转移的是
 A. 化合反应
B. 分解反应
A. 化合反应
B. 分解反应
 C. 置换反应
D. 复分解反应
C. 置换反应
D. 复分解反应
 答案:C
答案:C
 解析:置换反应中肯定有单质参加,一定属于氧化还原反应,即一定有电子转移,C项正确。
解析:置换反应中肯定有单质参加,一定属于氧化还原反应,即一定有电子转移,C项正确。
 8.(09广东化学17) 常温下,往H2O2溶液中滴加少量FeSO4溶液,可发生如下两个反应:2Fe2++H2O2+2H+=2Fe3++2H2O 2Fe3++H2O2=2Fe2++O2↑+2H+下列说法正确的是
8.(09广东化学17) 常温下,往H2O2溶液中滴加少量FeSO4溶液,可发生如下两个反应:2Fe2++H2O2+2H+=2Fe3++2H2O 2Fe3++H2O2=2Fe2++O2↑+2H+下列说法正确的是
 A.H2O2的氧化性比Fe3+强,其还原性比Fe2+弱
A.H2O2的氧化性比Fe3+强,其还原性比Fe2+弱
 B.在H2O2分解过程中,溶液的pH逐渐下降
B.在H2O2分解过程中,溶液的pH逐渐下降
 C.在H2O2分解过程中, Fe2+和Fe3+的总量保持不变
C.在H2O2分解过程中, Fe2+和Fe3+的总量保持不变
 D.H2O2生产过程要严格避免混入Fe2+
D.H2O2生产过程要严格避免混入Fe2+
 答案:CD
答案:CD
 解析:
解析:
 结合A、B两个方程式根据 氧化性、还原性强弱比较规律:得 H2O2的氧化性>Fe3+的氧化性, H2O2的还原性>Fe2+的还原性,A错;
结合A、B两个方程式根据 氧化性、还原性强弱比较规律:得 H2O2的氧化性>Fe3+的氧化性, H2O2的还原性>Fe2+的还原性,A错;
 2H2O2=2H2O+O2↑,分解过程中,Fe2+作催化剂,溶液pH值不变,B错,
2H2O2=2H2O+O2↑,分解过程中,Fe2+作催化剂,溶液pH值不变,B错,
 H2O2分解Fe3+或Fe2+作催化剂,所以总量不变。因为Fe2+可导致H2O2分解,所以H2O2生产过程要避免混入Fe2+,D正确。
H2O2分解Fe3+或Fe2+作催化剂,所以总量不变。因为Fe2+可导致H2O2分解,所以H2O2生产过程要避免混入Fe2+,D正确。
 9.(09上海卷7)在下列变化①大气固氮②硝酸银分解③实验室制取氨气中,按氮元素被氧化、被还原、既不被氧化又不被还原的顺序排列,正确的是
9.(09上海卷7)在下列变化①大气固氮②硝酸银分解③实验室制取氨气中,按氮元素被氧化、被还原、既不被氧化又不被还原的顺序排列,正确的是
 A.①②③ B.②①③ C.③②① D.③①②
A.①②③ B.②①③ C.③②① D.③①②
 答案:A
答案:A
 10.(09安徽卷27)(12分)
10.(09安徽卷27)(12分)
 某厂废水中含5.00×10-3mol·L-1的
某厂废水中含5.00×10-3mol·L-1的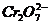 ,其毒性较大。某研究性学习小组为了变废为宝,将废水处理得到磁性材料
,其毒性较大。某研究性学习小组为了变废为宝,将废水处理得到磁性材料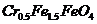 (
(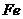 的化合价依次为+3、+2),设计了如下实验流程:
的化合价依次为+3、+2),设计了如下实验流程:







 (1)第①步反应的离子方程式是
(1)第①步反应的离子方程式是
 (2)第②步中用PH试纸测定溶液PH的操作是:
(2)第②步中用PH试纸测定溶液PH的操作是:

 (3)第②步过滤得到的滤渣中主要成分除Cr(OH)3外,还有
(3)第②步过滤得到的滤渣中主要成分除Cr(OH)3外,还有
 (4)欲使1L该废水中的
(4)欲使1L该废水中的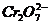 完全转化为
完全转化为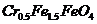 。理论上需要加入
。理论上需要加入
 GFeSO4·7H2O。
GFeSO4·7H2O。
 答案:
答案:
 (1)Cr2O72- + 6Fe2+ + 14H+
(1)Cr2O72- + 6Fe2+ + 14H+  2Cr3+ +
6Fe3+ + 7H2O
2Cr3+ +
6Fe3+ + 7H2O
 (2)将一小块pH试纸放在表面皿上,用玻璃棒蘸取少量待测液,点在pH试纸上,再与标准比色卡对照。
(2)将一小块pH试纸放在表面皿上,用玻璃棒蘸取少量待测液,点在pH试纸上,再与标准比色卡对照。
 (3)Fe(OH)3、Fe(OH)2
(3)Fe(OH)3、Fe(OH)2
 (4)13.9
(4)13.9
 解析:
解析:
 (1)第①步是Cr2O72-与Fe2+发生氧化还原反应,方程式为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O;
(1)第①步是Cr2O72-与Fe2+发生氧化还原反应,方程式为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O;
 (2)测定溶液的pH的方法是:用玻璃棒蘸取待测溶液滴在pH试纸的中心位置,然后对照标准比色卡,读出对应颜色的数据;
(2)测定溶液的pH的方法是:用玻璃棒蘸取待测溶液滴在pH试纸的中心位置,然后对照标准比色卡,读出对应颜色的数据;
 (3)从最终所得磁性材料的化学式可知,滤渣中主要有Cr(OH)3、Fe(OH)2、Fe(OH)3;
(3)从最终所得磁性材料的化学式可知,滤渣中主要有Cr(OH)3、Fe(OH)2、Fe(OH)3;
 (4)1L废水中的n(Cr2O72-)=5.00×10-3mol,根据关系式:Cr2O72--4Cr0.5Fe1.5FeO4-10FeSO4·7H2O,所以理论上n(FeSO4·7H2O)=0.05mol,m(FeSO4·7H2O)= 0.05mol×278g·mol-1=13.9g。
(4)1L废水中的n(Cr2O72-)=5.00×10-3mol,根据关系式:Cr2O72--4Cr0.5Fe1.5FeO4-10FeSO4·7H2O,所以理论上n(FeSO4·7H2O)=0.05mol,m(FeSO4·7H2O)= 0.05mol×278g·mol-1=13.9g。
 、
、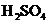 、
、 、
、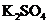 、
、 、
、 和一种未知物质X。
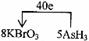
和一种未知物质X。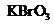 在反应中得到1mol电子生成X,则X的化学式为
。
在反应中得到1mol电子生成X,则X的化学式为
。 b.氧化性:
b.氧化性: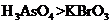
 d.还原性:
d.还原性: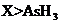

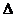 H
H
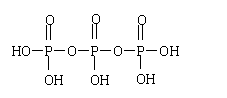
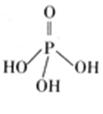 (2)三聚磷酸可视为三个磷酸分子(磷酸结构式见右图)之间脱去两个分子产物,其结构式为
。三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为
(2)三聚磷酸可视为三个磷酸分子(磷酸结构式见右图)之间脱去两个分子产物,其结构式为
。三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为
 ②
②