摘要:(1)①加热氧化铁,②通入一氧化碳,③点燃从尖嘴处排出的气体,④停止通入一氧化碳,⑤停止加热.正确的操作顺序为 . (2)加热过程中看到的现象为 . ,写出有关的化学方程式 , .(3)点燃从尖嘴处排出气体的目的是 .(4)验证该实验完毕后有单质铁生成的方法 .
网址:http://m.1010jiajiao.com/timu_id_910308[举报]
图1甲图是利用一氧化碳与氧化铁反应装置示意图,图1乙是高炉炼铁示意图.请回答下列问题:(A处为澄清石灰水)
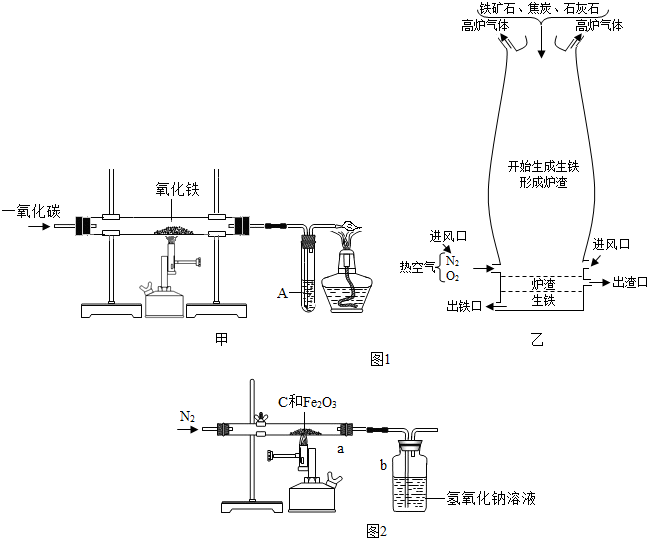
(1)甲图实验过程中,先要进行的是
(2)甲图中硬质玻璃管里发生反应的现象是
(3)甲图中实验要在装置末端a处燃着一盏酒精灯,其作用是
(4)乙图中高炉炼铁时焦炭的作用是
(5)为什么乙图中出铁口低于炉渣出口?
(6)化学兴趣小组的同学为了测定某赤铁矿石中氧化铁的质量分数.
某同学取一定质量的赤铁矿粉与过量的木炭粉混合后,用图2所示装置以合理的操作步骤测定(氢氧化钠溶液可以吸收二氧化碳气体).
①实验中持续通入干燥氮气.加热前缓缓通入一段时间,其作用是
②停止加热前是否需要先断开a和b的连接处以防止倒吸?为什么?
(7)试计算:我国铁矿石资源比较丰富,某钢铁厂用1000t 含氧化铁80% 的赤铁矿石,理论上可以炼出含铁96% 的生铁的质量是多少?(保留一位小数)
查看习题详情和答案>>

(1)甲图实验过程中,先要进行的是
Ⅱ
Ⅱ
(填Ⅰ或Ⅱ).Ⅰ:加热Ⅱ:通入CO(2)甲图中硬质玻璃管里发生反应的现象是
红色固体变成黑色
红色固体变成黑色
,观察到A处出现的现象是石灰水变浑浊
石灰水变浑浊
,其中发生的化学反应方程式是Fe2O3+3CO
2Fe+3CO2;CO2+Ca(OH)2=CaCO3↓+H20
| ||
Fe2O3+3CO
2Fe+3CO2;CO2+Ca(OH)2=CaCO3↓+H20
.
| ||
(3)甲图中实验要在装置末端a处燃着一盏酒精灯,其作用是
点燃一氧化碳,防止污染空气
点燃一氧化碳,防止污染空气
;其中发生的化学反应方程式是2CO+O2
2CO2
| ||
2CO+O2
2CO2
.
| ||
(4)乙图中高炉炼铁时焦炭的作用是
①提供热量、产生高温;②生成还原剂CO
①提供热量、产生高温;②生成还原剂CO
.(5)为什么乙图中出铁口低于炉渣出口?
生铁密度大于炉渣密度
生铁密度大于炉渣密度
.(6)化学兴趣小组的同学为了测定某赤铁矿石中氧化铁的质量分数.
某同学取一定质量的赤铁矿粉与过量的木炭粉混合后,用图2所示装置以合理的操作步骤测定(氢氧化钠溶液可以吸收二氧化碳气体).
①实验中持续通入干燥氮气.加热前缓缓通入一段时间,其作用是
排净空气,防止干扰实验的测定
排净空气,防止干扰实验的测定
.②停止加热前是否需要先断开a和b的连接处以防止倒吸?为什么?
不需要,因为实验中要持续通入氮气
不需要,因为实验中要持续通入氮气
.(7)试计算:我国铁矿石资源比较丰富,某钢铁厂用1000t 含氧化铁80% 的赤铁矿石,理论上可以炼出含铁96% 的生铁的质量是多少?(保留一位小数)
 某中学使用如图所示装置试验一氧化碳与氧化铜的反应.回答下列有关问题.
某中学使用如图所示装置试验一氧化碳与氧化铜的反应.回答下列有关问题.(1)实验开始时,应先
通入一氧化碳排净玻璃管中的空气
通入一氧化碳排净玻璃管中的空气
,然后再加热
再加热
.(2)实验进行一段时间后,A装置中出现的现象为
黑色粉末变红
黑色粉末变红
,说明有铜
铜
生成;B装置中出现的现象为澄清的石灰水变浑浊
澄清的石灰水变浑浊
,说明有二氧化碳
二氧化碳
生成.(3)由上述实验可知,一氧化碳具有
还原性
还原性
性.在我们已经学习过的物质中,具有这种性质的还有木炭
木炭
和氢气
氢气
,因此,它们在工业上常用来冶炼金属
冶炼金属
.(4)在C处放置燃着的酒精灯,目的是
点燃尾气中的一氧化碳,防止污染空气
点燃尾气中的一氧化碳,防止污染空气
.(5)100t含氧化铁80%的铁矿石在理论上可制得
583t.
583t.
t含杂质4%的生铁. 用如图所示装置测定某铁的氧化物中铁元素和氧元素的质量比,记录如下:
用如图所示装置测定某铁的氧化物中铁元素和氧元素的质量比,记录如下:①装铁的氧化物的硬质玻璃管的质量为20克.
②硬质玻璃管与铁的氧化物的质量共为23.6克.
③试管与澄清石灰水的质量共重686克.
④通入CO并加热至铁的氧化物全部转变为铁后,再称量盛石灰水的试管,其质量为688.2克.
回答下列问题:
(1)酒精灯C的作用是
点燃一氧化碳,防止污染空气
点燃一氧化碳,防止污染空气
;(2)实验中B处的现象是
澄清的石灰水变浑浊
澄清的石灰水变浑浊
;(3)根据以上实验记录,计算此铁的氧化物中铁元素和氧元素的质量比
7:2
7:2
;(4)该铁的氧化物化学式为
7:2
7:2
;(5)根据计算写出A处的化学方程式
CO+FeO
Fe+CO2
| ||
CO+FeO
Fe+CO2
.
| ||
资料显示:“氨气在氧气中催化氧化生成两种物质,其中之一是无色难溶于水的气体NO;在纯氧中安静燃烧生成的两种物质中有一种单质是空气的主要组成成分.已知NO遇到氧气立即化合生成NO2,NO2在低温条件下发生如下反应:2NO2═N2O4,N2O4是一种无色气体…”.某校化学小组学生设计如下装置(图中铁夹等夹持装置已略去)进行氨气与氧气在不同条件下反应的实验.
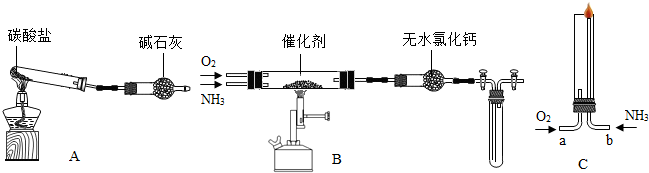
(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是
(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热.实验中同学们发现出来的气体是红色的,停止反应后,关闭B中两个活塞.再将试管浸入冰水中,试管内气体颜色变浅,请说明原因
(3)将过量的氧气与A产生的氨气分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气:
①两气体通入时先O2后NH3的理由是
②氨催化氧化与氨气燃烧的产物不同的原因是
查看习题详情和答案>>

(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是
NH4HCO3或(NH4)2CO3
NH4HCO3或(NH4)2CO3
;碱石灰的作用是吸收生成的CO2、H2O,得到干燥的氨气
吸收生成的CO2、H2O,得到干燥的氨气
.检验从A中出来的氨气的方法是将湿润的红色石蕊试纸置于干燥管管口处,观察颜色变化
将湿润的红色石蕊试纸置于干燥管管口处,观察颜色变化
.(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热.实验中同学们发现出来的气体是红色的,停止反应后,关闭B中两个活塞.再将试管浸入冰水中,试管内气体颜色变浅,请说明原因
生成的NO立即与O2反应生成红棕色的NO2,低温下NO2转化为无色的N2O4
生成的NO立即与O2反应生成红棕色的NO2,低温下NO2转化为无色的N2O4
.(3)将过量的氧气与A产生的氨气分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气:
①两气体通入时先O2后NH3的理由是
使氨气充分反应,防止氨气逸出污染空气
使氨气充分反应,防止氨气逸出污染空气
.②氨催化氧化与氨气燃烧的产物不同的原因是
反应条件不同
反应条件不同
.(2013?金山区一模)小明同学想研究一氧化碳的还原性,通过查阅资料知道:草酸(H2C2O4)与浓硫酸混合加热会产生一氧化碳,反应方程式为:H2C2O4
CO↑+CO2↑+H2O,于是他设计了如图的实验装置,结合装置回答下列问题:?

(1)图A方框中是用草酸制取CO的反应装置,你认为应选择
(2)A装置中产生的气体经过B、C装置(除去杂质),进入D装置的是纯净的CO气体,实验开始时,要先
(3)装置D中反应的化学方程式为
(4)为检验装置D中产生的气体,E装置中的液体应为
(5)装置F中酒精灯的作用是
查看习题详情和答案>>
| ||
| △ |

(1)图A方框中是用草酸制取CO的反应装置,你认为应选择
甲
甲
(填“甲”、“乙”或“丙”)装置;(2)A装置中产生的气体经过B、C装置(除去杂质),进入D装置的是纯净的CO气体,实验开始时,要先
通一段时间CO气体
通一段时间CO气体
,然后加热氧化铁
加热氧化铁
,其目的是排尽空气,防止爆炸;实验结束时,为了防止生成的铁被空气氧化
生成的铁被空气氧化
,要注意先停止加热,继续通一氧化碳直到冷却.(3)装置D中反应的化学方程式为
3CO+Fe2O3
2Fe+3CO2
| ||
3CO+Fe2O3
2Fe+3CO2
;
| ||
(4)为检验装置D中产生的气体,E装置中的液体应为
澄清的石灰水
澄清的石灰水
,化学反应方程式为CO2+Ca(OH)2=CaCO3↓+H2O
CO2+Ca(OH)2=CaCO3↓+H2O
;(5)装置F中酒精灯的作用是
点燃一氧化碳气体,防止污染空气
点燃一氧化碳气体,防止污染空气
.