题目内容
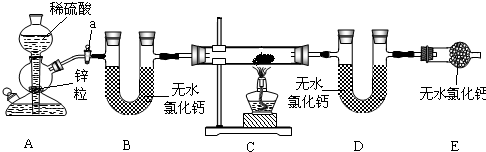
 用如图所示装置测定某铁的氧化物中铁元素和氧元素的质量比,记录如下:
用如图所示装置测定某铁的氧化物中铁元素和氧元素的质量比,记录如下:①装铁的氧化物的硬质玻璃管的质量为20克.
②硬质玻璃管与铁的氧化物的质量共为23.6克.
③试管与澄清石灰水的质量共重686克.
④通入CO并加热至铁的氧化物全部转变为铁后,再称量盛石灰水的试管,其质量为688.2克.
回答下列问题:
(1)酒精灯C的作用是
点燃一氧化碳,防止污染空气
点燃一氧化碳,防止污染空气
;(2)实验中B处的现象是
澄清的石灰水变浑浊
澄清的石灰水变浑浊
;(3)根据以上实验记录,计算此铁的氧化物中铁元素和氧元素的质量比
7:2
7:2
;(4)该铁的氧化物化学式为
7:2
7:2
;(5)根据计算写出A处的化学方程式
CO+FeO
Fe+CO2
| ||
CO+FeO
Fe+CO2
.
| ||
分析:一氧化碳有毒,因此不能直接放入空气中,酒精灯C的作用是:点燃一氧化碳,防止污染空气;实验中B处的现象是:澄清的石灰水变浑浊,因为一氧化碳和铁的氧化物反应生成铁和二氧化碳;有关的计算要准确.
解答:解:(1)一氧化碳有毒,因此不能直接放入空气中,酒精灯C的作用是:点燃一氧化碳,防止污染空气;故答案为:点燃一氧化碳,防止污染空气;
(2)实验中B处的现象是:澄清的石灰水变浑浊,因为一氧化碳和铁的氧化物反应生成铁和二氧化碳;故答案为:澄清的石灰水变浑浊
(3)设铁的氧化物为FexOy,由题意知,二氧化碳的质量=688.2g-686g=2.2g,铁的氧化物的质量=23.6g-20g=3.6g;
yCO+FexOy
xFe+yCO2
56x+16y 44y
3.6g 2.2g
=
x:y=1:1 因此铁的氧化物是FeO;
所以铁与氧的质量比=56:16=7:2
故答案为:7:2
(4)设铁的氧化物为FexOy,由题意知,二氧化碳的质量=688.2g-686g=2.2g,铁的氧化物的质量=23.6g-20g=3.6g;
yCO+FexOy
xFe+yCO2
56x+16y 44y
3.6g 2.2g
=
x:y=1:1 因此铁的氧化物是FeO;
故答案为:FeO
(5)一氧化碳与氧化亚铁反应生成铁和二氧化碳,故答案为:CO+FeO
Fe+CO2
(2)实验中B处的现象是:澄清的石灰水变浑浊,因为一氧化碳和铁的氧化物反应生成铁和二氧化碳;故答案为:澄清的石灰水变浑浊
(3)设铁的氧化物为FexOy,由题意知,二氧化碳的质量=688.2g-686g=2.2g,铁的氧化物的质量=23.6g-20g=3.6g;
yCO+FexOy
| ||
56x+16y 44y
3.6g 2.2g
| 56x+16y |
| 44y |
| 3.6g |
| 2.2g |
所以铁与氧的质量比=56:16=7:2
故答案为:7:2
(4)设铁的氧化物为FexOy,由题意知,二氧化碳的质量=688.2g-686g=2.2g,铁的氧化物的质量=23.6g-20g=3.6g;
yCO+FexOy
| ||
56x+16y 44y
3.6g 2.2g
| 56x+16y |
| 44y |
| 3.6g |
| 2.2g |
故答案为:FeO
(5)一氧化碳与氧化亚铁反应生成铁和二氧化碳,故答案为:CO+FeO
| ||
点评:实验探究题是近几年中考的重点内容之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过查阅资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握,有关的计算要准确,本考点主要出现在实验题中.

练习册系列答案
相关题目
 小沁同学用如图所示装置测定某纯碱样品(杂质为NaCl)中Na2CO3的质量分数.C为有刻度的玻璃仪器,可装合适的液体,根据液面位置变化测定气体体积.
小沁同学用如图所示装置测定某纯碱样品(杂质为NaCl)中Na2CO3的质量分数.C为有刻度的玻璃仪器,可装合适的液体,根据液面位置变化测定气体体积.