摘要:(1)100g生氧剂与水反应生成的氧气质量. (2)生氧剂中含KO2的质量分数.
网址:http://m.1010jiajiao.com/timu_id_896793[举报]
 有一种自生氧防毒面具,其使用的生氧剂的主要成分是KO2.某研究小组取100g生氧剂放入装置A中,加入足量水使之充分反应(4KO2+2H2O=4KOH+3O2↑),测定反应前后装置A的总质量.他们进行了三次实验,测定结果如下:
有一种自生氧防毒面具,其使用的生氧剂的主要成分是KO2.某研究小组取100g生氧剂放入装置A中,加入足量水使之充分反应(4KO2+2H2O=4KOH+3O2↑),测定反应前后装置A的总质量.他们进行了三次实验,测定结果如下:
| 测定序号 | 第1次 | 第2次 | 第3次 | 平均值 |
| 反应前装置A总质量(g) | 400.1 | 400.2 | 399.7 | 400.0 |
| 反应后装置A总质量(g) | 376.1 | 376.1 | 375.8 | 376.0 |
(1)100g 生氧剂与水反应生成的氧气质量;
(2)生氧剂中含钾元素的质量分数. 查看习题详情和答案>>
有一种自生氧防毒面具,其使用的生氧剂的主要成分是KO2.某研究小组取100g生氧剂放入装置A中,加入足量水使之充分反应(4KO2+2H2O═4KOH+3O2↑),测定反应前后装置A的总质量.他们进行了三次实验,测定结果如下:
请根据上述实验结果计算:(假设杂质不含钾元素且不与水反应)
(1)100g生氧剂与水反应生成的氧气质量;
(2)生氧剂中含钾元素的质量分数.

查看习题详情和答案>>
| 测定序号 | 第1次 | 第2次 | 第3次 | 平均值 |
| 反应前装置A总质量(g) | 400.1 | 400.2 | 399.7 | 400.0 |
| 反应后装置A总质量(g) | 376.1 | 376.1 | 375.8 | 376.0 |
(1)100g生氧剂与水反应生成的氧气质量;
(2)生氧剂中含钾元素的质量分数.

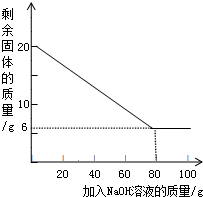
 图是一种“化学氧自救器”(又称“自生氧防毒面具”),其使用的生氧剂(主要成分是KO2)的作用原理为:4KO2+2CO2=2K2CO3+3O2.某研究小组取100g生氧剂,放入装置A中,加入足量水与生氧剂充分反应(化学方程式为:4KO2+2H2O=4KOH+3O2↑),测定反应前后装置A的总质量(装置中的生石灰可防止因反应放热汽化的水蒸气从装置中逸出),他们进行了三次实验.测定结果如下
图是一种“化学氧自救器”(又称“自生氧防毒面具”),其使用的生氧剂(主要成分是KO2)的作用原理为:4KO2+2CO2=2K2CO3+3O2.某研究小组取100g生氧剂,放入装置A中,加入足量水与生氧剂充分反应(化学方程式为:4KO2+2H2O=4KOH+3O2↑),测定反应前后装置A的总质量(装置中的生石灰可防止因反应放热汽化的水蒸气从装置中逸出),他们进行了三次实验.测定结果如下
| 测定序号 | 第1次 | 第2次 | 第3次 | 平均值 |
| 反应前装置A总质量(g) | 400.1 | 400.2 | 399.7 | 400.O |
| 反应后装置A总质量(g) | 368.1 | 368.1 | 367.8 | 368.O |
(1)100g生氧剂与足量水反应生成的氧气质量;
(2)生氧剂中KO2的质量分数;(保留到0.1%) 查看习题详情和答案>>
 某课外活动小组欲对铝镁合金进行研究,测定其中镁的质量分数.
某课外活动小组欲对铝镁合金进行研究,测定其中镁的质量分数.【查阅资料】
(1)氢氧化镁和氢氧化铝据难溶于水.难溶碱受热后能分解生成水和相应的金属氧化物.
(2)镁和氢氧化镁均不能与氢氧化钠溶液反应,但铝和氢氧化铝均能能与氢氧化钠溶液发生如下反应:2Al+2NaOH+2H2O=2NaAlO2+3H2↑ Al(OH)3+NaOH=NaAlO2+2H2O
【方案设计】他们利用实验室提供的盐酸、氢氧化钠溶液设计了三种不同的实验方案:
方案一:铝镁合金
| ||
方案二:铝镁合金
| ||
方案三:铝镁合金
| ||
| ||
【方案评价】
1)三个方案是否均可行,如有不可行的请说明理由.
2)如果你是小组成员,你愿意采用何种方案?
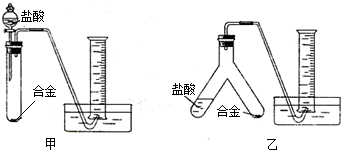
【实验设计】实验小组根据方案二设计了如下图所示(图中的铁架台已省略)的两个实验装置.
你认为选择
【交流讨论】
(1)小组成员实验后,通过交流讨论普遍认为上述三个实验方案均存在操作不够简便或容易产生测量误差的问题.于是按照上述形式重新设计了方案,请你帮助他们完成新方案的设计(在→上方填写相应的试剂和操作):
2)小组成员按照新的测定方案,取20g铝镁合金,研成金属粉末后,把100g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量.实验过程中得到的部分数据与图象如下:
| 加NaOH溶液的次数 | 第一次 | 第二次 | 第三次 | … |
| 剩余固体的质量/g | 1 6.5 | n | 9.5 | … |
(2)分析以上数据可知,上表中n的值为
(3)该金属粉末中Al的质量分数为
(4)列式计算:所用氢氧化钠溶液的溶质质量分数为多少?计算过程:
某课外活动小组欲对铝镁合金进行研究,测定其中镁的质量分数.
【查阅资料】
(1)氢氧化镁和氢氧化铝据难溶于水.难溶碱受热后能分解生成水和相应的金属氧化物.
(2)镁和氢氧化镁均不能与氢氧化钠溶液反应,但铝和氢氧化铝均能能与氢氧化钠溶液发生如下反应:2Al+2NaOH+2H2O==2NaAlO2+3H2↑、Al(OH)3+NaOH==NaAlO2+2H2O
【方案设计】他们利用实验室提供的盐酸、氢氧化钠溶液设计了三种不同的实验方案:
方案一:铝镁合金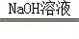 测定生成气体的体积
测定生成气体的体积
方案二:铝镁合金 测定生成气体的体积
测定生成气体的体积
方案三:铝镁合金 溶液
溶液 称量灼烧产物
称量灼烧产物
【方案评价】(1)三个方案是否均可行,如有不可行的请说明理由._________.
(2)如果你是小组成员,你愿意采用何种方案?_________(填“方案一”、“方案二”或“方案三”).理由是_________.
【实验设计】实验小组根据方案二设计了如下图所示(图中的铁架台已省略)的两个实验装置.
【查阅资料】
(1)氢氧化镁和氢氧化铝据难溶于水.难溶碱受热后能分解生成水和相应的金属氧化物.
(2)镁和氢氧化镁均不能与氢氧化钠溶液反应,但铝和氢氧化铝均能能与氢氧化钠溶液发生如下反应:2Al+2NaOH+2H2O==2NaAlO2+3H2↑、Al(OH)3+NaOH==NaAlO2+2H2O
【方案设计】他们利用实验室提供的盐酸、氢氧化钠溶液设计了三种不同的实验方案:
方案一:铝镁合金
 测定生成气体的体积
测定生成气体的体积方案二:铝镁合金
 测定生成气体的体积
测定生成气体的体积方案三:铝镁合金
 溶液
溶液 称量灼烧产物
称量灼烧产物【方案评价】(1)三个方案是否均可行,如有不可行的请说明理由._________.
(2)如果你是小组成员,你愿意采用何种方案?_________(填“方案一”、“方案二”或“方案三”).理由是_________.
【实验设计】实验小组根据方案二设计了如下图所示(图中的铁架台已省略)的两个实验装置.

你认为选择_________装置进行实验更合理,误差更小.
【交流讨论】(3)小组成员实验后,通过交流讨论普遍认为上述三个实验方案均存在操作不够简便或容易产生测量误差的问题.于是按照上述形式重新设计了方案,请你帮助他们完成新方案的设计(在→上方填写相应的试剂和操作):_________
小组成员按照新的测定方案,取20g铝镁合金,研成金属粉末后,把100g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量.实验过程中得到的部分数据与图象如下:加NaOH溶液的次数第一次第二次第三次…/g16.5n9.5…
【交流讨论】(3)小组成员实验后,通过交流讨论普遍认为上述三个实验方案均存在操作不够简便或容易产生测量误差的问题.于是按照上述形式重新设计了方案,请你帮助他们完成新方案的设计(在→上方填写相应的试剂和操作):_________
小组成员按照新的测定方案,取20g铝镁合金,研成金属粉末后,把100g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量.实验过程中得到的部分数据与图象如下:加NaOH溶液的次数第一次第二次第三次…/g16.5n9.5…

(4)小组成员将铝镁合金研成金属粉末的目的是 _________ .
(5)分析以上数据可知,上表中n的值为 _________ ;
(6)该金属粉末中Al的质量分数为 _________ %
(7)列式计算:所用氢氧化钠溶液的溶质质量分数为多少?计算过程:_________ _________.
查看习题详情和答案>>
(5)分析以上数据可知,上表中n的值为 _________ ;
(6)该金属粉末中Al的质量分数为 _________ %
(7)列式计算:所用氢氧化钠溶液的溶质质量分数为多少?计算过程:_________ _________.