摘要:(2)已知过氧化钠()是一种淡黄色固体粉末.常温下可与水反应生成氢氧化钠和氧气.如果在实验室中用过氧化钠和水反应来制取一瓶干燥的氧气.所选装置是 .(3)用B装置制取二氧化碳气体.应选用的液体药品是 ,检验该气体是否收集满的方法是 .
网址:http://m.1010jiajiao.com/timu_id_896539[举报]
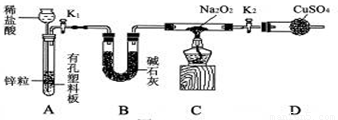
Na2O2是一种淡黄色固体,能与H2O、CO2、HCl等物质反应。某兴趣小组结合化学课学习的内容,探究Na2O2能否和氢气反应。
(已知无水CuSO4是白色粉末,遇水变成蓝色,碱石灰是氢氧化钠固体与生石灰的混合物)
①按图组装仪器,(图中夹持仪器省略)
②检查气密性(气密性良好),装入药品Na2O2
③打开K1、K2,产生的氢气流经装有Na2O2 的硬质玻璃管,一段时间后没有任何现象;
④检验氢气的纯度后,开始加热,观察到硬质玻璃管内Na2O2开始熔化,淡黄色的粉末渐渐变成了白色固体,干燥管内的硫酸铜未变蓝色;
⑤反应后撤去酒精灯,待硬质玻璃管冷却后关闭K1 。

请回答下列问题:
⑴B装置的作用 (填字母)。
A.吸收氢气中混有的氯化氢气体 B.吸收氢气携带的水蒸气
C.吸收装置A、B中空气中的二氧化碳
⑵步骤③目的是 。
⑶步骤⑤关闭K1后,将看到A装置中的现象
| |
⑷通过现象可知Na2O2能和氢气反应。请推测它们反应的生成物 (填字母)。
A. NaOH B. Na2CO3、H2O C. NaOH、H2O D. NaOH、O2
查看习题详情和答案>>
Na2O2是一种淡黄色固体,能与H2O、CO2、HCl等物质反应.某兴趣小组结合化学课学习的内容,探究Na2O2能否和氢气反应.(已知无水CuSO4是白色粉末,遇水变成蓝色,碱石灰是氢氧化钠固体与生石灰的混合物)
①按图组装仪器,(图中夹持仪器省略)
②检查气密性(气密性良好),装入药品Na2O2
③打开K1、K2,产生的氢气流经装有Na2O2 的硬质玻璃管,一段时间后没有任何现象;
④检验氢气的纯度后,开始加热,观察到硬质玻璃管内Na2O2开始熔化,淡黄色的粉末渐渐变成了白色固体,干燥管内的硫酸铜未变蓝色;
⑤反应后撤去酒精灯,待硬质玻璃管冷却后关闭K1.
请回答下列问题:
(1)B装置的作用 (填字母).
A.吸收氢气中混有的氯化氢气体
B.吸收氢气携带的水蒸气
C.吸收装置A、B中空气中的二氧化碳
(2)步骤③目的是 .
(3)步骤⑤关闭K1后,将看到A装置中的现象 .
(4)通过现象可知Na2O2能和氢气反应.请推测它们反应的生成物 (填字母).
A.NaOH B.Na2CO3、H2O C.NaOH、H2O D.NaOH、O2.
 查看习题详情和答案>>
查看习题详情和答案>>
①按图组装仪器,(图中夹持仪器省略)
②检查气密性(气密性良好),装入药品Na2O2
③打开K1、K2,产生的氢气流经装有Na2O2 的硬质玻璃管,一段时间后没有任何现象;
④检验氢气的纯度后,开始加热,观察到硬质玻璃管内Na2O2开始熔化,淡黄色的粉末渐渐变成了白色固体,干燥管内的硫酸铜未变蓝色;
⑤反应后撤去酒精灯,待硬质玻璃管冷却后关闭K1.
请回答下列问题:
(1)B装置的作用 (填字母).
A.吸收氢气中混有的氯化氢气体
B.吸收氢气携带的水蒸气
C.吸收装置A、B中空气中的二氧化碳
(2)步骤③目的是 .
(3)步骤⑤关闭K1后,将看到A装置中的现象 .
(4)通过现象可知Na2O2能和氢气反应.请推测它们反应的生成物 (填字母).
A.NaOH B.Na2CO3、H2O C.NaOH、H2O D.NaOH、O2.
 查看习题详情和答案>>
查看习题详情和答案>>
“过氧化钠(Na2O2)”是一种淡黄色固体,能与水或二氧化碳反应放出氧气.实验室有一份放置了较长时间的过氧化钠粉末,已发生了部分变质,小明想知道当中的成分,决定开展科学探究.
提出问题:变质的过氧化钠粉末中有哪些成分?
收集资料:2Na2O2+2H2O═4NaOH+O2,2Na2O2+2CO2═2Na2CO3+O2.
猜想:
猜测一:变质的过氧化钠粉末是Na2O2和NaOH的混合物;
猜测二:变质的过氧化钠粉末是______的混合物;
猜测三:变质的过氧化钠粉末是Na2O2、NaOH和Na2CO3的混合物.
实验探究:
| 实验操作 | 实验现象 | 实验结论 |
| ①取3.00g变质的过氧化钠粉于一支大试管里,加入适量的水,共收集到0.32g气体,用______检验该生成的气体. | _______________. | 证明粉末中有Na2O2. |
| ②在①的反应液中加入足量的Ba(NO3)2溶液,充分反应. | 白色沉淀 | 证明粉末中有_____. |
| ③将②反应液过滤、洗涤、干燥和称量,得固体1.97g. | \ |
通过对上面实验数据的综合计算,证明猜测______(选填“一”、“二”、“三”)成立.
反思:
(1)H2O2、Na2O2是一类特殊的氧化物,与H2O、CO2、Na2O等常见的氧化物想比较,氧元素的化合价不同.试推断H2O2与Na2O2中氧元素的化合价均为______.
(2)小明想改变实验探究的实验设计,在第②步反应后的反应液中加入硫酸铜溶液,得到了蓝色沉淀,于是证明变质的过氧化钠粉末中有NaOH.老师对小明的设计提出了质疑,原因是______. 查看习题详情和答案>>
 “过氧化钠(Na2O2)”是一种淡黄色固体,能与水或二氧化碳反应放出氧气.实验室有一瓶放置了较长时间的过氧化钠粉末,已知发生了部分变质,同学们取3.00g变质粉末决定探究其中的成分及其质量.
“过氧化钠(Na2O2)”是一种淡黄色固体,能与水或二氧化碳反应放出氧气.实验室有一瓶放置了较长时间的过氧化钠粉末,已知发生了部分变质,同学们取3.00g变质粉末决定探究其中的成分及其质量.
【提出问题】变质的过氧化钠粉末中有哪些成分,它们的质量是多少?
【查阅资料】
①2Na2O2+2H2O═4NaOH+O2↑ 2Na2O2+2CO2═2Na2CO3+O2
②碳酸钠溶液显碱性,氯化钙溶液显中性.
③Na2CO3+CaCl2═CaCO3↓+2NaCl
【猜想与假设】
(1)粉末成分是Na2O2和NaOH的混合物
(2)粉末成分是______的混合物
(3)粉末成分是Na2O2、NaOH 和Na2CO3的混合物
…
【设计与方案】
| 实验步骤 | 实验现象 |
| ①取3.00g变质粉末于一支大试管内,加入适量的水,共收集到0.32g气体,然后用带火星木条检验生成的气体. | 固体完全溶解,______ |
| ②继续向上述试管中加入足量的石灰水,充分反应. | ______ |
| ③将②中物质过滤,得到滤渣,将其洗涤、干燥并称量,得固体1.00g. |  |
| Na2O2 | NaOH | Na2CO3 | |
| 成分(填“有”或“没有”) | ______ | ______ | ______ |
| 质量(g) | ______ | ______ | ______ |
(1)实验室在保存过氧化钠时应注意______.
(2)有同学提出把第②步实验中足量的石灰水改为足量氯化钙溶液,至沉淀不再生成时过滤,向滤液中滴加无色酚酞试液,若液体变红,则证明原粉末中有NaOH.你认为该方案是否合理并说明理由______. 查看习题详情和答案>>
“过氧化钠(Na2O2)”是一种淡黄色固体,能与水或二氧化碳反应都能放出氧气.实验室有一份放置了较长时间的过氧化钠粉末,已发生了部分变质,小明想知道其中的成分,进行了如下实验.
[问 题]变质的过氧化钠粉末中有哪些成分?
[查阅资料]2Na2O2+2H2O═4NaOH+O2↑2Na2O2+2CO2═2Na2CO3+O2
[设 想]
设想一:部分变质的过氧化钠粉末是Na2O2和NaOH的混合物;
设想二:部分变质的过氧化钠粉末是______的混合物;
设想三:部分变质的过氧化钠粉末是Na2O2、NaOH和Na2CO3的混合物.
[实验过程]
| 实验操作 | 实验现象 | 实验结论 |
| ①取一定量变质的过氧化钠粉末一支试管里,加入过量的水,然后用______检验该生成的气体. | ______ | 证明粉末中有Na2O2. |
| ②在①的剩余的溶液中加入足量的硝酸钡溶液,充分反应. | 产生白色沉淀 | 证明粉末中有______. |
| ③在①的剩余的溶液中加入足量的硫酸铜溶液. | ______ |
(1)H2O2、Na2O2是一类特殊的氧化物,与H2O、CO2、Na2O等常见的氧化物想比较,氧元素的化合价不同.试推断H2O2与Na2O2中氧元素的化合价均为______.
(2)如果小明从第③步实验中就得到变质的过氧化钠粉末中含有NaOH,你肯定会提出质疑的,请说明原因:______.
(3)写出小明第②、③步实验中发生反应的化学方程式:______;______. 查看习题详情和答案>>