题目内容
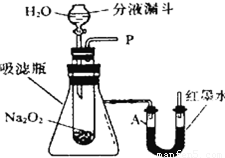
“过氧化钠(Na2O2)”是一种淡黄色固体,能与水或二氧化碳反应都能放出氧气.实验室有一份放置了较长时间的过氧化钠粉末,已发生了部分变质,小明想知道其中的成分,进行了如下实验.
[问 题]变质的过氧化钠粉末中有哪些成分?
[查阅资料]2Na2O2+2H2O═4NaOH+O2↑2Na2O2+2CO2═2Na2CO3+O2
[设 想]
设想一:部分变质的过氧化钠粉末是Na2O2和NaOH的混合物;
设想二:部分变质的过氧化钠粉末是______的混合物;
设想三:部分变质的过氧化钠粉末是Na2O2、NaOH和Na2CO3的混合物.
[实验过程]
| 实验操作 | 实验现象 | 实验结论 |
| ①取一定量变质的过氧化钠粉末一支试管里,加入过量的水,然后用______检验该生成的气体. | ______ | 证明粉末中有Na2O2. |
| ②在①的剩余的溶液中加入足量的硝酸钡溶液,充分反应. | 产生白色沉淀 | 证明粉末中有______. |
| ③在①的剩余的溶液中加入足量的硫酸铜溶液. | ______ |
(1)H2O2、Na2O2是一类特殊的氧化物,与H2O、CO2、Na2O等常见的氧化物想比较,氧元素的化合价不同.试推断H2O2与Na2O2中氧元素的化合价均为______.
(2)如果小明从第③步实验中就得到变质的过氧化钠粉末中含有NaOH,你肯定会提出质疑的,请说明原因:______.
(3)写出小明第②、③步实验中发生反应的化学方程式:______;______.
解:设想二:由于过氧化钠不但能和水发生反应生成氢氧化钠和氧气,而且还能与二氧化碳反应生成碳酸钠和氧气,
实验过程:由于过氧化钠、氢氧化钠和碳酸钠这三种物质中只有过氧化钠能和水发生反应生成气体,且生成的气体是氧气,
而加入的硝酸钡溶液只能和碳酸钠反应生成白色沉淀,说明溶液中含有碳酸根,故说明该粉末中有Na2CO3;加入硫酸铜是证明溶液中含有氢氧根,即含有氢氧化钠
【结论】(1)在过氧化物中钠元素的化合价是+1价,所以氧元素的化合价为-1.
(2)由于 第①步反应中Na2O2与水反应也生成了NaOH,不能证明原变质粉末中是否含有NaOH.
(3)②是碳酸钠与氢氧化钡的反应,其方程式是:Na2CO3+Ba(OH)2=BaCO3↓+2NaOH,③是氢氧化钠与硫酸铜的反应,其方程式为:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
故答案为:设想二:Na2O2和Na2CO3(或NaOH和Na2CO3);
实验过程:①带火星的木条 木条复燃②碳酸钠③产生蓝色沉淀;
结论:(1)1;(2)①步反应中Na2O2与水反应也生成了NaOH,不能证明原变质粉末中是否含有NaOH(3)Na2CO3+Ba(OH)2=BaCO3↓+2NaOH;2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
分析:解答该题时一定抓住提供的资料,由资料不难看出,过氧化钠不仅能与水发生反应,也能与二氧化碳发生反应,由此可知过氧化钠中可能混有氢氧化钠和碳酸钠中的一种或两种,也可能全部变质变成了氢氧化钠和碳酸钠中的一种或两种,故猜想二中变质的过氧化钠粉末可能是过氧化钠和碳酸钠的混合物,也有可能是碳酸钠和氢氧化钠的混合物.根据氧气的性质可对粉末中是否有过氧化钠进行判断,往①所得的溶液中加入硝酸钡溶液有白色沉淀生成说明该粉末中有碳酸钠,加入硫酸铜生成蓝色沉淀说明存在氢氧化钠,据此分析解答即可;
点评:本题主要考查碳酸根、氢氧根的检验,读明题设每个环节的要求,根据要求使用相应的物质的性质完成实验的设计是解题的关键.
实验过程:由于过氧化钠、氢氧化钠和碳酸钠这三种物质中只有过氧化钠能和水发生反应生成气体,且生成的气体是氧气,
而加入的硝酸钡溶液只能和碳酸钠反应生成白色沉淀,说明溶液中含有碳酸根,故说明该粉末中有Na2CO3;加入硫酸铜是证明溶液中含有氢氧根,即含有氢氧化钠
【结论】(1)在过氧化物中钠元素的化合价是+1价,所以氧元素的化合价为-1.
(2)由于 第①步反应中Na2O2与水反应也生成了NaOH,不能证明原变质粉末中是否含有NaOH.
(3)②是碳酸钠与氢氧化钡的反应,其方程式是:Na2CO3+Ba(OH)2=BaCO3↓+2NaOH,③是氢氧化钠与硫酸铜的反应,其方程式为:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
故答案为:设想二:Na2O2和Na2CO3(或NaOH和Na2CO3);
实验过程:①带火星的木条 木条复燃②碳酸钠③产生蓝色沉淀;
结论:(1)1;(2)①步反应中Na2O2与水反应也生成了NaOH,不能证明原变质粉末中是否含有NaOH(3)Na2CO3+Ba(OH)2=BaCO3↓+2NaOH;2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
分析:解答该题时一定抓住提供的资料,由资料不难看出,过氧化钠不仅能与水发生反应,也能与二氧化碳发生反应,由此可知过氧化钠中可能混有氢氧化钠和碳酸钠中的一种或两种,也可能全部变质变成了氢氧化钠和碳酸钠中的一种或两种,故猜想二中变质的过氧化钠粉末可能是过氧化钠和碳酸钠的混合物,也有可能是碳酸钠和氢氧化钠的混合物.根据氧气的性质可对粉末中是否有过氧化钠进行判断,往①所得的溶液中加入硝酸钡溶液有白色沉淀生成说明该粉末中有碳酸钠,加入硫酸铜生成蓝色沉淀说明存在氢氧化钠,据此分析解答即可;
点评:本题主要考查碳酸根、氢氧根的检验,读明题设每个环节的要求,根据要求使用相应的物质的性质完成实验的设计是解题的关键.

练习册系列答案
相关题目

 在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O粉末的脱脂棉上滴水,脱脂棉燃烧起来.小明很兴趣,于是,他和同学们进行探究.
在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O粉末的脱脂棉上滴水,脱脂棉燃烧起来.小明很兴趣,于是,他和同学们进行探究.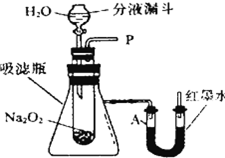 在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O粉末的脱脂棉上滴水,脱脂棉燃烧起来.小明很兴趣,于是,他和同学们进行探究.
在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O粉末的脱脂棉上滴水,脱脂棉燃烧起来.小明很兴趣,于是,他和同学们进行探究.