题目内容
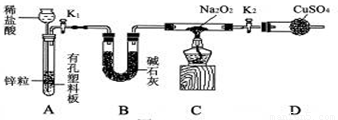
Na2O2是一种淡黄色固体,能与H2O、CO2、HCl等物质反应.某兴趣小组结合化学课学习的内容,探究Na2O2能否和氢气反应.(已知无水CuSO4是白色粉末,遇水变成蓝色,碱石灰是氢氧化钠固体与生石灰的混合物)①按图组装仪器,(图中夹持仪器省略)
②检查气密性(气密性良好),装入药品Na2O2
③打开K1、K2,产生的氢气流经装有Na2O2 的硬质玻璃管,一段时间后没有任何现象;
④检验氢气的纯度后,开始加热,观察到硬质玻璃管内Na2O2开始熔化,淡黄色的粉末渐渐变成了白色固体,干燥管内的硫酸铜未变蓝色;
⑤反应后撤去酒精灯,待硬质玻璃管冷却后关闭K1.
请回答下列问题:
(1)B装置的作用 (填字母).
A.吸收氢气中混有的氯化氢气体
B.吸收氢气携带的水蒸气
C.吸收装置A、B中空气中的二氧化碳
(2)步骤③目的是 .
(3)步骤⑤关闭K1后,将看到A装置中的现象 .
(4)通过现象可知Na2O2能和氢气反应.请推测它们反应的生成物 (填字母).
A.NaOH B.Na2CO3、H2O C.NaOH、H2O D.NaOH、O2.
【答案】分析:(1)根据B装置中的碱石灰的性质分析;
(2)步骤③的目的是使氢气排尽装置内的空气,防止Na2O2与空气中的物质反应;
(3)根据试管内气体压强分析;
(4)根据信息:淡黄色的粉末渐渐变成了白色固体,干燥管内的硫酸铜未变蓝色,和质量守恒定律分析.
解答:解:(1)碱石灰是氢氧化钠固体与生石灰的混合物,其中的氢氧化钠可以吸收氢气中混有的氯化氢气体,吸收装置A、B中空气中的二氧化碳;氧化钙可以吸收氢气携带的水蒸气.
故答案为:A B C.
(2)步骤③的目的是使氢气排尽装置内的空气,防止Na2O2与空气中的物质反应;
故答案为:排尽装置内的空气,防止Na2O2与空气中的物质反应.
(3)关闭K1后,试管内气压增大,将液体压回长颈漏斗,固液分离,反应停止.
故答案为:液体被压入长颈漏斗中,固液分离,反应停止.
(4)淡黄色的粉末渐渐变成了白色固体,干燥管内的硫酸铜未变蓝色,说明没有水生产,根据质量守恒可知生成物应该是NaOH.
故答案为:A.
点评:本题是一综合性较强的题目,要了解碱石灰的性质、实验装置的特点和性能、质量守恒的应用等,综合考查同学们对物质的性质和实验装置的应用能力.
(2)步骤③的目的是使氢气排尽装置内的空气,防止Na2O2与空气中的物质反应;
(3)根据试管内气体压强分析;
(4)根据信息:淡黄色的粉末渐渐变成了白色固体,干燥管内的硫酸铜未变蓝色,和质量守恒定律分析.
解答:解:(1)碱石灰是氢氧化钠固体与生石灰的混合物,其中的氢氧化钠可以吸收氢气中混有的氯化氢气体,吸收装置A、B中空气中的二氧化碳;氧化钙可以吸收氢气携带的水蒸气.
故答案为:A B C.
(2)步骤③的目的是使氢气排尽装置内的空气,防止Na2O2与空气中的物质反应;
故答案为:排尽装置内的空气,防止Na2O2与空气中的物质反应.
(3)关闭K1后,试管内气压增大,将液体压回长颈漏斗,固液分离,反应停止.
故答案为:液体被压入长颈漏斗中,固液分离,反应停止.
(4)淡黄色的粉末渐渐变成了白色固体,干燥管内的硫酸铜未变蓝色,说明没有水生产,根据质量守恒可知生成物应该是NaOH.
故答案为:A.
点评:本题是一综合性较强的题目,要了解碱石灰的性质、实验装置的特点和性能、质量守恒的应用等,综合考查同学们对物质的性质和实验装置的应用能力.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
小明发现一种淡黄色的粉末可以用于杀菌、消毒和漂白,于是想探究该固体的成分。
【提出问题】 该淡黄色固体的化学成分是什么?
【查阅资料】
(1)硫单质是一种淡黄色固体,难溶于水,在空气中点燃硫单质,生成一种无色、有刺激性气味的气体。
(2)过氧化钠(Na2O2)是一种淡黄色固体,能与水反应,生成气体并放出大量的热。
【设计实验方案】
方案一:取少量该固体粉末于试管中,加2mL水,振荡并观察现象。
方案二:在燃烧匙里放少量该固体,在酒精灯上加热,观察现象。
比较以上两方案,你认为的最佳方案是 ,理由是(从环保或操作角度分析) 。
【实验验证并得出结论】
小明向盛有少量该固体的试管中加入2mL水,立刻观察到有无色气泡产生,并且验证出该反应同时生成了氢氧化钠(NaOH)。通过实验验证,确定该淡黄色粉末为过氧化钠。
小明想对生成的气体成分判断,他提出了以下两种假设:①该气体是CO ②该气体是O2
你认为上述假设哪个更合理 (填“①”或“②”)。
请设计一个实验,验证你的合理假设(写出简要操作步骤、实验现象和结论)。
|
操作步骤 |
实验现象 |
结论 |
|
|
|
|
【分析】过氧化钠与水反应的文字表达式为 。
【计算】在过氧化钠(Na2O2)中,
①氧元素的化合价为 ;
②过氧化钠的相对分子质量为 ;
③ 过氧化钠中钠、氧元素的质量比为 ;
④78克过氧化钠与多少克二氧化碳中所含氧元素的质量相等?(列式计算)
 少量该固体的试管中加入2mL水,立刻观察到有无色气泡产生;再向试管中滴加几滴酚酞试液,可观察到溶液变红。小明判断反应生成了氢氧化钠(NaOH)和一种无色气体,并对生成的气体成分提出了以下三种假设:
少量该固体的试管中加入2mL水,立刻观察到有无色气泡产生;再向试管中滴加几滴酚酞试液,可观察到溶液变红。小明判断反应生成了氢氧化钠(NaOH)和一种无色气体,并对生成的气体成分提出了以下三种假设: