网址:http://m.1010jiajiao.com/timu_id_87713[举报]
1、D 2、B 3、B 4、B 5、A 6、D 7、A 8、B 9、C 10、D 11、B 12、C
13、D 14、C 15、C 16、A 17、BD 18、AD 19、BD 20、BD 21、D 22、B
23、(12分)(1)甲  或
或
(2)①3000;
②丙;乙图中电流表的示数太小,误差太大。丙图中R的阻值与电压表阻值接近,误差小。
③
24、(15分)解:
(1)对零件在斜面上向上运动时受力分析如图,从B到C过程中,设零件加速度为a1,到达B点速度为v,根据牛顿第二定律得

 (3分)
(3分)

得
 (3分)
(3分)
得到传送带的速度 (2分)
(2分)
(2)零件在传送带上加速运动,设加速度为a2,运动时间为t1,位移为s1,由牛顿第二定律可得
 (2分)
(2分)
 加速时间为
加速时间为 (2分)
(2分)
匀加速运动的能移
设在传送带上匀速运动时间为
 (2分)
(2分)
设零件在斜面上向上运动时间为

 (1分)
(1分)
25、(18分)
(1)ab棒离开磁场右边界前做匀速运动
速度为, 则有
则有
 对ab棒
对ab棒 
解得: (6分)
(6分)
(2)由能量守恒可得:
得:W电=F(l0+l)- (6分)
(6分)
(3)设棒刚进入磁场时速度为v,由F?l0= mv2 可得
mv2 可得
棒在进入磁场前做匀加速直线运动,在磁场中运动可分三种情况讨论;
①若 则棒做匀速直线运动;(2分)
则棒做匀速直线运动;(2分)
②若 则棒先加速后匀速;(2分)
则棒先加速后匀速;(2分)
③若 则棒先减速后匀速。(2分)
则棒先减速后匀速。(2分)
26、(17分)(除特殊说明外,每空2分)
(1)释放神经递质
(2)T细胞活性下降后,呈递抗原信息的能力降低(1分),影响了B细胞增殖分化成浆细胞的过程(1分),使抗体生成量减少(1分)。
(3)激素、神经递质、淋巴因子(或其他合适的答案如CO2、H+,填2个1分,填3个2分)
通过细胞间的接触
(4)自身免疫病 过敏反应
(5)自身以外生物的合成 自身B淋巴细胞的合成
27、(16分)(除特殊说明外,每空2分)
(1)4 ; 1AA: 2Aa: 1aa (2)8%
(100%-[1/2×100%+1/4×88%+1/4×80%]=8%或20%×1/4+12%×1/4=8%)
(3)从窄叶植株上采种(含Aa、aa)(2分) 次年播种后,选择宽叶植株栽种(2分)
 |
(4)遗传图解:(符号和箭头都正确得1分,亲本基因型和表现型都正确得1分,配子正确得1分,F2基因型和表现型都正确得1分,F2基因型和表现型都正确得1分,语言叙述正确得1分)。
在F2中获取的宽叶甜玉米(Aabb)种子也就是我们需要的高产的甜玉米种子。
28.(1)H2 FeCl2 2分
(2)H++Cl →H Cl 2分
(3)b;Fe-2e=Fe2+ 各2分
(4)2Na2O2+2H2O=4NaOH+O2↑ 2分
(5)因为Na2O2溶于水生NaOH的同时生成氧气,碱与Fe2+反应生成的Fe(OH)2被氧化成Fe(OH)3(其他合理答案均给分)2分
 29.(1)
29.(1)
(2)N2H4+2NO=2N2+2H2O
(3)N2H4+H2O
 N2H5++OH-(不用“
N2H5++OH-(不用“
 ”不得分,写两步各1分)
”不得分,写两步各1分)
(4)N2H4+4OH-→N2↑+4H2O+4e-
(5)①减小(1分)②2H++2e→H2↑ 0.5
(6)N2H4 (1)+O2(g)=N2(g)+2H2O(1) △H=-621.23kJ?mol-1
(除注明,其余每空2分,共14分,其他合理答案均得分)
30.(1)B(1分) A(1分) C(1分)
CaCO3+2H+=Ca2++CO2↑+H2O (2分)
(2)①2Na+2CO2
 CO+Na2CO3 (3分)
CO+Na2CO3 (3分)
②4Na+3CO2
 2Na2CO3+C (3分)
2Na2CO3+C (3分)
(3)将残留物溶于适量水,若有黑色不溶物则证明残留物中有C,在溶液中加足量BaCl2溶液,然后过滤,在滤液中滴加几滴酚酞,若溶液变红,则证明残留物中含有Na2O(3分)
32.(1)CH4、SP3 正四面体 (2)分子 原子 (3)H2O (4)C (5)1s-2s22p63p63d10(每空1分,共8分)
33.(8分)(1)G:HO―CH2CH2CH2―OH
F:HOOC―CH2―COOH (2分)
(2)①消去反应 ④取代(水解)反应(2分)
(3)①Br―CH2CH2―COOH+2NaOH

 CH2=CH―COONa+NaBr+2H2O
CH2=CH―COONa+NaBr+2H2O
③CH2=CH-COOCH2CH2CH2Br+H2O

 CH2=CH-COOH+BrCH2CH2CH2OH(各2分)
CH2=CH-COOH+BrCH2CH2CH2OH(各2分)
34.(除特殊说明外,每空1分,共8分)
(1)菌落 (2)高压蒸汽灭菌法(2分) (3)B组 低 培养基中可能有两个或多个细菌紧挨在一起,共同形成一个菌落(2分) 灭菌
35.(除特殊说明外,每空1分,共8分)
(1)限制性核酸内切(或限制) 能识别特定的核苷酸序列并能在特定的位点切割(双链)DNA 分子(2分)
(2)一段有特殊结构的DNA片段 RNA聚合
(3)转基因技术、早期胚胎培养技术(动物细菌培养技术)、胚胎移植技术等(2分,写全给2分,写出其中2项或1项给1分)
(4)动物血清(浆)等
选修3―3
36.(8分)【物理―物理 3―3】
①设压缩后气体的压强为P,活塞的横截面积为S,10=
解出:p=2×105Pa (1分)
②大气压力对活塞做功W1=P0S(l0-l)=1J,人做功W2=10J,(1分)
由热力学第一定律:△U=W1+W2+Q (2分)
将Q=-2J等代入,解出△U=9J (1分)
 37.选修3―4
37.选修3―4
1.A
2.解析:①光在圆柱体中的传播速度

②设光线PC经折射后经过B点,光路图如所示
由折射定律有:
又由几何关系有: ②
②
解①②得
光线PC离直线AB的距离
则距离直线AB为 的入射光线经折射后能到达B点。
的入射光线经折射后能到达B点。
38.选修3―5
1.A
2.中子和氮核碰撞土家程遵循动量守恒定律,设中子质量为m,入射速度大小为v,反弹速度大小为v1,氮核获得的速度大小为v2,取中子入射方向为正方向,由动量守恒定律:

代入数据有:
解得: 
 已知X为中学化学中一种常见的盐,F为淡黄色固体;M、N为常见的金属,N的氧化物可作耐火材料,可用它来制造耐火坩埚和耐高温试验仪器;H为气体单质,D为无色气体,D在空气中会出现红棕色,各物质的转化关系如图,(部分反应产物已略去).
已知X为中学化学中一种常见的盐,F为淡黄色固体;M、N为常见的金属,N的氧化物可作耐火材料,可用它来制造耐火坩埚和耐高温试验仪器;H为气体单质,D为无色气体,D在空气中会出现红棕色,各物质的转化关系如图,(部分反应产物已略去).请回答下列问题;
(1)E的化学式为
(2)将M丝插入盛有X溶液的试管中,反应一段时间后的现象是:
(3)反应①②③④中属于置换反应的是
(4)反应②的离子方程式为
(5)用石墨作电极电解500mL X溶液,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;电解一段时间后,取出A电极,洗涤、干燥、称量,电极增重1.6g.
请回答下列问题:
①写出电解时的阳极反应式
②电解一段时间后转移
 已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).
已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).(1)若A和E为单质,组成A单质的元素是自然界中形成化合物种类最多的元素.
①B属于分子
②向50mL 4mol/L的NaOH溶液中通入1.12L B(标准状况),反应后溶液中溶质的物质的量之比为
③4g A单质完全燃烧放出131.2kJ的热量,写出表示A单质燃烧热的热化学方程式
(2)若A为第三周期中的元素所形成的氯化物.
①写出A溶液→B的离子方程式
②写出A和B的溶液反应的离子方程式
(3)若A为常见的金属,在E的冷、浓溶液中,A有钝化现象.已知:X为含有非极键的离子化合物,且1mol X含有38mol电子,向D溶液中加入与D等物质的量的X固体,恰好完全反应,写出该反应的离子方程式
(1)X元素的名称是
(2)X、Y、Z的原子半径从大到小的顺序是(用元素符号表示)
(3)写出F的电子式


(4)已知X单质、A、B、D均为固体,分别与E反应都生成同一种物质,其中X单质、A、B分别与E的反应均是氧化还原反应.请写出X单质、B分别与E反应的化学方程式
B中含有的化学键是
(5)请写出由化合物C制取Y的单质反应的化学方程式
 2H2O+O2↑
2H2O+O2↑ 2H2O+O2↑
2H2O+O2↑(1)写出XY2分子的电子式
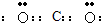
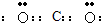
(2)Z的最高价氧化物对应水化物W是重要的化工原料.W的化学式为
工业制造W的生产过程主要分为三个阶段.
①在 101kPa时,3.2g Z的固体单质完全燃烧可放出29.7kJ的热量,写出能够表示该固体单质燃烧热的热化学方程式
②在接触氧化阶段,为提高ZY2的转化率,从理论上判断,应选择的条件是低温和高压.从下表给出不同温度、压强下ZY2平衡转化率的实验数据进行分析,结合工业生产的实际,应选择的适合的温度和压强是
A.400℃~500℃10MPa
B.400℃~500℃1MPa
C.500℃~500℃10MPa
D.400℃~500℃0.1MPa
| 压强/MPa 转化率/% 温度/℃ |
0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
A.水 B.0.5mol/L的硫酸 C.98.3%的硫酸 D.浓氨水
(3)已知X与XY都是工业上常用的还原剂.
①写出X单质与W的浓溶液反应的化学方程式
| ||
| ||
②500℃,11.2L(标准状况)ZY2在催化剂作用下与XY发生化学反应.若有2×6.02×1023个电子转移时,该反应的化学方程式是
| ||
| △ |
| ||
| △ |
| 元素 | 相关信息 |
| T | T原子所处的周期数、族序数分别与其原子序数相等 |
| X | X的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子数相同 |
| Z | Z可形成Z2、Z3两种气态单质 |
| Q | 在该元素所在周期中,Q的基态原子的第一电离能最小 |
| R | 3p能级上有1个电子 |
| W | W的一种核素的质量数为56,中子数为30 |
(2)X与Y原子结合形成的X3Y4晶体,其硬度比金刚石大,则X3Y4晶体中含有
(3)T、X两种元素组成的一种化合物M是重要的化工原料,常把它的产量作为衡量石油化工发展水平的标志,则M分子中σ键和π键的个数比为
(4)将amolQ单质与bmolR单质组成的固体混合物投入到足量的水中,若固体完全溶解最终得到澄清溶液,则同时产生的气体的物质的量为
(5)已知25℃、101kPa条件下:
4R(s)+3Z2(g) 2R2Z3(s)△H=-2834.9kJ/mol
4R(s)+2Z3(g) 2R2Z3(s)△H=-3119.1kJ/mol
则16g Z2(g)完全转化为Z3(g)的△H=