题目内容
 已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).
已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).(1)若A和E为单质,组成A单质的元素是自然界中形成化合物种类最多的元素.
①B属于分子
非极性
非极性
(填“极性”或“非极性”),B分子中各原子最外层是
是
(填“是”或“否”)都满足8电子结构;②向50mL 4mol/L的NaOH溶液中通入1.12L B(标准状况),反应后溶液中溶质的物质的量之比为
n(Na2CO3):n(NaOH)═1:2
n(Na2CO3):n(NaOH)═1:2
(填化学式和物质的量之比);③4g A单质完全燃烧放出131.2kJ的热量,写出表示A单质燃烧热的热化学方程式
C(s)+O2(g)=CO2(g);△H=-393.6kJ/mol
C(s)+O2(g)=CO2(g);△H=-393.6kJ/mol
.(2)若A为第三周期中的元素所形成的氯化物.
①写出A溶液→B的离子方程式
Al3++4OH-=AlO2-+2H2O
Al3++4OH-=AlO2-+2H2O
;②写出A和B的溶液反应的离子方程式
Al3++3AlO2-+6H2O=4Al(OH)3↓
Al3++3AlO2-+6H2O=4Al(OH)3↓
.(3)若A为常见的金属,在E的冷、浓溶液中,A有钝化现象.已知:X为含有非极键的离子化合物,且1mol X含有38mol电子,向D溶液中加入与D等物质的量的X固体,恰好完全反应,写出该反应的离子方程式
4Fe2++4Na2O2+6H2O=4Fe(OH)3+O2↑+8Na+
4Fe2++4Na2O2+6H2O=4Fe(OH)3+O2↑+8Na+
.分析:(1)由题意,若A和E为单质,组成A单质的元素是自然界中形成化合物种类最多的元素,确定A单质是碳,根据碳的化学性质及框图中A能和少量E与过量E反应生成两种含碳化合物B和D,可推测E是氧气,B为CO2、D为CO,再解答问题;
CO2通入NaOH溶液中发生两个反应:CO2+NaOH(少量)═NaHCO3、CO2+2NaOH(过量)═Na2CO3+H2O.根据CO2和NaOH量的关系,确定CO2少量,NaOH过量,最后溶质有Na2CO3和NaOH,求出物质的量之比即可;
热化学方程式书写要求标明各物质的状态、热量用△H表示、放热用符号“-”、吸热用符号“+”、单位为kJ/mol,各物质前的计量数表示物质的量,注意热量随着计量数而改变;
(2)若A为第三周期中的元素所形成的氯化物.可能为NaCl、MgCl2、AlCl3中的一种,根据A能和少量E与过量E反应生成两种化合物B和D,即可推断A为AlCl3,E为含OH-的碱,发生离子反应Al3++3OH-═Al(OH)3↓、Al3++4OH-=AlO2-+2H2O,确定出B中含有AlO2-,D为Al(OH)3;
(3)若A为常见的金属,在E的冷、浓溶液中,A有钝化现象.能发生钝化现象的金属有Fe和Al,即可确定A为Fe.结合A能和少量E与过量E反应生成两种化合物B和D,即可确定A为Fe,E为硝酸,硝酸具有强氧化性,铁与过量硝酸反应生成Fe3+,铁与少量硝酸反应生成Fe2+,所以B中含Fe3+,D中含Fe2+.根据已知信息,X为含有非极键的离子化合物,且1mol X含有38mol电子,非极性键是由两个相同非金属原子通过共用电子对形成的,常见的为-O-O-非极性键,氧原子含8个电子,2个氧原子共含16个电子,而X含有38mol电子,还相差22个电子,可考虑含2个Na,即得X为Na2O2.Na2O2具有强氧化性,可把Fe2+氧化成Fe3+,根据题意,向Fe2+溶液中加入与Fe2+等物质的量的Na2O2固体,恰好完全反应,反应过程可看成Na2O2先与水反应,生成的NaOH再与Fe2+反应,生成Fe(OH)2,最后Fe(OH)2再被氧化成Fe(OH)3.
CO2通入NaOH溶液中发生两个反应:CO2+NaOH(少量)═NaHCO3、CO2+2NaOH(过量)═Na2CO3+H2O.根据CO2和NaOH量的关系,确定CO2少量,NaOH过量,最后溶质有Na2CO3和NaOH,求出物质的量之比即可;
热化学方程式书写要求标明各物质的状态、热量用△H表示、放热用符号“-”、吸热用符号“+”、单位为kJ/mol,各物质前的计量数表示物质的量,注意热量随着计量数而改变;
(2)若A为第三周期中的元素所形成的氯化物.可能为NaCl、MgCl2、AlCl3中的一种,根据A能和少量E与过量E反应生成两种化合物B和D,即可推断A为AlCl3,E为含OH-的碱,发生离子反应Al3++3OH-═Al(OH)3↓、Al3++4OH-=AlO2-+2H2O,确定出B中含有AlO2-,D为Al(OH)3;
(3)若A为常见的金属,在E的冷、浓溶液中,A有钝化现象.能发生钝化现象的金属有Fe和Al,即可确定A为Fe.结合A能和少量E与过量E反应生成两种化合物B和D,即可确定A为Fe,E为硝酸,硝酸具有强氧化性,铁与过量硝酸反应生成Fe3+,铁与少量硝酸反应生成Fe2+,所以B中含Fe3+,D中含Fe2+.根据已知信息,X为含有非极键的离子化合物,且1mol X含有38mol电子,非极性键是由两个相同非金属原子通过共用电子对形成的,常见的为-O-O-非极性键,氧原子含8个电子,2个氧原子共含16个电子,而X含有38mol电子,还相差22个电子,可考虑含2个Na,即得X为Na2O2.Na2O2具有强氧化性,可把Fe2+氧化成Fe3+,根据题意,向Fe2+溶液中加入与Fe2+等物质的量的Na2O2固体,恰好完全反应,反应过程可看成Na2O2先与水反应,生成的NaOH再与Fe2+反应,生成Fe(OH)2,最后Fe(OH)2再被氧化成Fe(OH)3.
解答:解:(1)①由题意,若A和E为单质,组成A单质的元素是自然界中形成化合物种类最多的元素,确定A单质是碳,碳元素是自然界中形成化合物种类最多的元素.根据碳的化学性质及框图中A能和少量E与过量E反应生成两种含碳化合物B和D,可推测E是氧气,反应为C+O2(过量)
CO2,C+O2(少量)
2CO,即得B为CO2、D为CO.CO2中碳原子最外层4个电子,氧原子最外层6个电子,碳原子分别与两个氧原子各形成两对共用电子对,即电子式为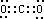 ,结构式为O═C═O,键角180°正电荷重心和负电荷重心重合,所以为非极性分子,由电子式可知CO2分子中各原子最外层都满足8电子结构.
,结构式为O═C═O,键角180°正电荷重心和负电荷重心重合,所以为非极性分子,由电子式可知CO2分子中各原子最外层都满足8电子结构.
故答案为:非极性;是;
②CO2通入NaOH溶液中发生两个反应:CO2+NaOH(少量)═NaHCO3、CO2+2NaOH(过量)═Na2CO3+H2O,
根据题意,n(NaOH)=4mol/L×0.05L=0.2mol,n(CO2)=
=0.05mol,可见NaOH过量,CO2全部反应掉,
发生反应CO2+2NaOH(过量)═Na2CO3+H2O.0.05molCO2消耗0.1molNaOH,生成0.05molNa2CO3,溶液中还剩余0.1molNaOH,
所以溶液中溶质为0.05molNa2CO3、0.1molNaOH,n(Na2CO3):n(NaOH)=1:2,
故答案为:n(Na2CO3):n(NaOH)═1:2;
③4g 碳单质,物质的量为1/3mol,完全燃烧放出131.2kJ的热量,则1mol碳单质完全燃烧放出131.2kJ×3的热量,热化学方程式为C(s)+O2(g)=CO2(g)△H=-393.6kJ/mol,
故答案为:C(s)+O2(g)=CO2(g)△H=-393.6kJ/mol;
(2)①若A为第三周期中的元素所形成的氯化物.可能为NaCl、MgCl2、AlCl3中的一种,根据A能和少量E或过量E反应生成两种化合物B和D,即可推断A为AlCl3,E为含OH-的碱,发生离子反应Al3++3OH-═Al(OH)3↓、Al3++4OH-=AlO2-+2H2O,确定出B中含有AlO2-,D为Al(OH)3.则A溶液→B的离子方程式为Al3++4OH-=AlO2-+2H2O,
故答案为:Al3++4OH-=AlO2-+2H2O;
②A为AlCl3,B中含有AlO2-,在两溶液中,Al3+和AlO2-都能发生水解反应,当两溶液混合后,Al3+和AlO2- 发生双水解反应生成氢氧化铝沉淀,反应为Al3++3AlO2-+6H2O=4Al(OH)3↓.
故答案为:Al3++3AlO2-+6H2O=4Al(OH)3↓;
(3)A为常见的金属,在E的冷、浓溶液中,A有钝化现象.能发生钝化现象的金属有Fe和Al,结合A能和少量E与过量E反应生成两种化合物B和D,即可确定A为Fe,E为硝酸,硝酸具有强氧化性,铁与过量硝酸反应生成Fe3+,铁与少量硝酸反应生成Fe2+,所以B中含Fe3+,D中含Fe2+.根据已知信息,X为含有非极键的离子化合物,且1mol X含有38mol电子,非极性键是由两个相同非金属原子通过共用电子对形成的,常见的为-O-O-非极性键,氧原子含8个电子,2个氧原子共含16个电子,而X含有38mol电子,还相差22个电子,可考虑含2个Na,即得X为Na2O2.Na2O2具有强氧化性,可把Fe2+氧化成Fe3+,根据题意,向Fe2+溶液中加入与Fe2+等物质的量的Na2O2固体,恰好完全反应,反应过程可看成Na2O2先与水反应,生成的NaOH再与Fe2+反应,生成Fe(OH)2,最后Fe(OH)2再被氧化成Fe(OH)3,反应方程式为2Na2O2+2H2O═4NaOH+O2↑、Fe2++2OH-═Fe(OH)2↓、4Fe(OH)2+O2+2H2O═4Fe(OH)3↓,上述三个反应合并即得总反应方程式为4Fe2++4Na2O2+6H2O=4Fe(OH)3+O2↑+8Na+.
故答案为:4Fe2++4Na2O2+6H2O=4Fe(OH)3+O2↑+8Na+.
| ||
| ||
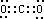 ,结构式为O═C═O,键角180°正电荷重心和负电荷重心重合,所以为非极性分子,由电子式可知CO2分子中各原子最外层都满足8电子结构.
,结构式为O═C═O,键角180°正电荷重心和负电荷重心重合,所以为非极性分子,由电子式可知CO2分子中各原子最外层都满足8电子结构.故答案为:非极性;是;
②CO2通入NaOH溶液中发生两个反应:CO2+NaOH(少量)═NaHCO3、CO2+2NaOH(过量)═Na2CO3+H2O,
根据题意,n(NaOH)=4mol/L×0.05L=0.2mol,n(CO2)=
| 1.12L |
| 22.4L/mol |
发生反应CO2+2NaOH(过量)═Na2CO3+H2O.0.05molCO2消耗0.1molNaOH,生成0.05molNa2CO3,溶液中还剩余0.1molNaOH,
所以溶液中溶质为0.05molNa2CO3、0.1molNaOH,n(Na2CO3):n(NaOH)=1:2,
故答案为:n(Na2CO3):n(NaOH)═1:2;
③4g 碳单质,物质的量为1/3mol,完全燃烧放出131.2kJ的热量,则1mol碳单质完全燃烧放出131.2kJ×3的热量,热化学方程式为C(s)+O2(g)=CO2(g)△H=-393.6kJ/mol,
故答案为:C(s)+O2(g)=CO2(g)△H=-393.6kJ/mol;
(2)①若A为第三周期中的元素所形成的氯化物.可能为NaCl、MgCl2、AlCl3中的一种,根据A能和少量E或过量E反应生成两种化合物B和D,即可推断A为AlCl3,E为含OH-的碱,发生离子反应Al3++3OH-═Al(OH)3↓、Al3++4OH-=AlO2-+2H2O,确定出B中含有AlO2-,D为Al(OH)3.则A溶液→B的离子方程式为Al3++4OH-=AlO2-+2H2O,
故答案为:Al3++4OH-=AlO2-+2H2O;
②A为AlCl3,B中含有AlO2-,在两溶液中,Al3+和AlO2-都能发生水解反应,当两溶液混合后,Al3+和AlO2- 发生双水解反应生成氢氧化铝沉淀,反应为Al3++3AlO2-+6H2O=4Al(OH)3↓.
故答案为:Al3++3AlO2-+6H2O=4Al(OH)3↓;
(3)A为常见的金属,在E的冷、浓溶液中,A有钝化现象.能发生钝化现象的金属有Fe和Al,结合A能和少量E与过量E反应生成两种化合物B和D,即可确定A为Fe,E为硝酸,硝酸具有强氧化性,铁与过量硝酸反应生成Fe3+,铁与少量硝酸反应生成Fe2+,所以B中含Fe3+,D中含Fe2+.根据已知信息,X为含有非极键的离子化合物,且1mol X含有38mol电子,非极性键是由两个相同非金属原子通过共用电子对形成的,常见的为-O-O-非极性键,氧原子含8个电子,2个氧原子共含16个电子,而X含有38mol电子,还相差22个电子,可考虑含2个Na,即得X为Na2O2.Na2O2具有强氧化性,可把Fe2+氧化成Fe3+,根据题意,向Fe2+溶液中加入与Fe2+等物质的量的Na2O2固体,恰好完全反应,反应过程可看成Na2O2先与水反应,生成的NaOH再与Fe2+反应,生成Fe(OH)2,最后Fe(OH)2再被氧化成Fe(OH)3,反应方程式为2Na2O2+2H2O═4NaOH+O2↑、Fe2++2OH-═Fe(OH)2↓、4Fe(OH)2+O2+2H2O═4Fe(OH)3↓,上述三个反应合并即得总反应方程式为4Fe2++4Na2O2+6H2O=4Fe(OH)3+O2↑+8Na+.
故答案为:4Fe2++4Na2O2+6H2O=4Fe(OH)3+O2↑+8Na+.
点评:本题考查元素化合物的推断,解题关键是根据已知信息结合化合物的性质分析、尝试确定各物质,各物质确定后抓住化学性质解决问题.本题涉及知识点较多,难度较大.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
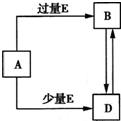 已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).下列说法错误的是( )
已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).下列说法错误的是( )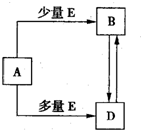 已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).
已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).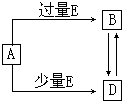 已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).
已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).