网址:http://m.1010jiajiao.com/timu_id_78695[举报]
22. (1)交流电源(或电源)
(1)交流电源(或电源)
(2)
平衡摩擦力
(3)B
(4)GK(学生只要取匀速部分均为正确)
(5)
作图:要求明确标注坐标轴的物理量,合理设置标度,并用尺规作图
所作图线应通过原点,
在误差容许的范围内,图像是经过原点的直线,说明Wn与vn2成正比
23.(1)依题知,木块受到的滑动摩擦力f为3.12N
而 


(2)木块受力如图所示,根据牛顿第二定律有
 1
1
而 2
2
联立12式并代入数据解得:F=8.7N
24.

25.解:(1)风轮机可接收的风能为
 ①
①
 ②
②
每秒钟接收的风能为
 ③
③
由①②③得
 ④
④
(2)发电机功率为
 ⑤
⑤
由④⑤得

代入数据得
r=7.0m
(3)可增加风轮叶片长度 安装调向装置,以保证风轮机与风速垂直等
(其他答案合理的也给分)
26.(1)E: CH =CHCOOH: G:CH
=CHCOOH: G:CH =CHCOOCH
=CHCOOCH ;
;
(2)HCOOCH CH=CH
CH=CH ;
CH
;
CH COOCH=CH
COOCH=CH 。
。
(3)CH COCO CH
COCO CH
(4)X:加成反应;Y:消去反应;
(5)①HC≡CH+CO+H O
O H
H C=CHCOOH
C=CHCOOH
②CH CH
CH COOH+CH
COOH+CH OH
OH
 CH
CH CH
CH COOCH
COOCH +H
+H O
O
27.(1)A . H O
E . N2 F
. Ag K. AgCl ;
O
E . N2 F
. Ag K. AgCl ;
(2)4NH3+5O2 4NO+6H2O
4NO+6H2O
(3) 
(4)  + 2
+ 2  + NO3- ==
+ NO3- ==  +
NO2↑ + H2O
+
NO2↑ + H2O
28.(1) (略) 、 减小。 (2) A B
(3) -33.42 NH3 (4) N2 H2
29. (1) BaSO4(s) Ba2+(aq)+ SO42-(aq)
Ba2+(aq)+ SO42-(aq)
[Ba2+] = 1.05 × 10-5mol?L-1 < 2×10-3 mol?L-1
胃液中H+ 对BaSO4的沉淀溶解平衡没有影响,因此BaSO4可用做“钡餐”。
(2)BaCO3(s) Ba2+(aq)+
CO32-(aq),由于胃液是酸性的,如果服下BaCO3,胃酸可与CO32-反应生成二氧化碳和水,使CO32-的浓度降低,从而使BaCO3的沉淀溶解平衡向右移动,使Ba2+浓度增大而引起人体中毒。
Ba2+(aq)+
CO32-(aq),由于胃液是酸性的,如果服下BaCO3,胃酸可与CO32-反应生成二氧化碳和水,使CO32-的浓度降低,从而使BaCO3的沉淀溶解平衡向右移动,使Ba2+浓度增大而引起人体中毒。
30.Ⅰ(1)光合作用 二氧化碳 (2)蒸腾 (3)A组用自来水配制的,自来水中可能含有植物必需的矿质元素,植物能正常生长.B组是用蒸馏水配制的,蒸馏水中缺少植物必须的矿质元素,植物不能正常生长。(4)铁
Ⅱ培育AABB采用单倍体育种方法:
过程: AAbb x aaBB
↓
AaBb
配子AB Ab aB ab
单倍体AB Ab aB ab
个体AABB AAbb aaBB aabb
若用杂交育种的方法表现型为双显个体中AABB仅占1/9,要确定是否为纯合体必须自交才能确定。
培育ddee采用杂交育种的方法:
过程:
P DDee x ddEE
↓
F DdEe
F2 D__E__ D__ee ddE__ ddee
隐性性状出现就可以确定为纯合体
31.(1)②线粒体 ⑥核糖体 (2)B细胞或记忆细胞 抗体 (3)组织液、血浆 (4)胰高血糖素
(5)中心体 (6)动物血清 细胞系 (7)46
工业上合成氨是在一定条件下进行如下反应:N2(g)+3H2(g)
 2NH3(g),△H = -92.44kJ/mol;其部分工艺流程如下
2NH3(g),△H = -92.44kJ/mol;其部分工艺流程如下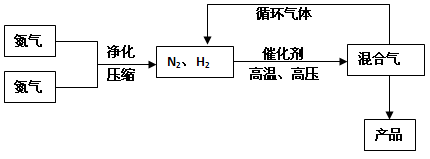
(1)写出该反应的化学平衡常数表达式:K=__________。随着温度的升高,K值_______(填增大、减小、不变)。
(2)平衡常数K值越大,表明__________(填序号)。
A.N2的转化率越高
B.NH3的产率越大
C.原料中N2的含量越高
D.化学反应速率越快
(3)合成氨反应的平衡常数很小,所以在工业上采取气体循环的流程。即反应后通过把混合气体的温度降低到__________使__________分离出来;继续循环的气体是_______。
工业上合成氨是在一定条件下进行如下反应:
N2(g)+3H2(g)![]() 2NH3(g),△H=-92.2kJ/mol;其部分工艺流程如下:
2NH3(g),△H=-92.2kJ/mol;其部分工艺流程如下:

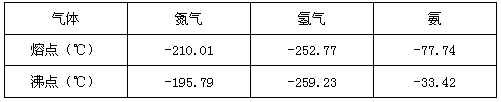
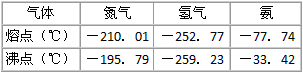
反应体系中各组分的部分性质见下表:
| 气体 | 氮气 | 氢气 | 氨 |
| 熔点(℃) | -210.01 | -252.77 | -77.74 |
| 沸点(℃) | -195.79 | -259.23 | -33.42 |
回答下列问题:
(1)写出该反应的化学平衡常数表达式:K= 。随着温度升高,
K值 (填增大、减小、不变)。
(2)平衡常数K值越大,表明 (填序号)。
A.N2的转化率越高 B.NH3的产率越大
C.原料中N2的含量越高 D.化学反应速率越快
(3)合成氨反应的平衡常数很小,所以在工业上采取气体循环的流程。即反应后通过把混合气体的温度降低到 使 分离出来;继续循环的气体是 。
查看习题详情和答案>>工业上合成氨是在一定条件下进行如下反应:
N2(g)+3H2(g)2NH3(g),△H=-92.2kJ/mol;其部分工艺流程如下:
反应体系中各组分的部分性质见下表:
| 气体 | 氮气 | 氢气 | 氨 |
| 熔点(℃) | -210.01 | -252.77 | -77.74 |
| 沸点(℃) | -195.79 | -259.23 | -33.42 |
回答下列问题:
(1)写出该反应的化学平衡常数表达式:K= 。随着温度升高,
K值 (填增大、减小、不变)。
(2)平衡常数K值越大,表明 (填序号)。
A.N2的转化率越高 B.NH3的产率越大
C.原料中N2的含量越高 D.化学反应速率越快
(3)合成氨反应的平衡常数很小,所以在工业上采取气体循环的流程。即反应后通过把混合气体的温度降低到 使 分离出来;继续循环的气体是 。
查看习题详情和答案>>
工业上合成氨是在一定条件下进行如下反应:
N2(g)+3H2(g)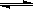 2NH3(g),△H=-92.2kJ/mol;其部分工艺流程如下:
2NH3(g),△H=-92.2kJ/mol;其部分工艺流程如下:

反应体系中各组分的部分性质见下表:
|
气体 |
氮气 |
氢气 |
氨 |
|
熔点(℃) |
-210.01 |
-252.77 |
-77.74 |
|
沸点(℃) |
-195.79 |
-259.23 |
-33.42 |
回答下列问题:
(1)写出该反应的化学平衡常数表达式:K= 。随着温度升高,
K值 (填增大、减小、不变)。
(2)平衡常数K值越大,表明 (填序号)。
A.N2的转化率越高 B.NH3的产率越大
C.原料中N2的含量越高 D.化学反应速率越快
(3)合成氨反应的平衡常数很小,所以在工业上采取气体循环的流程。即反应后通过把混合气体的温度降低到 使 分离出来;继续循环的气体是 。
查看习题详情和答案>>
 2NH3(g),△H=-92.2kJ/mol;其部分工艺流程如下
2NH3(g),△H=-92.2kJ/mol;其部分工艺流程如下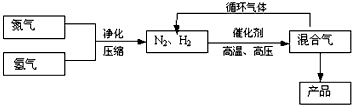
(1)写出该反应的化学平衡常数表达式:K=___________。随着温度升高,K值___________(填增大、减小、不变)。
(2)平衡常数K值越大,表明___________(填序号)。
A.N2的转化率越高
B.NH3的产率越大
C.原料中N2的含量越高
D.化学反应速率越快
(3)合成氨反应的平衡常数很小,所以在工业上采取气体循环的流程。即反应后通过把混合气体的温度降低到___________使___________分离出来;继续循环的气体是___________。