题目内容
(三选一)【化学--化学与技术】
工业上合成氨是在一定条件下进行如下反应:N2(g)+3H2(g) 2NH3(g),△H = -92.44kJ/mol;其部分工艺流程如下
2NH3(g),△H = -92.44kJ/mol;其部分工艺流程如下
工业上合成氨是在一定条件下进行如下反应:N2(g)+3H2(g)
 2NH3(g),△H = -92.44kJ/mol;其部分工艺流程如下
2NH3(g),△H = -92.44kJ/mol;其部分工艺流程如下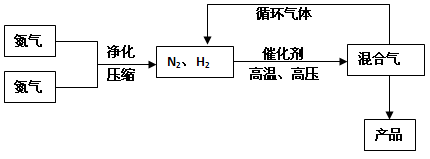
反应体系中各组分的部分性质见下表:
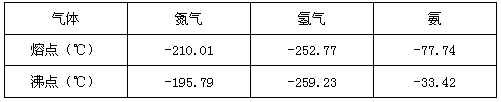
回答下列问题:
(1)写出该反应的化学平衡常数表达式:K=__________。随着温度的升高,K值_______(填增大、减小、不变)。
(2)平衡常数K值越大,表明__________(填序号)。
A.N2的转化率越高
B.NH3的产率越大
C.原料中N2的含量越高
D.化学反应速率越快
(3)合成氨反应的平衡常数很小,所以在工业上采取气体循环的流程。即反应后通过把混合气体的温度降低到__________使__________分离出来;继续循环的气体是_______。
(1)写出该反应的化学平衡常数表达式:K=__________。随着温度的升高,K值_______(填增大、减小、不变)。
(2)平衡常数K值越大,表明__________(填序号)。
A.N2的转化率越高
B.NH3的产率越大
C.原料中N2的含量越高
D.化学反应速率越快
(3)合成氨反应的平衡常数很小,所以在工业上采取气体循环的流程。即反应后通过把混合气体的温度降低到__________使__________分离出来;继续循环的气体是_______。
(1) ;减小
;减小
(2)AB
(3)-33.42℃;氨;N2、H2
 ;减小
;减小(2)AB
(3)-33.42℃;氨;N2、H2

练习册系列答案
相关题目

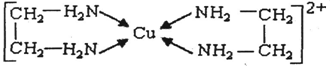

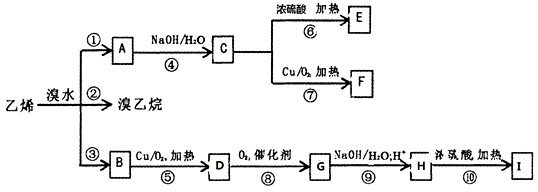
 ,I的分子式为C4H4O4,是一种环状化合物。请回答下列问题:
,I的分子式为C4H4O4,是一种环状化合物。请回答下列问题:
 MnFe2O4-x+O2↑、MnFe2O4-x+xH2O →MnFe2O4+xH2↑,请认真分析上述两个反应并回答下列问题:
MnFe2O4-x+O2↑、MnFe2O4-x+xH2O →MnFe2O4+xH2↑,请认真分析上述两个反应并回答下列问题: 