摘要: 玉溪一中高2010届高二上学期期末化学考试答案第Ⅰ 卷
网址:http://m.1010jiajiao.com/timu_id_555238[举报]
在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命.下表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
(1)下列“鲜花保鲜剂”的成分中,属于非电解质的是
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)配制上述“鲜花保鲜剂”所需的仪器有:烧杯、玻璃棒、药匙、
(3)在溶液配制过程中,下列操作对配制结果没有影响的是
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(4)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为
查看习题详情和答案>>
| 成分 | 质量(g) | 摩尔质量(g?mol-1) |
| 蔗糖 | 25.00 | 342 |
| 硫酸钾 | 0.87 | 174 |
| 阿司匹林 | 0.17 | 180 |
| 高锰酸钾 | 0.316 | 158 |
| 硝酸银 | 0.02 | 170 |
A
A
.A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)配制上述“鲜花保鲜剂”所需的仪器有:烧杯、玻璃棒、药匙、
托盘天平
托盘天平
、胶头滴管
胶头滴管
、500mL容量瓶
500mL容量瓶
.(在横线上填写所缺仪器的名称)(3)在溶液配制过程中,下列操作对配制结果没有影响的是
BD
BD
.A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(4)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为
0.024
0.024
mol/L.(写出简要计算过程) Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大;W与Q按1:4形成的化合物A是一种重要能源;W与Y,X与Y组成的化合物是常见的大气污染物;Y与Z按1:1形成的离子化合物B,其摩尔质量为78g?mol-1.请回答下列问题.
Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大;W与Q按1:4形成的化合物A是一种重要能源;W与Y,X与Y组成的化合物是常见的大气污染物;Y与Z按1:1形成的离子化合物B,其摩尔质量为78g?mol-1.请回答下列问题.(1)W在元素周期表中的位置
(2)写出A完全燃烧的化学方程式
(3)将盛有12mL XY2和Y2的混合气体的量筒倒立于水槽中,充分反应后,剩余2mL 无色气体,若该剩余气体为XY,计算原混合气体中Y2的体积
(4)WQ4Y是21世纪新型燃料,可通过WY和Q2化合生成,该反应的化学方程式为
将一定质量的Mg-A1合金投入100mL一定物质的量浓度的某HCl溶液中,充分反应.向反应后的溶液中逐滴加入一定物质的量浓度的NaOH溶液,生成沉淀的质量与所加NaOH溶液的体积关系如右图.计算下列问题:(写出简要计算过程) 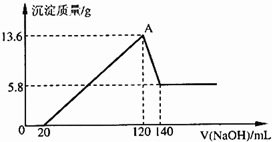
(1)求合金中Mg与Al的物质的量之比?
(2)所加NaOH溶液的物质的量浓度是多少?
(3)原HCl溶液的物质的量浓度是多少?
查看习题详情和答案>>

(1)求合金中Mg与Al的物质的量之比?
(2)所加NaOH溶液的物质的量浓度是多少?
(3)原HCl溶液的物质的量浓度是多少?
 右图是我校化学实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.计算:(要求写出简要计算过程)
右图是我校化学实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.计算:(要求写出简要计算过程)①求该浓硫酸的物质的量浓度?
②用该浓硫酸配制200mL1mol/L的稀硫酸,量筒所需量取该浓硫酸的体积是多少mL?
(2012?江苏一模)锂/磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,其制备方法如下:称取适量的Na3PO4?12H2O和CuSO4?5H2O分别溶解在蒸馏水中,充分搅拌,转入反应釜中,调节溶液pH为7~9,密封,放入130°烘箱中反应4h.自然冷却到室温,过滤,所得沉淀分别用蒸馏水和乙醇洗涤数次,干燥,得到产品.反应原理为:
2Na3PO4+4CuSO4+2NH3?H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)用蒸馏水洗涤时,检验洗涤是否完全的方法是
(2)电池放电时,负极锂转化为Li2O,正极磷酸铜转变为Cu和Li3PO4,写出该电池反应的方程式
(3)准确称取上述样品1.928g[假定只含Cu4O(PO4)2和CuO两种物质],使其完全溶于一定量硝酸中,再加氢氧化钠溶液,使铜完全沉淀,将沉淀灼烧使其转变为黑色氧化铜,最终称得残留固体质量为1.360g.计算得样品中磷酸氧铜(摩尔质量为:462g/mol)的质量分数(写出简要计算过程和结果)
查看习题详情和答案>>
2Na3PO4+4CuSO4+2NH3?H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)用蒸馏水洗涤时,检验洗涤是否完全的方法是
取最后一次洗涤的流出液,向其中加入氯化钡溶液,若无白色沉淀,说明已经洗涤干净
取最后一次洗涤的流出液,向其中加入氯化钡溶液,若无白色沉淀,说明已经洗涤干净
;最后用乙醇洗涤的目的是快速干燥固体
快速干燥固体
.(2)电池放电时,负极锂转化为Li2O,正极磷酸铜转变为Cu和Li3PO4,写出该电池反应的方程式
Cu4O(PO4)2+8Li=4Cu+Li2O+2Li3PO4
Cu4O(PO4)2+8Li=4Cu+Li2O+2Li3PO4
.(3)准确称取上述样品1.928g[假定只含Cu4O(PO4)2和CuO两种物质],使其完全溶于一定量硝酸中,再加氢氧化钠溶液,使铜完全沉淀,将沉淀灼烧使其转变为黑色氧化铜,最终称得残留固体质量为1.360g.计算得样品中磷酸氧铜(摩尔质量为:462g/mol)的质量分数(写出简要计算过程和结果)