题目内容
 右图是我校化学实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.计算:(要求写出简要计算过程)
右图是我校化学实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.计算:(要求写出简要计算过程)①求该浓硫酸的物质的量浓度?
②用该浓硫酸配制200mL1mol/L的稀硫酸,量筒所需量取该浓硫酸的体积是多少mL?
分析:①根据c=
计算浓硫酸的物质的量浓度;
②根据溶液稀释前后溶质的物质的量不变计算.
| 1000ρw |
| M |
②根据溶液稀释前后溶质的物质的量不变计算.
解答:解:①c=
=
=18.4 mol/L,
答:该浓硫酸的物质的量浓度为18.4 mol/L.
②溶液稀释前后溶质的物质的量不变,设需浓硫酸的体积为V,
则有:0.2L×1mol/L=V×18.4mol/L,
V=
=0.0109L,即10.9ml,
答:量筒所需量取该浓硫酸的体积是10.9 ml.
| 1000ρw |
| M |
| 1000×1.84g/L×98% |
| 98g/mol |
答:该浓硫酸的物质的量浓度为18.4 mol/L.
②溶液稀释前后溶质的物质的量不变,设需浓硫酸的体积为V,
则有:0.2L×1mol/L=V×18.4mol/L,
V=
| 0.2L×1mol/L |
| 18.4mol/L |
答:量筒所需量取该浓硫酸的体积是10.9 ml.
点评:本题考查物质的量浓度的相关计算,题目难度不大,注意相关物理量的计算公式的运用.

练习册系列答案
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案
相关题目

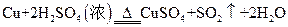 反应中,
反应中, 反应中,若有3.2 g的Cu参与反应,则被还原的H2SO4的物质的量是 mol.
反应中,若有3.2 g的Cu参与反应,则被还原的H2SO4的物质的量是 mol.

 反应中,
反应中,