网址:http://m.1010jiajiao.com/timu_id_49703[举报]
第Ⅰ卷
一、选择题,二、多选题
题号
1
2
3
4
5
6
7
8
9
10
答案
B
C
C
D
A
B
B
C
B
A
题号
11
12
13
14
15
16
17
18
19
20
21
答案
D
C
B
B
BC
ACD
B
AD
C
B
C
第Ⅱ卷
22(一)
(1)频率相同、位相差恒定………2分
(2)暗条纹…………………………2分
(3)19.22,  ………4分
………4分
(二)⑴A2………(2分)
V2………(2分)
⑵ ………(3分);
………(3分);
⑶ ………(2分),
………(2分),
U2表示电压表V2的示数,I2表示电流A2的示数.rV2表示电压表V2的内阻. ………(1分)
23、(16分)
解:由于月球引力提供向心力
 (4分)
(4分)
 (2分)
(2分)
由于地球引力提供月球运动的向心力
 (4分)
(4分)
 (2分)
(2分)
 (4分)
(4分)
24.解:(20分)①ab导体棒运动的最大速度时:
mgSinθ=BIι…………………………2分
I=BιV/3R…………………………………2分
 ………………………2分
………………………2分
②ab导体棒匀速运动时重力的功率、
P1=
V mgSinθ= ………………………3分
………………………3分
整个回路的电功率
P2= ………………………………3分
………………………………3分
通过计算说明是等大。
③对cd分析Mg= 2mgSinθ+ 2BIι= 4mgSinθ…………………3分
M≥4mSinθ…………………………………………………………3分
25.解:(18分)①对n个小车m和M用动量守恒定律
mV0=nmV1=(nm+M)V2………………………6分
物体的加速度a=μg………………………3分
t= ………………………3分
………………………3分
②由能量关系得μMgnL= ………………………4分
………………………4分
 ………………………4分
………………………4分
 26.(14分)
26.(14分)
⑴. (2分)
直线型 极性 极性 非极性(4分)
(2)③ ② (2分) (3)CH4 NH3 NH3 (3分)
⑷.3SO2
+ 2NO + 3Ba2+ + 2H2O
==== 3BaSO4 ↓ + 2NO + 4H+
(2分)SO2 (1分)
+ 3Ba2+ + 2H2O
==== 3BaSO4 ↓ + 2NO + 4H+
(2分)SO2 (1分)
27.(10分) (1)SO3 (1分)

(2) (2分)
(3)2Na2O2+2H2O
4Na++4OH-+O2↑ (2分) (4)Fe2O3+6H+ 2Fe3++3H2O (2分)
(5)FeS2(s)+11/4O2(g)
1/2 Fe2O3(s)+2SO2(g);△H=-852
kJ/mol (3分)
28.(18分)(1)Zn + 2H+ === Zn2+ + H2↑ (2分)
(2)装置I的不足是通过气体中含有HCl气体;装置II制备CaH2的装置后没有干燥装置。(各3分) (3)CB(4分)
(4)(不加热情况下)通氢气排完整套装置里的空气;验纯;点燃未反应的氢气。(不分前后)(4分) (5)CaH2 + 2H2O === Ca(OH)2 +H2↑(2分)]
 29.(16分)
29.(16分)
(1)
A; C (各2分)
(2) (3分)

(3)(各3分)

(4)(3分)
 或
或 
30.(16分,每空2分)
(1)第五组(或答含H2O + N + P + Mg + K的培养液)。
(2) 光照强度、温度、溶液通气状况等(至少写两种)但不能将“加入土壤”也作为变量)。
(3)每组栽培相同数量多株(必须两株以上,答一株者不给分)同种长势相同的植物;将五组植物放在相同适宜的光照、温度等条件下培养 。
(4) 4 。硫和钙(或S 、Ca) 。
(5) 溶液培养法(或无土栽培) 。
(6) 二氧化碳 。
31.(26分)
(Ⅰ)(12分,每空2分):
 (1)
(1)
。
(2)( D )
(3)① 单链 (或是合成蛋白质的模板)。
② 含有U(或尿嘧啶),不含T(胸腺嘧啶) 。
(4)( C )
(5) 1 。
(Ⅱ)(14分,每空2分)(1)___2___. (2) AaXBXb . _ AaXBY _。
(3) 1/ 3 , 5/24 . (4) B、E 、 C、F (两组答案不能互换)。
(1)写出下列元素符号:A
(2)用电子式表示B和F形成化合物的过程:


(3)写出A、C、F三种元素最高价氧化物对应的水化物相互反应的化学方程式:
(1)常见化合物W由A、D、E三种元素组成,则W中含有的化学键类型有
(2)X、Y、Z三种常见化合物均有A、C、D三种元素组成,X和Z的水溶液呈酸性,Y的水溶液呈碱性,在溶液中,X促进水的电离,Y和Z抑制水的电离,则它们的化学式分别是:X
(3)用A2D2在酸性条件下处理含BC-的工业废水,将得到C2及BD2等无污染的物质,请写出该反应的离子方程式
| 化合物 | 甲 | 乙 | 丙 |
| 各元素原子个数比 | n(A):n(C)=2:1 | n(A):n(C)=1:1 | n(B):n(A)=1:4 |
| 化合物 | 丁 | 戊 | 己 |
| 各元素原子个数比 | n(D):n(B):n(C)=2:1:3 | n(E):n(F)=1:3 | n(B):n(F)=1:4 |
(1)乙的电子式:
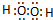
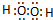
(2)D的离子结构示意图


(3)8g 丙完全燃烧,生成液态水和CO2,放出445kJ的热量,则丙燃烧的热化学方程式为
(4)F的单质与甲反应的离子方程式为
(5)将丁与戊两种水溶液混合,发生反应的离子方程式为
(1)B的单质分子的结构式为
(2)A元素形成的同素异形体的晶体类型可能是(填序号)
①离子晶体 ②原子晶体 ③金属晶体 ④分子晶体
(3)A、B、C形成的10电子氢化物中,A、B、C的氢化物沸点最高的是(写化学式)
(1)F+的价层电子排布为
(2)B、D形成一种超硬、耐磨、耐高温的新型化合物,该化合物化学式为
由氢气与C2反应生成1mol气态H2C产物,放热241.8KJ,若1g 气态H2C转化成液态H2C放热2.444KJ,则反应:2H2(g)+C2(g)=2H2C(L)的△H=
(3)C与氢元素形成的正一价离子含有10电子,该离子中C原子的杂化方式为
(4)1molAC2分子中σ键与π键的数目之比为