网址:http://m.1010jiajiao.com/timu_id_4425878[举报]
(一)(3分)下列实验操作不正确的是 _。
A.在催化剂存在的条件下, 苯和溴水发生反应可生成无色、![]() 比水重的液体溴苯
比水重的液体溴苯
B.将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,
完成乙醇氧化为乙醛的实验
C.醇中含有少量水可加入硫酸铜再蒸馏制得无水乙醇
D.试管中先加入一定量浓硫酸,再依次加入适量浓硝酸、苯,然后加热制取硝基苯
E.实验室制取乙烯时,放入几片碎瓷片,以避免混合液在受热沸腾时剧烈跳动
F.配制银氨溶液时,将稀氨水慢慢滴入硝酸银溶液中,产生沉淀后继续滴加到沉淀
刚好溶解为止
G.验证溴乙烷水解产![]() 物时,将溴乙烷和氢氧化钠溶液混合,充分振荡溶液、静置、
物时,将溴乙烷和氢氧化钠溶液混合,充分振荡溶液、静置、
待液体分层后,滴加硝酸银溶液
(二)(7分)乙醇分子中的羟基在一定条件下可以被氧化为醛基,为验证此性质,有关实验如下:
(1)在试管中加入2mL乙醇,把一端弯成螺旋状的铜丝在酒精灯外焰加热后立即插入乙醇中,反复操作几次后把铜丝晾干称重,发现其质量未发生变化,由此可推测铜丝的作用是 ,反应方程式为: 。
 (2)某化学兴趣小组认为上述实验操作简单,但
(2)某化学兴趣小组认为上述实验操作简单,但
通过实验得到的信息量较少。他们对此实验
进行了完善(如图,夹持仪器略去)。指导老师首先肯定了同学们的学习积极性,并提出
以下意见:
优点:实验原理正确,相对实验(1)而言,在
反应产物的检验方面有较大改进。
缺点:加热时乙醇汽化速率不易控制,有可能
造成C装置中产生倒吸现象。
注意:B装置若加热温度过高,可能存在安全隐患!
同学们因此又对实验进行研讨和改进:
① A处采用了水浴加热的方式,这样做的好处是:
② C装置可改用以下 装置(填字母)。

③ 实验时可对B部分采取合理的操作方法以防止安全隐患,请对此提出你的意见:
查看习题详情和答案>>
反应分两步进行:
第一步,乙醇与浓硫酸共热到170℃生成乙烯(CH3CH2OH
| H2SO4(浓) |
| 170℃ |
第二步,乙烯与溴生成1,2-二溴乙烷(CH2=CH2+Br2→BrCH2CH2Br).
可能存在的副反应有:乙醇在浓硫酸的存在下于l40℃脱水生成乙醚(C2H5-O-C2H5);温度过高,乙醇与浓硫酸反应生成SO2、CO2等酸性气体.
有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | 溴 | |
| 色、态 | 无色液体 | 无色液体 | 无色液体 | 深红棕色液体 |
| 密度/(g?cm-3) | 0.79 | 2.2 | 0.71 | 3.1 |
| 沸点/℃ | 78.5 | 132 | 34.6 | 59.47 |
| 熔点/℃ | -130 | 9 | -116 | -7.25 |
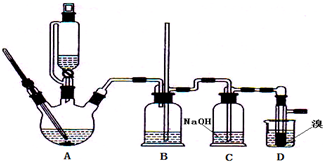
回答下列问题:
(1)熔沸点:乙醇>乙醚.利用物质结构的相关知识解释原因
(2)组装好仪器后检查A、B、C装置气密性的操作是
(3)如果D中导气管发生堵塞事故,装置B中可能观察到的现象是
(4)装置C中可能发生反应的化学方程式是
(5)将1,2-二溴乙烷粗产品置于分液漏斗中,加水,振荡后静置,产物应在
a.水 b.氢氧化钠溶液 c.乙醇
(6)若产物中有少量副产物乙醚,可采用的除杂方法是
(7)反应时装置D的烧杯中应装
a.冷水 b.冰水. 查看习题详情和答案>>
| 实验步骤 | 实验现象 |
| I.向编号为①②③的3支试管中,分别加入1mL 20%的蔗糖溶液,向试管②和③中加入0.5mL稀硫酸,并将这3支试管同时水浴加热约5min | 均无明显现象 |
| II.取试管①和②,加入新制氢氧化铜悬浊液,加热至沸腾 | 均无明显现象 |
| III.取试管③,先加入NaOH溶液调溶液pH至碱性,再加入新制氢氧化铜悬浊液,加热至沸腾 | |
| 结论:证明蔗糖在稀硫酸作用下发生了水解反应 | |
①试管a中生成乙酸乙酯的化学反应方程式是
②试管b中盛放的试剂是
③若要把b中制得的乙酸乙酯从混合物中分离出来,应采用的实验操作是
④生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态.下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号)
a单位时间里,生成1mol乙酸乙酯,同时生成1mol水
b单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
c单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
d正反应的速率与逆反应的速率相等
e混合物中各物质的浓度不再变化
(3)加热聚丙烯塑料得到的产物如表:
| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
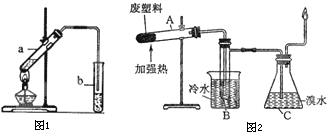
①试管A中的最终残余物为
②试管B收集到的产品中,有能使酸性高锰酸钾溶液褪色的物质,该物质的一氯代物有
③锥形瓶C中观察到的现象是
A.《化学与生活》
(1)食品和药品关系人的生存和健康.
①市场上销售的食盐品种很多.下列食盐中,所添加的元素不属于人体必需微量元素的是
A.加锌盐 B.加碘盐 C.加钙盐
②纤维素被称为“第七营养素”.食物中的纤维素虽然不能为人体提供能量,但能促进肠道蠕动、吸附排出有害物质.从化学成分看,纤维素是一种
A.多糖 B.蛋白质 C.脂肪
③某同学感冒发烧,他可服用下列哪种药品进行治疗
A.麻黄碱 B.阿司匹林 C.抗酸药
(2)蛋白质是生命的基础,没有蛋白质就没有生命.请回答下列问题:
①油脂被摄入人体后,在酶的作用下水解为高级脂肪酸和
②人体摄入的蛋白质在胃蛋白酶和胰蛋白酶的作用下,水解成
③维生素C是一种重要维生素,能防治坏血病.用淀粉溶液、碘水为试剂,验证维生素C具有还原性的实验操作和现象是
(3)材料是人类赖以生存和发展的重要物质基础.
①普通玻璃是生活中常用的硅酸盐材料,其主要成分是Na2SiO3、CaSiO3和
| ||
| ||
②通常使用的钢铁是铁和
③天然橡胶(生胶)是线型高分子,因高分子链上有双键易老化,工业上常将它与含硫物质作用转变成为体型的网状分子的
B.《有机化学》
(1)有机物含有的官能团不同,性质也有差异.
①1mol下列有机物可与2mol溴单质发生加成反应的是
A.乙烯 B.乙炔 C.乙烷
②下列有机物中,核磁共振氢谱只有一个吸收峰的是
A.苯 B.苯酚 C.苯甲酸
③下列有机物中,能发生银镜反应的是
A.乙酸乙酯 B.乙醇 C.葡萄糖
(2)分子式为C4H10O,属于醇的同分异构体有




(3)科学家常采用将药物连接在高分子载体上,制成缓释长效药物.已知某种解热镇痛类药物,其结构简式如图甲,把它连接到高分子聚合物B上,形成缓释长效药物C如图乙.
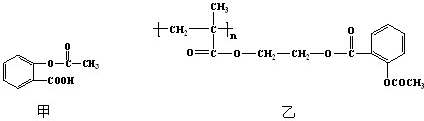
①分子聚合物B的结构简式为


②A与B反应生成C的有机反应类型是
③A可水解成

