网址:http://m.1010jiajiao.com/timu_id_432526[举报]
一、选择题:
1、C 2、C 3、B 4、A 5、D 6、B 7、A 8、A 9、D 10、C
11、D 12、D 13、D
二、不定向选择题:
14、D 15、C 16、CD 17、AC 18、AD 19、AD 20、D 21、B
三必答题:
22、(15分)(1)71.4(3分),(2)1.47V(2分),0.73Ω(2分)
(3)①(S4 ―S1)/3t2(2分),②B(3分),
③(a)沙及沙桶质量m过大或M远大于m没有满足 (2分)
(b)平衡摩擦过分。(2分)
23、(15分)解:
(1)由牛顿第二定律得到Kmg―mg=ma(3分)
解得当K=4时,a1=
所以飞船在竖直向上发射时的加速度值的变化范围为
(2)由万有引力定律和牛顿第二定律得到GMm/(R+H)2=mV2/(R+H)(4分)
在地面物体受到的重力约为万有引力,即GM/R2=g(3分)
两式联立解得V= =7.
=7.
24.(17分)解:
(1)因粒子垂直地打到屏PQ上的某一点,所以该粒子一定是从M板的边缘进入磁场区域的,可知M板带正电,N板带负电。(2分)
(2)粒子在电场中运动时由运动学公式得
L=V0t (2分) L/2=at2/2=VYt/2(2分) 解得VY=V0 (1分)
所以V= =
= V0 (1分) 方向向右偏上α角,tanα=1,α=45°(1分)
V0 (1分) 方向向右偏上α角,tanα=1,α=45°(1分)
(3)粒子在磁场中运动时由几何关系得d/R=sin45°圆运动半径R= d(2分)
d(2分)
由运动定律和运动学相关公式得到 BqV0=m(
BqV0=m( V0)2/R(2分)
V0)2/R(2分)
解得q/m=V0/Bd(1分)
(4)由动能定理得qU/2=mV2/2 ―mV02/2 (2分) 解得U=mV02/2q=BdV0/2(1分)
25.本题共14分。方程式未配平的扣1分
(1)O2+4e +2H2O=4OH-(2分) (2)32(2分)
(3)2Fe3++Cu=2Fe2++Cu2+(2分)
(4)防止Fe2+被氧化(1分) ①抑制FeSO4水解(1分)
②2;10;8;5;2;1;8(2分)
③酸(1分); 紫(或紫红)(1分) ④0.02 mol/L(2分)
26.本题共14分
(1)1.6×
(3)①15~20 min(1分)和25~30 min(1分)②增加了O2的量(1分)③ab(2分)
27.本题共15分。方程式未配平的扣1分。
(1)6.25(2分) (2)①圆底烧瓶(1分);
 安全管(或:防止装置中压力过大而发生危险;防止冷却时发生倒吸)(2分);
安全管(或:防止装置中压力过大而发生危险;防止冷却时发生倒吸)(2分);
NH+4+OH- NH3↑+H2O(2分); B(1分)
②消除其它试剂、实验操作等因素引起的误差(2分)
③(NH4)2B4O7+2HCl+5H2O=4H3BO3+2NH4Cl(2分)
④32.00(1分); 4.480(2分)
28、(26分)回答下列I、II题:
I、(每空1分)(1)转录和翻译
(2)B细胞和记忆(B)细胞(漏答或答错均不得分)
(3)注射抗原(疫苗) 可刺激家禽体内产生相应的抗体和记忆细胞
Ⅱ、(22分)(1)2n(3分)
(2)基因通过控制酶的合成来控制代谢,进而控制生物性状(3分)
(3)①×④(3分) ②×⑤(3分)
(4)AaXBY、AaXBXb(3分)
(5)由于残翅性状不利于果蝇生存,在自然选择的作用下,残翅基因的频率较低,因而
残翅果蝇数量较少(3分)
(6)实验步骤:让这只黑体雄果蝇与正常黑体雌果蝇(未用添加剂饮料喂过)
交配(2分),将孵化出的幼虫用正常饲料(不含添加剂)喂养,其它条件适当,
观察果蝇体色状况(2分)
29、(13分每空1分) (2)热能 升高
(4) ③备用的葡萄糖溶液 ④适量的酵母菌培养液和液体石蜡油 与A等量的酵母菌培养液 与A等量的蒸馏水
(5) 升高少 酵母菌在无氧条件下无氧呼吸放出的能量少
升高多 酵母菌在有氧条件下有氧呼吸释放的能量多
不升高 无酵母菌没有呼吸作用释放能量
(6)酵母菌的细胞呼吸方式包括有氧呼吸和无氧呼吸两种,有氧呼吸比无氧呼吸释放的能量多
四、选答题:
30、【物理-----选修2―2】
(1)C (6分)
(2)(9分)解:由有固定转动轴物体的平衡条件得
m1gL/2+m2gd=FLSin530 (5分) 解得(1分)
F的大小逐渐增大(3分)
31、(1)AD
(2)(9分)解:由理想气体状态方程得
P1 (H1―h)/T1=P2H2/T2(4分)
由题意得P1 =P0 ―h (2分) P2=P0+(H2―H1)(2分)
解得T2=480k,∴t2=
32、(1)C(6分)(2)(9分)解;
①由折射定律得到 Sini/Sinγ=1/n(2分) 解得n= (1分)
(1分)
②由SinC=1/n(1分) 解得C=450(1分)
向下移动L1=R Sin450―R Sin300=( ―1)R/2(2分)
―1)R/2(2分)
向下移动L2=R Sin450+R Sin300=( +1)R/2(2分)
+1)R/2(2分)
33、【物理-----选修3―5】
(1)AB(6分)
(2)(9分)解:由动量守恒定律得m(L―X)=MX
解得X=mL/(M+m)(3分)
所以人和船对地的位移大小分别为ML/(M+m)和mL/(M+m)(1分)。
由能量守恒可知此过程人做的功等与人、船的动能之和
所以有W=mV2/2+MU2/2(2分)
又由动量守恒定律得mV=MU(2分)
联立解得W=mV2/2+MU2/2= (1分)
(1分)
 34.本题共15分。方程式未配平的扣1分。
34.本题共15分。方程式未配平的扣1分。
(1)①CaCO3 CaO+CO2↑(2分)(2)Mg2++2e-=Mg(2分)
(3)蒸发皿(1分)、玻璃棒(1分) (4)提高Mg2+的浓度,起到富集的作用(2分)
(5)在HCl气流中(1分); 抑制MgCl2水解生成Mg(OH)2(1分),带走水蒸气(1分)
(6)abd(2分,部分选对给1分,选错不给分)
(7)BaCl2、Na2CO3、NaOH(或BaCl2、NaOH、Na2CO3;NaOH、BaCl2、Na2CO3)(2分)
35.本题共15分
(1)O(2分)
(2)SiO2(1分); SiO2是原子晶体,微粒间的作用力为共价键(1分);CO2是分子晶体,微粒间的作用力为范德华力(1分)。故SiO2的熔点高于CO2。
(3)N(1分); N的2p能级为半充满状态的2p3,是稳定结构(1分),而O的2p能级为2p4,是不稳定结构(1分)。故N的第一电离能高于O。
(4)V型(或角型)(2分); sp2杂化(2分)
(5)Cu(1分); 1s22s22p63s23p63d104s1或[Ar]3d104s1(2分)
36.本题共15分
(1)
 (2分)
(2)取代反应(1分)
(2分)
(2)取代反应(1分)
(3)
 +CO2+H2O→
+CO2+H2O→
 +NaHCO3(2分);
+NaHCO3(2分);
CH3COOH+C2H5OH
 CH3COOC2H5+H2O(2分)
CH3COOC2H5+H2O(2分)
(4)4(2分); 
 (其它合理答案也可)(2分)
(其它合理答案也可)(2分)
(5)HO-CH2-CHO(2分); HCOOCH3(2分)
37、【生物-----选修1生物技术实践】(15分)
(1)通入空气(2分) 密闭发酵罐(2分) C6H12O6???
(2)发酵过程中产生大量的CO2,及时排气可防止发酵瓶爆裂(2分)
(3)加入醋酸菌、通入空气(2分) 30-
C2H5OH+O2――CH3COOH+H2O(1分)
(4)①为果醋发酵的初期提供O2 ②为CO2的产生创造一个缓冲空间(2分)
38、【生物----选修3现代生物科技专题】(15分)
(1)人体蛋白基因与奶牛胚胎细胞中DNA(即基因) (3分)
(2)相同。因为它们都是重组细胞②经过卵裂(有丝分裂)产生的(3分)
(3)导入基因表达的产品是人血清蛋白,利用雌性奶牛可通过产奶把这种“表达物质”分泌出来(3分)
(4)核移植、胚胎分割 (3分) 胚胎移植(3分)
注意:其它解法正确的,也得分。
在工厂中常使用煤作燃料,但煤燃烧后会产生有害的SO2,按“循环经济”的模式,就是要将SO2收集起来,把它变为有用的东西.
(1)向大气中过量排放SO2将会形成酸雨污染.正常雨水的pH约为
(2)三氧化硫通入浓氨水,可得到一种肥料,写出反应的化学的方程式:
(3)某空气监测是根据SO2和溴水的定量反应来测定SO2的含量.该反应的化学方程式为
(4)近闻美国和日本正在研究用Na2SO3吸收法作为治理SO2污染的一种新方法:
第一步是用Na2SO3水溶液吸收SO2;
第二步是加热吸收液,使之重新生成Na2SO3,同时得到含高浓度SO2水蒸气副产品,写出上述两步反应的化学方程式:
①
②
| ||
| ||
(1)纯碱是一种重要的化工原料.目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺.
①“氨碱法”产生大量CaCl2废弃物,写出该工艺中产生CaCl2的化学方程式:
 2NH3↑+CaCl2+2H2O
2NH3↑+CaCl2+2H2O 2NH3↑+CaCl2+2H2O
2NH3↑+CaCl2+2H2O②写出“联合制碱法”有关反应的化学方程式:
2NaHCO3
 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O2NaHCO3
 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O③CO2是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO2的来源有何不同?
(2)钢铁工业对促进经济和社会发展起了重要作用.
①炼钢时,加入硅、锰和铝的目的是
②不锈钢含有的Cr元素是在炼钢过程的氧吹
③炼铁和炼钢生产中,尾气均含有的主要污染物是
重晶石矿石主要含有BaSO4,还含有少量有SiO2、Al2O3、Fe2O3、MnO2、FeS2、Na2O、K2O等杂质.以下是某工业制备硫酸钡以及分离某些金属的流程图.
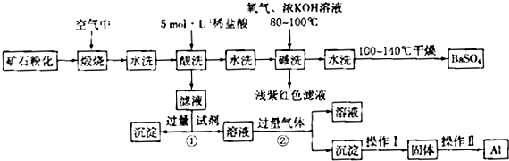
(1)煅烧过程中产生的污染性气体主要是
(2)确定第一次水洗液中有K+存在的实验现象是
(3)写出碱洗时的氧化还原反应方程式
(4)①反应生成沉淀的化学式
(5)操作I为
农作物生长不仅需要阳光、空气和水,还需要多种化学元素.当植物缺乏N元素时,表现为植株生长缓慢、叶色发黄,严重时叶片脱落直至死亡.
(1)下列可作氮肥的化合物是
A.硫酸铵 B.磷酸二氢钙 C.硫酸钾 D.尿素
(2)氮肥的制备,首先涉及氨的合成,请填写下列合成氨工艺流程图中的设备名称:
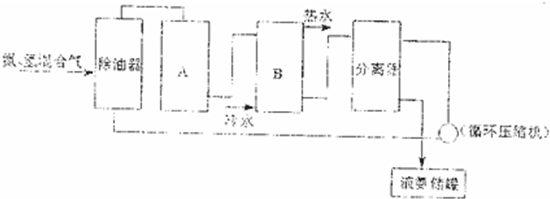
A
(3)某化工厂为了综合利用生产过程中的副产品CaSO4,与相邻的合成氨厂联合设计了以下制备(NH4)2SO4的工艺流程:
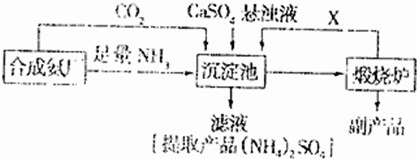
①沉淀池中发生的主要反应方程式是
②在上述流程的沉淀池中通入足量氨气的目的是
③从物质的性质和工业生产实际的角度考虑该流程的主要缺陷是
工业上用硫铁矿为主要原料抽取硫酸,主要设备有沸腾米,接触室和吸引塔.
(1)硫铁矿在进入沸腾炉前需要粉碎,其目的是
(2)为了充分利用反应放出的热量,接触室中应安装
(3)吸收塔排放的尾气中含有少量的SO2,防止污染大气、充分利用原料,在排放前必须进行尾气处理并设法进行综合利用.
传统的方法是:尾气中的SO2通常用足量氨水吸收,然后再用稀硫酸处理,写出上述过程中的化学反应方程式:
创新方法是:将尾气中的SO2用Na2SO3溶液吸收,然后再加热所得溶液,写出上述过程中的化学反应方程式:
(4)在硫酸的工业制法中,下列生产操作及说法生产操作的主要原因二者都正确的是
A.从沸腾炉出来的炉气需净化,因为炉气中的SO2与杂质反应
B.硫酸生产中常采用高压条件,目的是提高SO2的转化率
C.SO2被氧化为SO3时需要使用催化剂,这样可以提高SO2的转化率
D.SO3用98.3%浓硫酸吸收,目的是防止形成酸雾,有利于SO3吸收完全
(5)某硫酸厂若要生产8吨98%的浓硫酸至少需要标准状况下的空气