网址:http://m.1010jiajiao.com/timu_id_427853[举报]
(1)过碳酸钠 (化学式2Na2CO3?3H2O2) 俗称固体双氧水,白色结晶颗粒.过碳酸钠溶于水或受热时,分解生成碳酸钠和过氧化氢,是很好的固体氧释放剂.
①请你写出过氧化氢的电子式
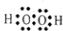
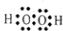
②H2O2有时可作为矿业废物消毒剂,有“绿色氧化剂”的美称,如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:
KCN+H2O2+H2O=A+NH3↑,则生成物A的化学式为
③某强酸性反应体系中,反应物和生成物共六种物质;O2、MnO4-、H2O、Mn2+、H2O2、H+.已知该反应中H2O2只发生了如下过程:H2O2→O2.写出该反应的离子方程式
④实验室制O2主要有4种方法,用化学方程式写出任意一种
| ||
| ||
(2)碳酸钠水溶液显碱性.用离子方程式解释其原因
(3)漂白剂亚氯酸钠 (NaClO2) 在常温黑暗处可保存一年.亚氯酸不稳定可分解,反应的离子方程式为:
HClO2→ClO2↑+H++Cl-+H2O(未配平).在该反应中,当有1molClO2生成时,转移的电子数是
(4)ClO2不稳定,可与NaOH溶液、H2O2反应,转化为较稳定的亚氯酸钠 (NaClO2).该反应的化学方程式为
自2009年3月起,从墨西哥、美国等国逐渐扩散到全世界的甲型H1N1型流感爆发疫情,引起全球关注和积极应对.防控专家表示,含氯消毒剂和过氧化物等强氧化性消毒剂可预防甲型H1N1型流感.
(1)过碳酸钠 (化学式2Na2CO3?3H2O2) 俗称固体双氧水,白色结晶颗粒.过碳酸钠溶于水或受热时,分解生成碳酸钠和过氧化氢,是很好的固体氧释放剂.
①请你写出过氧化氢的电子式______,其中氧元素的化合价是______.
②H2O2有时可作为矿业废物消毒剂,有“绿色氧化剂”的美称,如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:
KCN+H2O2+H2O=A+NH3↑,则生成物A的化学式为______,H2O2被称为“绿色氧化剂”的理由是______.
③某强酸性反应体系中,反应物和生成物共六种物质;O2、MnO4-、H2O、Mn2+、H2O2、H+.已知该反应中H2O2只发生了如下过程:H2O2→O2.写出该反应的离子方程式______.
④实验室制O2主要有4种方法,用化学方程式写出任意一种______.
(2)碳酸钠水溶液显碱性.用离子方程式解释其原因______;pH值相同的①碳酸钠溶液、②醋酸钠溶液、③氢氧化钠溶液,其浓度由大到小的顺序是:______(填写序号).
(3)漂白剂亚氯酸钠 (NaClO2) 在常温黑暗处可保存一年.亚氯酸不稳定可分解,反应的离子方程式为:
HClO2→ClO2↑+H++Cl-+H2O(未配平).在该反应中,当有1molClO2生成时,转移的电子数是______个.
(4)ClO2不稳定,可与NaOH溶液、H2O2反应,转化为较稳定的亚氯酸钠 (NaClO2).该反应的化学方程式为______.
查看习题详情和答案>>
电解质的电离
酸、碱、盐的电离
(1)酸、碱、盐溶液导电的原因:以NaCl为例分析.NaCl晶体是由带________的Na+和带________的Cl-构成的,晶体中的离子(Na+和Cl-)________自由移动,因此NaCl晶体________导电.当NaCl溶于水时,Na+和Cl-就会逐渐脱离晶体的表面进入溶液成为________的离子,这些离子因为带电荷,所以在电场作用下会发生________移动,因此NaCl溶液导电.当将NaCl晶体加热至熔化时,晶体中的Na+和Cl-也会成为________的离子,因此液态的NaCl也能导电.
(2)电离:化合物溶于水或熔化时,离解成能够移动的离子的过程称为电离.酸、碱、盐在溶于水或受热熔化时能发生电离,其特点为:酸:电离时产生的阳离子全部是________.碱:电离时产生的阴离子全部是________.盐:电离时产生的阳离子为________(或![]() ),阴离子是________.
),阴离子是________.
(3)电离方程式:表示电离的式子.
HCl![]() ________,
________,
NaOH![]() ________,
________,
NaCl![]() ________
________
(1)1个![]() 离子含有________个电子,
离子含有________个电子,![]() 的电子式为________.
的电子式为________.
(2)形成![]() 离子的中性分子的结构式是________.
离子的中性分子的结构式是________.
(3)写出![]() 离子在强碱溶液中反应的离子方程式________________________.
离子在强碱溶液中反应的离子方程式________________________.
(4)固体A的化学式为NH5,它的所有原子最外层都符合稀有气体原子的最外层电子结构,该物质适当加热就分解成两种气体,试回答:
①固体A属于________晶体,它的电子式________.
②A溶于水后溶液呈________性(填“酸”“碱”或“中”),其原因用化学方程式表示为________________________.
③A受热分解的化学方程式是________________________.
查看习题详情和答案>>
(12分)固体A是离子晶体,结构类似于CsCl,组成中含氮的质量分数为73.68%,它的所有原子的最外层都符合相应的稀有气体原子的最外层电子结构。该物质适当加热就分解成两种气体单质。试回答下列问题:
1.写出A的化学式 ,A的电子式 ;阳离子的结构为 体,其中心原子的杂化形态为 。
2.A溶于水后溶液呈 性(填“酸”、“碱”或“中”),其原因是(用化学方程式表示) 。
3.A与CuI在一定条件下可合成一种化合物B。B是一种红棕色、难溶于水的固体,X一射线衍射证实B是一种六方晶体,结构类同于闪锌矿(ZnS)测后的化学式为_________;生成B的化学反应为 。将B投入酸性溶液中(如盐酸溶液)可能看到的现象为 ,其化学反应方程式为 。
4.写出A受热分解的化学反应方程式 。该反应 (填“是”或“否”)属于氧化还原反应。
查看习题详情和答案>>