摘要:4.分子式用元素符号表示物质的分子组成的式子.一般分子式是最简式的整数倍.多数无机物二者是一致的.但也有例外.如最简式为NO2的分子可能是NO2.也可能是N2O4.有些单质.原子晶体和离子晶体通常情况下不存在简单分子.它的化学式则表示这种晶体中各元素的原子或离子数目的最简整数比.如C.SiO2.CsCl.Na2CO3.2CaSO4?H2O等.分子式的意义:(1)表示物质的元素组成,(2)表示该物质的一个分子,(3)表示分子中各元素的原子个数,(4)表示该物质的相对分子质量.例如.硫酸的分子式是H2SO4.它表示硫酸这种物质.也表示了硫酸的一个分子及分子是由2个氢原子.1个硫原子.4个氧原子组成.H2SO4同时也表示它的相对分子质量为
网址:http://m.1010jiajiao.com/timu_id_427835[举报]
[物质结构与性质]
原子序数小于36的X、Y、Z、W、J五种元素,原子序数依次增大,其中X元素原子半径是所有元素原子中最小的,Y元素原子核外有三种不同的能级且各个能级所填充的电子数相同,W元素原子最外层电子数是内层电子数的3倍,J元素原子序数为24.(用元素符号或化学式表示).
(1)Y、Z、W的第一电离能由小到大的顺序为
(2)J原子的核外电子排布式为
(3)Y2X2分子中Y原子轨道的杂化类型为
(4)Z与W形成的一种Z2W分子,与该分子互为等电子体的阴离子为
(5)JCl3能与Z、W的氢化物形成配位数为6的络合物,且相应两种配体的物质的量之比为2:1,氯离子全部位于外界.则该配合物的化学式为
查看习题详情和答案>>
原子序数小于36的X、Y、Z、W、J五种元素,原子序数依次增大,其中X元素原子半径是所有元素原子中最小的,Y元素原子核外有三种不同的能级且各个能级所填充的电子数相同,W元素原子最外层电子数是内层电子数的3倍,J元素原子序数为24.(用元素符号或化学式表示).
(1)Y、Z、W的第一电离能由小到大的顺序为
1s22s22p63s23p63d54s1
1s22s22p63s23p63d54s1
.(2)J原子的核外电子排布式为
1s22s22p63s23p63d54s1
1s22s22p63s23p63d54s1
.(3)Y2X2分子中Y原子轨道的杂化类型为
sp
sp
.1mol Y2X2分子中含有σ键与π键的数目之比为3:2
3:2
.(4)Z与W形成的一种Z2W分子,与该分子互为等电子体的阴离子为
N3-
N3-
(任写一种).(5)JCl3能与Z、W的氢化物形成配位数为6的络合物,且相应两种配体的物质的量之比为2:1,氯离子全部位于外界.则该配合物的化学式为
[Cr(NH3)4(H2O)2]Cl3
[Cr(NH3)4(H2O)2]Cl3
.物质A~M有下图所示的转化关系(部分生成物省略)。其中C、D是由 X、Y、Z中两种元素组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X 的原子半径最小,Y、Z两原子最外层电子数之和为
10,D为无色非可燃性气体, G为黄绿色气体单质,J、M为金属,I有漂白作用,反应①常用于制作印刷电 路板。
10,D为无色非可燃性气体, G为黄绿色气体单质,J、M为金属,I有漂白作用,反应①常用于制作印刷电 路板。
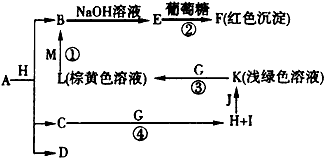
请回答下列问题:
(1)比较Y与Z的原子半径大小:____>____(填元素符号)。
(2)写出A的化学式:________;D的电子式:________。
(3)举出反应②在生活中的一个应用实例:____________。
(4)写出反应④的化学方程式:____________________。
(5)已知F溶于稀硝酸,溶液变成蓝色,并放出无色气体,请写出该反应的化学方程式:_____________。
(6)研究表明:气体D在一定条件下可被还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出N及其两种同素异形体的名称:________、 ________、________
查看习题详情和答案>>
(1)比较Y与Z的原子半径大小:____>____(填元素符号)。
(2)写出A的化学式:________;D的电子式:________。
(3)举出反应②在生活中的一个应用实例:____________。
(4)写出反应④的化学方程式:____________________。
(5)已知F溶于稀硝酸,溶液变成蓝色,并放出无色气体,请写出该反应的化学方程式:_____________。
(6)研究表明:气体D在一定条件下可被还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出N及其两种同素异形体的名称:________、 ________、________
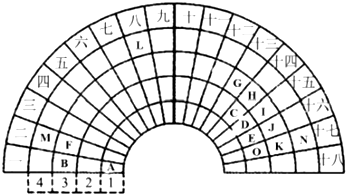
元素周期表是学习物质结构与性质的重要工具.下表是元素周期表的一部分,表中所列字母A、B、D、E、G、H、Q、M、R分别代表某一化学元素.请用所给元素回答下列问题.
(1)Q元素在元素周期表中的位置

(2)E、Q、R三种元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是(填离子符号)
(3)M、D两元素形成的化合物中含有的化学键类型是
(4)用表中所给元素组成反应物,用化学方程式说明元素Q和R非金属性的强弱:
查看习题详情和答案>>
| A | ||||||||||||||||||
| M | B | D | ||||||||||||||||
| G | H | Q | R | |||||||||||||||
| E | ||||||||||||||||||
第三周期ⅥA族
第三周期ⅥA族
,E元素原子结构示意图为

(2)E、Q、R三种元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是(填离子符号)
S2->Cl->K+
S2->Cl->K+
.(3)M、D两元素形成的化合物中含有的化学键类型是
共价键
共价键
,其MD2分子的结构式:O=C=O
O=C=O
.(4)用表中所给元素组成反应物,用化学方程式说明元素Q和R非金属性的强弱:
H2S+C12=2HC1+S
H2S+C12=2HC1+S
;元素G、H的金属性强弱:2Na+2H2O=2NaOH+H2↑
2Na+2H2O=2NaOH+H2↑
.【物质结构与性质】
(1)金属镁有许多重要的用途,格利雅试剂的结构简式可表示为RMgX,它是金属镁和卤代烃反应的产物,简称格氏试剂,它在醚的稀溶液中以单体形式存在,并与二分子醚络合,在浓溶液中以二聚体存在,结构如下图:


上述2种结构中均存在配位键,把你认为是配位键的用“→”标出.
(2)在短周期主族元素中,氯及其相邻元素的电负性由大到小的顺序是
(3)A、B、C为同一短周期金属元素.依据下表数据分析,C元素在化合物中的主要化合价为
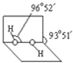 (4)已知过氧化氢分子的空间结构如图所示,分子中氧原子采取
(4)已知过氧化氢分子的空间结构如图所示,分子中氧原子采取
(5)R是1~36号元素中未成对电子数最多的原子.R3+在溶液中存在如下转化关系:
①基态R原子的价电子排布式为
②[R(OH)4]-中存在的化学键是
A.离子键 B.极性键 C.非极性键 D.配位键.
查看习题详情和答案>>
(1)金属镁有许多重要的用途,格利雅试剂的结构简式可表示为RMgX,它是金属镁和卤代烃反应的产物,简称格氏试剂,它在醚的稀溶液中以单体形式存在,并与二分子醚络合,在浓溶液中以二聚体存在,结构如下图:


上述2种结构中均存在配位键,把你认为是配位键的用“→”标出.
(2)在短周期主族元素中,氯及其相邻元素的电负性由大到小的顺序是
F>Cl>S
F>Cl>S
(用元素符号表示)(3)A、B、C为同一短周期金属元素.依据下表数据分析,C元素在化合物中的主要化合价为
+3
+3
;第二电离能(I2)B小于A的原因是A+外层电子排布为2s22p6稳定结构,难再失去一个电子.B+外层电子排布为3s1,易失去一个电子
A+外层电子排布为2s22p6稳定结构,难再失去一个电子.B+外层电子排布为3s1,易失去一个电子
.| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| A | 500 | 4600 | 6900 | 9500 |
| B | 740 | 1500 | 7700 | 10500 |
| C | 580 | 1800 | 2700 | 11600 |
 (4)已知过氧化氢分子的空间结构如图所示,分子中氧原子采取
(4)已知过氧化氢分子的空间结构如图所示,分子中氧原子采取sp3
sp3
杂化;通常情况下,H2O2与水任意比互溶的主要原因是H2O2分子H2O分子之间形成氢键,使H2O2与水任意比互溶
H2O2分子H2O分子之间形成氢键,使H2O2与水任意比互溶
.(5)R是1~36号元素中未成对电子数最多的原子.R3+在溶液中存在如下转化关系:

①基态R原子的价电子排布式为
3d54s1
3d54s1
.②[R(OH)4]-中存在的化学键是
BD
BD
.A.离子键 B.极性键 C.非极性键 D.配位键.