题目内容
【物质结构与性质】
(1)金属镁有许多重要的用途,格利雅试剂的结构简式可表示为RMgX,它是金属镁和卤代烃反应的产物,简称格氏试剂,它在醚的稀溶液中以单体形式存在,并与二分子醚络合,在浓溶液中以二聚体存在,结构如下图:


上述2种结构中均存在配位键,把你认为是配位键的用“→”标出.
(2)在短周期主族元素中,氯及其相邻元素的电负性由大到小的顺序是
(3)A、B、C为同一短周期金属元素.依据下表数据分析,C元素在化合物中的主要化合价为
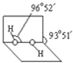 (4)已知过氧化氢分子的空间结构如图所示,分子中氧原子采取
(4)已知过氧化氢分子的空间结构如图所示,分子中氧原子采取
(5)R是1~36号元素中未成对电子数最多的原子.R3+在溶液中存在如下转化关系:
①基态R原子的价电子排布式为
②[R(OH)4]-中存在的化学键是
A.离子键 B.极性键 C.非极性键 D.配位键.
(1)金属镁有许多重要的用途,格利雅试剂的结构简式可表示为RMgX,它是金属镁和卤代烃反应的产物,简称格氏试剂,它在醚的稀溶液中以单体形式存在,并与二分子醚络合,在浓溶液中以二聚体存在,结构如下图:


上述2种结构中均存在配位键,把你认为是配位键的用“→”标出.
(2)在短周期主族元素中,氯及其相邻元素的电负性由大到小的顺序是
F>Cl>S
F>Cl>S
(用元素符号表示)(3)A、B、C为同一短周期金属元素.依据下表数据分析,C元素在化合物中的主要化合价为
+3
+3
;第二电离能(I2)B小于A的原因是A+外层电子排布为2s22p6稳定结构,难再失去一个电子.B+外层电子排布为3s1,易失去一个电子
A+外层电子排布为2s22p6稳定结构,难再失去一个电子.B+外层电子排布为3s1,易失去一个电子
.| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| A | 500 | 4600 | 6900 | 9500 |
| B | 740 | 1500 | 7700 | 10500 |
| C | 580 | 1800 | 2700 | 11600 |
 (4)已知过氧化氢分子的空间结构如图所示,分子中氧原子采取
(4)已知过氧化氢分子的空间结构如图所示,分子中氧原子采取sp3
sp3
杂化;通常情况下,H2O2与水任意比互溶的主要原因是H2O2分子H2O分子之间形成氢键,使H2O2与水任意比互溶
H2O2分子H2O分子之间形成氢键,使H2O2与水任意比互溶
.(5)R是1~36号元素中未成对电子数最多的原子.R3+在溶液中存在如下转化关系:

①基态R原子的价电子排布式为
3d54s1
3d54s1
.②[R(OH)4]-中存在的化学键是
BD
BD
.A.离子键 B.极性键 C.非极性键 D.配位键.
分析:(1)格氏试剂RMgX与醚可以形成络合物,由络合物的结构可知,RMgX与二分子醚络合,Mg提供空轨道、醚键氧原子体积孤对电子,形成配位键,RMgX与醚形成的以二聚体中除Mg与O原子形成配位键外、Mg与X原子也形成1个配位键;
(2)同周期自左而右电负性增大,同主族自上而下电负性减小,据此判断;
(3)由表中数据可知,C的第四电离能剧增,故C表现+3价,为金属Al元素,由表中数据可知,A第二电离能剧增,故A表现+1价,为Na元素,B的第三电离能剧增,表现+2价,为Mg元素,结合失去A、B失去1个电子后形成的+1微粒的外围电子排布的稳定性解答;
(4)由H2O2的结构可知,O原子形成1个O-H键、1个O-O键,含有2对孤对电子,杂化轨道数为4,据此判断杂化方式;
H2O2中氧元素的电负性很强,H2O2分子H2O分子之间形成氢键,使H2O2与水任意比互溶;
(5)R是1~36号元素中未成对电子数最多的原子,则R原子外围电子排布为3d54s1,为Cr元素;
根据[Al(OH)4]-的结构理解[Cr(OH)4]-中成键情况,Cr3+与OH-之间形成配位键,氧原子与氢原子之间形成极性键.
(2)同周期自左而右电负性增大,同主族自上而下电负性减小,据此判断;
(3)由表中数据可知,C的第四电离能剧增,故C表现+3价,为金属Al元素,由表中数据可知,A第二电离能剧增,故A表现+1价,为Na元素,B的第三电离能剧增,表现+2价,为Mg元素,结合失去A、B失去1个电子后形成的+1微粒的外围电子排布的稳定性解答;
(4)由H2O2的结构可知,O原子形成1个O-H键、1个O-O键,含有2对孤对电子,杂化轨道数为4,据此判断杂化方式;
H2O2中氧元素的电负性很强,H2O2分子H2O分子之间形成氢键,使H2O2与水任意比互溶;
(5)R是1~36号元素中未成对电子数最多的原子,则R原子外围电子排布为3d54s1,为Cr元素;
根据[Al(OH)4]-的结构理解[Cr(OH)4]-中成键情况,Cr3+与OH-之间形成配位键,氧原子与氢原子之间形成极性键.
解答:解:(1)格氏试剂RMgX与醚可以形成络合物,由络合物的结构可知,RMgX与二分子醚络合,Mg提供空轨道、醚键氧原子体积孤对电子,形成配位键,RMgX与醚形成的以二聚体中除Mg与O原子形成配位键外、Mg与X原子也形成1个配位键,配位键如图: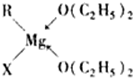 ,
,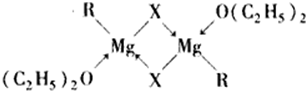 ,
,
故答案为: ,
, ;
;
(2)短周期主族元素中,与氯相邻两元素为F、S,同周期自左而右电负性增大,同主族自上而下电负性减小,
故电负性F>Cl>S,故答案为:F>Cl>S;
(2)由表中数据可知,C的第四电离能剧增,故C表现+3价,为金属Al元素,由表中数据可知,A第二电离能剧增,故A表现+1价,为Na元素,B的第三电离能剧增,表现+2价,为Mg元素,A+外层电子排布为2s22p6稳定结构,难再失去一个电子,B+外层电子排布为3s1,易失去一个电子,故第二电离能(I2)B小于A,
故答案为:+3;A+外层电子排布为2s22p6稳定结构,难再失去一个电子.B+外层电子排布为3s1,易失去一个电子;
(4)由H2O2的结构可知,O原子形成1个O-H键、1个O-O键,含有2对孤对电子,杂化轨道数为4,杂化方式为sp3,H2O2中氧元素的电负性很强,H2O2分子H2O分子之间形成氢键,使H2O2与水任意比互溶,
故答案为:sp3;H2O2分子H2O分子之间形成氢键,使H2O2与水任意比互溶;
(5)①R是1~36号元素中未成对电子数最多的原子,则R原子外围电子排布为3d54s1,故答案为:3d54s1;
②R为Cr元素,[Cr(OH)4]-与[Al(OH)4]-结构相似,Cr3+与OH-之间形成配位键,氧原子与氢原子之间形成极性键,故答案为:BD.
 ,
, ,
,故答案为:
 ,
, ;
;(2)短周期主族元素中,与氯相邻两元素为F、S,同周期自左而右电负性增大,同主族自上而下电负性减小,
故电负性F>Cl>S,故答案为:F>Cl>S;
(2)由表中数据可知,C的第四电离能剧增,故C表现+3价,为金属Al元素,由表中数据可知,A第二电离能剧增,故A表现+1价,为Na元素,B的第三电离能剧增,表现+2价,为Mg元素,A+外层电子排布为2s22p6稳定结构,难再失去一个电子,B+外层电子排布为3s1,易失去一个电子,故第二电离能(I2)B小于A,
故答案为:+3;A+外层电子排布为2s22p6稳定结构,难再失去一个电子.B+外层电子排布为3s1,易失去一个电子;
(4)由H2O2的结构可知,O原子形成1个O-H键、1个O-O键,含有2对孤对电子,杂化轨道数为4,杂化方式为sp3,H2O2中氧元素的电负性很强,H2O2分子H2O分子之间形成氢键,使H2O2与水任意比互溶,
故答案为:sp3;H2O2分子H2O分子之间形成氢键,使H2O2与水任意比互溶;
(5)①R是1~36号元素中未成对电子数最多的原子,则R原子外围电子排布为3d54s1,故答案为:3d54s1;
②R为Cr元素,[Cr(OH)4]-与[Al(OH)4]-结构相似,Cr3+与OH-之间形成配位键,氧原子与氢原子之间形成极性键,故答案为:BD.
点评:本题考查电负性、电离能、化学键与杂化轨道、氢键对物质性质影响、核外电子排布规律等,难度中等,注意理解第一电离能与化合价关系.

练习册系列答案
 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目