摘要:①B.C的单质是常见气体,A.D的单质是常见固体且均能与稀酸反应.②甲是黑色固体,反应①的原理可用于冶金工业,乙具有很高的熔点.是工业制取D单质的原料.试根据上图和题中有关叙述推断回答:⑴写出化合物甲的化学式 ,⑵写出反应②的化学方程式 ,⑶实验室中用MnO2作为试剂之一制取C单质的离子方程式 ,⑷在丁溶液中逐滴滴加稀盐酸直到过量.出现的实验现象是: .有关的离子方程式为 .
网址:http://m.1010jiajiao.com/timu_id_41152[举报]
A、B、C、D均为中学化学常见的纯净物,它们之间有如下转化关系(某些生成物已略去)
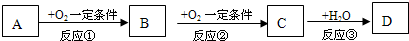
试回答:
(1)若A是非金属元素形成的化合物,且A与B、C在一定条件下都能反应生成一种无毒的气体.请写出下列化学方程式
①C→D
(2)若A是金属单质.
①向AlCl3溶液中滴加D的水溶液,能看到的现象是
②继续向所得溶液中通入足量的CO2气体,可看到的现象是
查看习题详情和答案>>
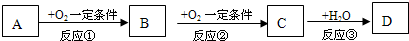
试回答:
(1)若A是非金属元素形成的化合物,且A与B、C在一定条件下都能反应生成一种无毒的气体.请写出下列化学方程式
①C→D
3NO2+H2O=2HNO3+NO
3NO2+H2O=2HNO3+NO
;②A和C反应8NH3+6NO2=7N2+12H2O
8NH3+6NO2=7N2+12H2O
.(2)若A是金属单质.
①向AlCl3溶液中滴加D的水溶液,能看到的现象是
首先看到白色沉淀,而后沉淀溶解
首先看到白色沉淀,而后沉淀溶解
,理由是(用离子方程式表示)Al3++3OH-=Al(OH)3↓、Al(OH)3+OH-=[Al(OH)4]-
Al3++3OH-=Al(OH)3↓、Al(OH)3+OH-=[Al(OH)4]-
;②继续向所得溶液中通入足量的CO2气体,可看到的现象是
有白色沉淀生成
有白色沉淀生成
,写出反应的离子方程式[Al(OH)4]-+CO2=Al(OH)3↓+HCO3-
[Al(OH)4]-+CO2=Al(OH)3↓+HCO3-
.A、B、C、D是中学化学常见的四种短周期元素,已知:
①A元素原子最外层电子数是次外层电子数的2倍,且A与D同主族;
②B元素最高正价与负价的代数和为2;
③C元素有多种化合价,且常温下C元素的气态单质与NaOH溶液反应,可得两种含C元素的化合物;
④B、C两种元素质子数之和是A元素质子数的4倍.
(1)A、B、C三种元素最高价氧化物对应水化物的酸(碱)性由强到弱的顺序是(用化学式表示)
(2)B的最高价氧化物的水化物的稀溶液与铜单质反应,离子方程为
(3)B、D两元素可形成一种新型无机非金属化合物材料X.X可由C、D两元素形成的化合物Z与B的氢化物在一定条件下制得,则生成X的化学方程为
(4)由B、C两种元素组成的化合物Y,常温下为易挥发的淡黄色液体,Y分子为三角锥形分子,且B、C两种原子最外层均达到8个电子的稳定结构.Y遇水蒸气可生成一种常见的漂白性物质.则Y的电子式为
 ,Y与水反应产物的化学式为
,Y与水反应产物的化学式为
查看习题详情和答案>>
①A元素原子最外层电子数是次外层电子数的2倍,且A与D同主族;
②B元素最高正价与负价的代数和为2;
③C元素有多种化合价,且常温下C元素的气态单质与NaOH溶液反应,可得两种含C元素的化合物;
④B、C两种元素质子数之和是A元素质子数的4倍.
(1)A、B、C三种元素最高价氧化物对应水化物的酸(碱)性由强到弱的顺序是(用化学式表示)
HClO4>HNO3>H2CO3
HClO4>HNO3>H2CO3
,D元素在元素周期表中的位置是第三周期ⅣA族
第三周期ⅣA族
(2)B的最高价氧化物的水化物的稀溶液与铜单质反应,离子方程为
3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O
,现有19.2g 铜粉溶解,产生标准状况下气体的体积是4.48
4.48
L.(3)B、D两元素可形成一种新型无机非金属化合物材料X.X可由C、D两元素形成的化合物Z与B的氢化物在一定条件下制得,则生成X的化学方程为
3SiCl4+4NH3═Si3N4+12HCl
3SiCl4+4NH3═Si3N4+12HCl
.(4)由B、C两种元素组成的化合物Y,常温下为易挥发的淡黄色液体,Y分子为三角锥形分子,且B、C两种原子最外层均达到8个电子的稳定结构.Y遇水蒸气可生成一种常见的漂白性物质.则Y的电子式为


NH3和HClO
NH3和HClO
.A、B、C、D、E为中学化学常见的单质或化合物,它们之间的相互转化关系如图所示(部分产物略去).

请回答下列问题:
(1)若A是能使湿润的红色石蕊试纸变蓝的气体,C、D均为空气的主要成分,E是一种有毒气体.
①C分子的电子式为
 :
:
②写出反应I的化学方程式:
③写出反应Ⅱ的化学方程式:
(2)若A是淡黄色固体化合物;常温下D是无色气体;C分子中含有的阴、阳离子均为10电子粒子.
①D的结构式为
②写出反应I的化学方程式:
③写出反应Ⅱ的化学方程式:
(3)将(2)中一定量的气体D通入2L含C的溶液中,在反应后所得的溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发).

①O点溶液中所含溶质的化学式为
②标准状况下,通入气体D的体积为
查看习题详情和答案>>

请回答下列问题:
(1)若A是能使湿润的红色石蕊试纸变蓝的气体,C、D均为空气的主要成分,E是一种有毒气体.
①C分子的电子式为


②写出反应I的化学方程式:
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
;
| ||
| △ |
③写出反应Ⅱ的化学方程式:
2NO+2CO
N2+2CO2
| ||
2NO+2CO
N2+2CO2
.
| ||
(2)若A是淡黄色固体化合物;常温下D是无色气体;C分子中含有的阴、阳离子均为10电子粒子.
①D的结构式为
O=C=O
O=C=O
,C分子中所含化学键的类型是离子键和共价键
离子键和共价键
;②写出反应I的化学方程式:
2Na2O2+2CO2=2Na2CO3+O2
2Na2O2+2CO2=2Na2CO3+O2
;③写出反应Ⅱ的化学方程式:
Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
(3)将(2)中一定量的气体D通入2L含C的溶液中,在反应后所得的溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发).

①O点溶液中所含溶质的化学式为
NaHCO3、NaOH
NaHCO3、NaOH
,常温下a点溶液的pH>
>
7(填“>”、“=”或“<”),a点溶液中各离子浓度由大到小的关系是c(Na+)>c(Cl-)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-)
c(Na+)>c(Cl-)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-)
;②标准状况下,通入气体D的体积为
44.8
44.8
L,C溶液的物质的量浓度为2.5
2.5
mol?L-1. A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件及部分产物未列出)
A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件及部分产物未列出)(1)若A是常见金属单质,与B的水溶液反应生成C和D.D、F是气体单质,D在F中燃烧时发出苍白色火焰.则F所对应的元素在周期表位置是
第三周期、第ⅦA族
第三周期、第ⅦA族
,反应②(在水溶液中进行)的离子方程式为2Fe2++Cl2=2Fe3++2Cl-
2Fe2++Cl2=2Fe3++2Cl-
;(2)若A、D为短周期元素单质,且所含元素的原子序数A是D的2倍,所含元素的原子核外最外层电子数D是A的2倍,且③④两个反应都有红棕色气体生成,则反应①、④的化学方程式分别为
①
2Mg+CO2
2MgO+C
| ||
2Mg+CO2
2MgO+C
,
| ||
④
C+4HNO3(浓)
CO2↑+4NO2↑+2H2O
| ||
C+4HNO3(浓)
CO2↑+4NO2↑+2H2O
;
| ||
(3)若A、D、F都是短周期非金属单质,且A、D所含元素同主族,A、F所含元素同周期,C是一种能与血红蛋白结合的有毒气体;则物质B的晶体类型是
原子晶体
原子晶体
,分子E的结构式是O=C=O
O=C=O
.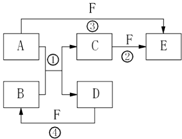 A、B、C、D、E、F六种物质的相互转化关系如右图所示(反应条件及部分产物未列出).
A、B、C、D、E、F六种物质的相互转化关系如右图所示(反应条件及部分产物未列出).(1)若A是常见金属单质,与B的水溶液反应生成C和D.D、F是气体单质,D在F中燃烧时发出苍白色火焰.则反应②(在水溶液中进行)的离子方程式为
2Fe2++Cl2=2Fe3++2Cl-
2Fe2++Cl2=2Fe3++2Cl-
.(2)若A、D为短周期元素组成的固体单质,一种为金属,另一种为非金属.且③④两个反应都有红棕色气体生成,则反应④的化学方程式为
C+4HNO3(浓)
CO2↑+4NO2↑+2H2O
| ||
C+4HNO3(浓)
CO2↑+4NO2↑+2H2O
.
| ||
(3)若A是黑色固体,D是有臭鸡蛋气味的气体,E溶液中滴加KSCN溶液呈血红色.则D的电子式是


4FeS2+11O2
2Fe2O3+8SO2
| ||
4FeS2+11O2
2Fe2O3+8SO2
,使用的设备是
| ||
沸腾炉
沸腾炉
.(4)若B是由地壳中含量最高的两种元素组成,A的一种同素异形体与B、D属同一种类型的晶体,则反应①的化学方程式是
2C+SiO2
Si+2CO↑
| ||
2C+SiO2
Si+2CO↑
,B与烧碱溶液反应的化学方程式是
| ||
SiO2+2NaOH=Na2SiO3+H2O
SiO2+2NaOH=Na2SiO3+H2O
.