题目内容
A、B、C、D均为中学化学常见的纯净物,它们之间有如下转化关系(某些生成物已略去)
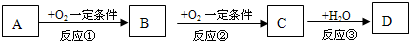
试回答:
(1)若A是非金属元素形成的化合物,且A与B、C在一定条件下都能反应生成一种无毒的气体.请写出下列化学方程式
①C→D
(2)若A是金属单质.
①向AlCl3溶液中滴加D的水溶液,能看到的现象是
②继续向所得溶液中通入足量的CO2气体,可看到的现象是
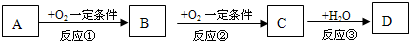
试回答:
(1)若A是非金属元素形成的化合物,且A与B、C在一定条件下都能反应生成一种无毒的气体.请写出下列化学方程式
①C→D
3NO2+H2O=2HNO3+NO
3NO2+H2O=2HNO3+NO
;②A和C反应8NH3+6NO2=7N2+12H2O
8NH3+6NO2=7N2+12H2O
.(2)若A是金属单质.
①向AlCl3溶液中滴加D的水溶液,能看到的现象是
首先看到白色沉淀,而后沉淀溶解
首先看到白色沉淀,而后沉淀溶解
,理由是(用离子方程式表示)Al3++3OH-=Al(OH)3↓、Al(OH)3+OH-=[Al(OH)4]-
Al3++3OH-=Al(OH)3↓、Al(OH)3+OH-=[Al(OH)4]-
;②继续向所得溶液中通入足量的CO2气体,可看到的现象是
有白色沉淀生成
有白色沉淀生成
,写出反应的离子方程式[Al(OH)4]-+CO2=Al(OH)3↓+HCO3-
[Al(OH)4]-+CO2=Al(OH)3↓+HCO3-
.分析:(1)若A是非金属元素形成的化合物,且A与B、C在一定条件下都能反应生成一种无毒的气体,A为NH3,B为NO,C为NO2,D为HNO3,符合转化关系;
(2)若A是金属单质,B、C为金属氧化物,且C与水反应,故A为Na,B为Na2O,C为Na2O2,D为NaOH,符合转化关系.
(2)若A是金属单质,B、C为金属氧化物,且C与水反应,故A为Na,B为Na2O,C为Na2O2,D为NaOH,符合转化关系.
解答:解:(1)若A是非金属元素形成的化合物,且A与B、C在一定条件下都能反应生成一种无毒的气体,A为NH3,B为NO,C为NO2,D为HNO3,符合转化关系;
①C→D的反应是二氧化氮与水反应生成硝酸与NO,反应方程式为:3NO2+H2O=2HNO3+NO,故答案为:3NO2+H2O=2HNO3+NO;
②A和C反应是氨气与二氧化氮反应生成氮气与水,反应方程式为:8NH3+6NO2=7N2+12H2O,故答案为:8NH3+6NO2=7N2+12H2O;
(2)若A是金属单质,B、C为金属氧化物,且C与水反应,故A为Na,B为Na2O,C为Na2O2,D为NaOH,符合转化关系;
①向AlCl3溶液中滴加NaOH的水溶液,首先发生反应Al3++3OH-=Al(OH)3↓,Al3+反应完毕,再发生Al(OH)3+OH-=[Al(OH)4]-,故能看到的现象是:首先看到白色沉淀,而后沉淀溶解;
故答案为:首先看到白色沉淀,而后沉淀溶解;Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-=[Al(OH)4]-;
②继续向所得溶液中通入足量的CO2气体,发生反应:[Al(OH)4]-+CO2=Al(OH)3↓+HCO3-;可看到的现象是:有白色沉淀生成;
故答案为:有白色沉淀生成;[Al(OH)4]-+CO2=Al(OH)3↓+HCO3-.
①C→D的反应是二氧化氮与水反应生成硝酸与NO,反应方程式为:3NO2+H2O=2HNO3+NO,故答案为:3NO2+H2O=2HNO3+NO;
②A和C反应是氨气与二氧化氮反应生成氮气与水,反应方程式为:8NH3+6NO2=7N2+12H2O,故答案为:8NH3+6NO2=7N2+12H2O;
(2)若A是金属单质,B、C为金属氧化物,且C与水反应,故A为Na,B为Na2O,C为Na2O2,D为NaOH,符合转化关系;
①向AlCl3溶液中滴加NaOH的水溶液,首先发生反应Al3++3OH-=Al(OH)3↓,Al3+反应完毕,再发生Al(OH)3+OH-=[Al(OH)4]-,故能看到的现象是:首先看到白色沉淀,而后沉淀溶解;
故答案为:首先看到白色沉淀,而后沉淀溶解;Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-=[Al(OH)4]-;
②继续向所得溶液中通入足量的CO2气体,发生反应:[Al(OH)4]-+CO2=Al(OH)3↓+HCO3-;可看到的现象是:有白色沉淀生成;
故答案为:有白色沉淀生成;[Al(OH)4]-+CO2=Al(OH)3↓+HCO3-.
点评:本题以转化关系的形式考查Na、N等元素单质及其化合物之间的相互转化关系、化学用语的书写,旨在考查学生对基础知识的熟练掌握程度,注意归纳总结中学常见A
B
C转化.
| X |
| X |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
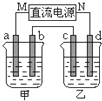 如图所示的装置中,甲、乙两烧杯中分别盛放有足量的CuSO4溶液和100g 10.00%的K2SO4溶液,a、b、c、d均为石墨电极.接通电源一段时间后,测得乙中K2SO4溶液浓度为10.47%,甲中a电极的质量增加.下列说法正确的是( )
如图所示的装置中,甲、乙两烧杯中分别盛放有足量的CuSO4溶液和100g 10.00%的K2SO4溶液,a、b、c、d均为石墨电极.接通电源一段时间后,测得乙中K2SO4溶液浓度为10.47%,甲中a电极的质量增加.下列说法正确的是( )| A、甲、乙溶液的pH均减小 | B、电极b上生成气体的体积约为2.8L(标准状况下) | C、电极d上发生的反应为:2H2O+2e-?H2↑+2OH- | D、欲使甲中的溶液恢复至原来的浓度,可加入24.5g的Cu(OH)2 |
 A、B、C、D均为常见物质,相互之间的关系如图所示.“-”表示两种物质间能发生反应,“→”表示物质间的转化关系,部分反应物或生成物以及反应条件已略去).
A、B、C、D均为常见物质,相互之间的关系如图所示.“-”表示两种物质间能发生反应,“→”表示物质间的转化关系,部分反应物或生成物以及反应条件已略去).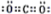
 A、B、C、D均为中学化学中常见的物质,它们之间的转化关系如下图(部分产物已略去):试回答:
A、B、C、D均为中学化学中常见的物质,它们之间的转化关系如下图(部分产物已略去):试回答: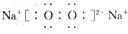
 A、B、C、D均为短周期元素,A和B是同周期相邻的两种元素,A和C是同主族相邻的两种元素:A、B、C三种元素的原子序数之和为31;D元素与A、B、C三种元素既不是同周期,也不同主族.请回答:
A、B、C、D均为短周期元素,A和B是同周期相邻的两种元素,A和C是同主族相邻的两种元素:A、B、C三种元素的原子序数之和为31;D元素与A、B、C三种元素既不是同周期,也不同主族.请回答: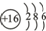
 NH3?H2O+H+
NH3?H2O+H+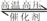 2NH3
2NH3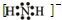
 .甲和丙可形成两种化合物X和Y,X和水反应后生成一种具有还原性的二元酸M.1mol乙与足量丙可化合生成Z,所得的Z与热水反应的产物W需用12mol KOH才能完全中和.乙在足量丁中燃烧生成化合物N,N和水反应生成W和D元素的气态氢化物.试回答下列问题:
.甲和丙可形成两种化合物X和Y,X和水反应后生成一种具有还原性的二元酸M.1mol乙与足量丙可化合生成Z,所得的Z与热水反应的产物W需用12mol KOH才能完全中和.乙在足量丁中燃烧生成化合物N,N和水反应生成W和D元素的气态氢化物.试回答下列问题: