摘要:2NH3+3CuO3Cu+N2↑+3H2OCuSO4+5H2O=CuSO4?5H2O
网址:http://m.1010jiajiao.com/timu_id_17544[举报]
A、B、C、D、E五种短周期元素,其原子序数依次增大,而原子半径按A、C、B、E、D顺序依次增大.A、D同主族;C、D、E三种元素原子、的最外层电子数之和为10,C原子电子数比E原子电子数少5个.B的单质分子中有三对共用电子.
请回答下列问题:
(1)A、C两元素形成的原子个数比为1:1且呈电中性的微粒的电子式为
 (写两种)
(写两种)
(2)A、C、D可形成化合物W,其含有的化学键有
(3)A2和B2在工业上可合成一种重要的原料BA3.
①下列的措施有利于提高B2的转化率的是
A.采用20?50MPa的大气压
B.选用400?500℃的高温
C.使用催化剂
D.及时将BA3液化
②现有甲、乙两个固定体积的容器,在相同的体积和温度下,甲中充入2molBA3,反应达到平衡时,吸收Q1kJ的能量;乙中充入
1mol B2和3mol A2,反应达到平衡时,放出Q2kJ的能量;则合成BA3的热化学方程式为
③现有甲、乙两个体积和温度相同的容器,甲容器维持温度和体积不变,乙容器维持温度和压强不变,甲中充入2mol BA3,乙中充入1mol B2和3mol A2,当反应都达到平衡时,BA3的体积分数甲
(4)化合物甲、乙都由A、B、C三种元素组成,甲为弱碱,乙为强酸;常温下,若两溶液中水的电离程度相同.
①若乙溶液的pH=a,则甲溶液中水电离产生的C(H+)=
(5)用D2C2在酸性条件下处理含CN-的工业废水,将得到一种能够参与大气生态环境循环的气体以及C02等物质,请写出该反应的离子方程式
查看习题详情和答案>>
请回答下列问题:
(1)A、C两元素形成的原子个数比为1:1且呈电中性的微粒的电子式为


(2)A、C、D可形成化合物W,其含有的化学键有
离子键、共价键
离子键、共价键
,以W溶液作为电解质溶液,E棒与铁棒分别作为电极构成原电池,则负极的电极反应式为Al-3e-+4OH-=AlO2-+2H2O
Al-3e-+4OH-=AlO2-+2H2O
;以铁棒为电极,W溶液为电解液构成电解池,则阴极的电极反应为2H++2e-=H2↑
2H++2e-=H2↑
.(3)A2和B2在工业上可合成一种重要的原料BA3.
①下列的措施有利于提高B2的转化率的是
AD
AD
.A.采用20?50MPa的大气压
B.选用400?500℃的高温
C.使用催化剂
D.及时将BA3液化
②现有甲、乙两个固定体积的容器,在相同的体积和温度下,甲中充入2molBA3,反应达到平衡时,吸收Q1kJ的能量;乙中充入
1mol B2和3mol A2,反应达到平衡时,放出Q2kJ的能量;则合成BA3的热化学方程式为
N2(g)+3H2(g)
2NH3(g),△H=-(Q1+Q2)kJ/mol
| 高温高压 |
| 催化剂 |
N2(g)+3H2(g)
2NH3(g),△H=-(Q1+Q2)kJ/mol
.| 高温高压 |
| 催化剂 |
③现有甲、乙两个体积和温度相同的容器,甲容器维持温度和体积不变,乙容器维持温度和压强不变,甲中充入2mol BA3,乙中充入1mol B2和3mol A2,当反应都达到平衡时,BA3的体积分数甲
<
<
乙(填“>”、“<”,或“=”),原因是乙容器中压强大,生成氨气的过程进行的程度大,因而氨气的体积分数高
乙容器中压强大,生成氨气的过程进行的程度大,因而氨气的体积分数高
(4)化合物甲、乙都由A、B、C三种元素组成,甲为弱碱,乙为强酸;常温下,若两溶液中水的电离程度相同.
①若乙溶液的pH=a,则甲溶液中水电离产生的C(H+)=
10a-14mol/L
10a-14mol/L
,②两溶液等体积混合后,混合溶液中的离子浓度由大到小的是c(NH4+)>c(NO3-)>c(OH-)>c(H+)
c(NH4+)>c(NO3-)>c(OH-)>c(H+)
(5)用D2C2在酸性条件下处理含CN-的工业废水,将得到一种能够参与大气生态环境循环的气体以及C02等物质,请写出该反应的离子方程式
5Na2O2+2CN-+12H+=2CO2↑+N2↑+10Na++6H2O
5Na2O2+2CN-+12H+=2CO2↑+N2↑+10Na++6H2O
.(2012?海淀区二模)合成氨尿素工业生产过程中涉及到的物质转化过程如下图所示.

(1)天然气在高温、催化剂作用下与水蒸气反应生成H2和CO的化学方程式为
(2)在合成氨生产中,将生成的氨及时从反应后的气体中分离出来.运用化学平衡的知识分析这样做的是否有利于氨的合成,说明理由:
(3)如图为合成氨反应在不同温度和压强、使用相同催化剂条件下,初始时氮气、氢气的体积比为1:3时,平衡混合物中氨的体积分数.

①若分别用υA(NH3)和υB(NH3) 表示从反应开始至达平衡状态A、B时的化学反应速率,则υA(NH3)
②在相同温度、当压强由p1变为p3时,合成氨反应的化学平衡常数
③在250℃、1.0×104kPa下,H2的转化率为
(4)NH3(g) 与CO2(g) 经过两步反应生成尿素,两步反应的能量变化示意图如下:

NH3(g) 与CO2(g) 反应生成尿素的热化学方程式为
(5)运输氨时,不能使用铜及其合金制造的管道阀门.因为,在潮湿的环境中,金属铜在有NH3存在时能被空气中的O2氧化,生成Cu(NH3)42+,该反应的离子方程式为
查看习题详情和答案>>

(1)天然气在高温、催化剂作用下与水蒸气反应生成H2和CO的化学方程式为
CH4+H2O
CO+3H2
| ||
CH4+H2O
CO+3H2
.
| ||
(2)在合成氨生产中,将生成的氨及时从反应后的气体中分离出来.运用化学平衡的知识分析这样做的是否有利于氨的合成,说明理由:
移走氨气,减小生成物浓度,平衡右移,有利于氨生成
移走氨气,减小生成物浓度,平衡右移,有利于氨生成
.(3)如图为合成氨反应在不同温度和压强、使用相同催化剂条件下,初始时氮气、氢气的体积比为1:3时,平衡混合物中氨的体积分数.

①若分别用υA(NH3)和υB(NH3) 表示从反应开始至达平衡状态A、B时的化学反应速率,则υA(NH3)
<
<
υB(NH3)(填“>”、“<”或“=”).②在相同温度、当压强由p1变为p3时,合成氨反应的化学平衡常数
不变
不变
.(填“变大”、“变小”或“不变”).③在250℃、1.0×104kPa下,H2的转化率为
66.7
66.7
%(计算结果保留小数点后1位).(4)NH3(g) 与CO2(g) 经过两步反应生成尿素,两步反应的能量变化示意图如下:

NH3(g) 与CO2(g) 反应生成尿素的热化学方程式为
2NH3(g)+CO2(g)═CO(NH2)2(s)+H2O(l)△H=-134kJ/mol
2NH3(g)+CO2(g)═CO(NH2)2(s)+H2O(l)△H=-134kJ/mol
.(5)运输氨时,不能使用铜及其合金制造的管道阀门.因为,在潮湿的环境中,金属铜在有NH3存在时能被空气中的O2氧化,生成Cu(NH3)42+,该反应的离子方程式为
2Cu+8NH3+O2+2H2O═2Cu(NH3)42++4OH-
2Cu+8NH3+O2+2H2O═2Cu(NH3)42++4OH-
.(2011?花都区模拟)(1)合成氨反应反应N2(g)+3H2(g)?2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡
(2)已知:
N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-543kJ?mol-1
H2(g)+
F2(g)=HF(g);△H=-269kJ?mol-1
H2(g)+
O2(g)=H2O(g);△H=-242kJ?mol-1则反应 N2H4(g)+2F2(g)=N2(g)+4HF(g) 的△H=
(3)已知25℃时Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.2×10-20.在25℃下,向浓度均为0.1mol?L-1的MgCL2和CuCl2混合溶液中逐滴加入氨水,先生成
(4)在25℃下,将a mol?L-1的氨水与0.01mol?L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显
mol?L-1.(说明:溶液的体积可以直接相加)
查看习题详情和答案>>
向左
向左
移动(填“向左”“向右”或“不”);使用催化剂不改变
不改变
反应的△H(填“增大”“减小”或“不改变”).(2)已知:
N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-543kJ?mol-1
| 1 |
| 2 |
| 1 |
| 2 |
H2(g)+
| 1 |
| 2 |
-1135
-1135
kJ?mol-1.(3)已知25℃时Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.2×10-20.在25℃下,向浓度均为0.1mol?L-1的MgCL2和CuCl2混合溶液中逐滴加入氨水,先生成
Cu(OH)2
Cu(OH)2
沉淀(填化学式),生成该沉淀的离子方程式为Cu2++2NH3?H2O=Cu(OH)2↓+2NH4+
Cu2++2NH3?H2O=Cu(OH)2↓+2NH4+
.(4)在25℃下,将a mol?L-1的氨水与0.01mol?L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显
中
中
性(填“酸”“碱”或“中”);用含a的代数式表示此时溶液中NH3?H2O的物质的量浓度| (α-0.01) |
| 2 |
| (α-0.01) |
| 2 |
Ⅰ工业上铜的冶炼常采取火法熔炼工艺.以辉铜矿(主要成分 Cu2S)为原料,该过程中有如下反应:
2Cu2S(s)+3O2(g)=2Cu2O(s)十2SO2(g)△H=-768.2KJ?mol-1
2Cu2O(s)+Cu2S(s)=6Cu(s)+SO2(g)△H=+116.0KJ?mol-1
反应Cu2S(s)+O2(g)=2Cu(s)+SO2(g)的△H=
在上述工业生产过程中产生的SO2气体直接排放会污染大气.工业上常用氨水吸收SO2,反应的化学方程式为
Ⅱ大气污染的另一个重要问题是臭氧层的破坏.为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏.化学家研究在催化条件下,通过下列反应,使CCl4转化为重要的化工原料氯仿(CHCl3).CCl4(g)+H2(g)
CHCl3(g)+HCl(g).此反应伴随有副反应,会生成CH2Cl2、CH3Cl和CH4等.已知CCl4的沸点为 77℃,CHCl3的沸点为 61.2℃.
如果不考虑反应过程中的副反应,在一个密闭容器中发生上述反应,该反应达到平衡后,测得下表中的数据.
请回答下列问题:
(1)实验1中,CCl4的转化率a
(2)在实验2的平衡体系中,再加入0.5mol?L-1CCl4和1mol?L-1HCl,平衡将向
(3)120℃,在相同条件的密闭容器中,分别进行实验3、4,测得CCl4的转化率(x)和生成物中CHCl3的体积分数(y)随时间(t)的变化关系如图(图中实线是CCl4转化率变化曲线,虚线是产物中CHCl3的体积分数变化曲线).
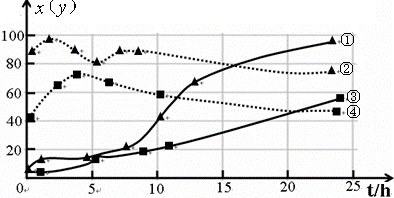
图中的四条线中,表示H2起始浓度为2mol?L-1实验中CCl4的转化率(x)变化曲线是
查看习题详情和答案>>
2Cu2S(s)+3O2(g)=2Cu2O(s)十2SO2(g)△H=-768.2KJ?mol-1
2Cu2O(s)+Cu2S(s)=6Cu(s)+SO2(g)△H=+116.0KJ?mol-1
反应Cu2S(s)+O2(g)=2Cu(s)+SO2(g)的△H=
-217.4KJ/mol
-217.4KJ/mol
.在上述工业生产过程中产生的SO2气体直接排放会污染大气.工业上常用氨水吸收SO2,反应的化学方程式为
SO2+2NH3?H2O=(NH4)2SO3+H2O或 SO2+NH3?H2O=NH4HSO3
SO2+2NH3?H2O=(NH4)2SO3+H2O或 SO2+NH3?H2O=NH4HSO3
.Ⅱ大气污染的另一个重要问题是臭氧层的破坏.为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏.化学家研究在催化条件下,通过下列反应,使CCl4转化为重要的化工原料氯仿(CHCl3).CCl4(g)+H2(g)
| 催化剂 |
| △ |
如果不考虑反应过程中的副反应,在一个密闭容器中发生上述反应,该反应达到平衡后,测得下表中的数据.
| 实验序号 | 温度℃ | 初始CCl4浓度(mol?L-1) | 初始H2浓度(mol?L-1) | CCl4的转化率 |
| 1 | 110 | 0.8 | 1.2 | a |
| 2 | 110 | 1 | 1 | 50% |
| 3 | 120 | 1 | 2 | x |
| 4 | 120 | 1 | 4 |
(1)实验1中,CCl4的转化率a
大于
大于
50%(填“大于”“小于”“等于”);(2)在实验2的平衡体系中,再加入0.5mol?L-1CCl4和1mol?L-1HCl,平衡将向
逆
逆
反应方向移动(填“正”、“逆”或“不移动”).(3)120℃,在相同条件的密闭容器中,分别进行实验3、4,测得CCl4的转化率(x)和生成物中CHCl3的体积分数(y)随时间(t)的变化关系如图(图中实线是CCl4转化率变化曲线,虚线是产物中CHCl3的体积分数变化曲线).

图中的四条线中,表示H2起始浓度为2mol?L-1实验中CCl4的转化率(x)变化曲线是
③
③
(选填序号).根据上图曲线,氢气的起始浓度为4mol/L
4mol/L
有利于提高CCl4的平衡转化率. (2008?重庆)化学反应N2+3H2=2NH3的能量变化如图所示,该反应的热化学方程式是( )
(2008?重庆)化学反应N2+3H2=2NH3的能量变化如图所示,该反应的热化学方程式是( )