题目内容
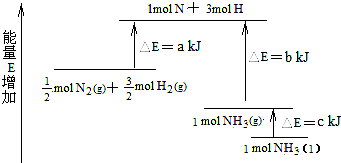 (2008?重庆)化学反应N2+3H2=2NH3的能量变化如图所示,该反应的热化学方程式是( )
(2008?重庆)化学反应N2+3H2=2NH3的能量变化如图所示,该反应的热化学方程式是( )分析:根据反应热等于反应物总能量减去生成物总能量计算反应热并书写热化学方程式,注意反应物的物质的量和生成物的聚集状态.
解答:解:由图可以看出,
molN2(g)+
molH2(g)的能量为akJ,1molNH3(g)的能量为bkJ,
所以
N2(g)+
H2(g)=NH3(g);△H=(a-b)kJ/mol,
而1mol的NH3(g)转化为1mol的NH3(l)放出的热量为ckJ,
所以有:
N2(g)+
H2(g)=NH3(l);△H=(a-b-c)kJ/mol,
即:N2(g)+3H2(g)=2NH3(1);△H=2(a-b-c)kJ?mol-1.
故选:A.
| 1 |
| 2 |
| 3 |
| 2 |
所以
| 1 |
| 2 |
| 3 |
| 2 |
而1mol的NH3(g)转化为1mol的NH3(l)放出的热量为ckJ,
所以有:
| 1 |
| 2 |
| 3 |
| 2 |
即:N2(g)+3H2(g)=2NH3(1);△H=2(a-b-c)kJ?mol-1.
故选:A.
点评:本题考查热化学方程式的书写,题目难度不大,注意书写热化学方程式的注意事项以及反应热的计算方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
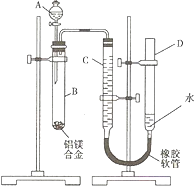 (2008?重庆)某学习小组用如图装置测定铝镁合金中铝的质量分数和铝的相对原子质量.
(2008?重庆)某学习小组用如图装置测定铝镁合金中铝的质量分数和铝的相对原子质量.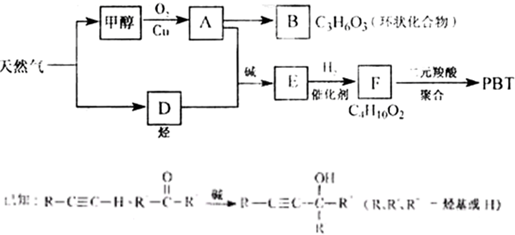

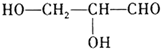
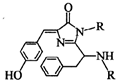 美籍华裔科学家钱永健、日本科学家下修村和美国科学家马丁?沙尔菲因在发现和研究绿色荧光蛋白(GFP)方面做出突出贡献而分享了2008年诺贝尔化学奖.经研究发现GFP中的生色基团结构如图所示,下列有关说法正确的是( )
美籍华裔科学家钱永健、日本科学家下修村和美国科学家马丁?沙尔菲因在发现和研究绿色荧光蛋白(GFP)方面做出突出贡献而分享了2008年诺贝尔化学奖.经研究发现GFP中的生色基团结构如图所示,下列有关说法正确的是( )