网址:http://m.1010jiajiao.com/timu_id_14305[举报]
一、选择题
题号
1
2
3
4
5
6
7
8
9
10
答案
D
D
B
D
D
C
D
C
B
D
二、选择题
题号
11
12
13
14
15
答案
AD
C
A
C
B
三、填空、简答和计算
16.(1)还原性;(2)漂白性;(3)还原性;(4)酸酐的性质。
17.溶液变为棕色 溶液变为无色并有白色沉淀 ①Cl2+2Br-=2Cl-+Br2
②Br2+SO2+2H2O=SO42-+2Br-+4H+ ③Ba2++SO42-=BaSO4↓
18.(1)S+O2 = SO2 ,2CaO+2SO2+O2 == 2CaSO4(或:SO2+CaO=CaSO3;2CaSO3+O2=2CaSO4)
(2)①2SO2+2CaCO3+O2+4H2O==2CaSO4?2H2O+2CO2
②2SO2+2Ca(OH)2+O2+2H2O==2CaSO4?2H2O
因为石灰乳中Ca(OH)2的含量较多,吸收SO2的容量较大
19.(1)SO2;CO2 (2)过量酸性KMnO4溶液→品红试液→澄清石灰水。
20.(1)乙 (2)甲方案不可行的理由是:用品红溶液检验生成的二氧化硫时,吸收二氧化硫可能不充分,影响二氧化碳气体的检验;同时气体通过品红溶液和澄清石灰水时,也会打出水汽,影响对生成物中水的检验。
(3)A.验证反应生成的水 B.验证产生的SO
21.(1)2∶1(2)4 (3)
22.(1)N2、O2的体积;(2)偏低;(3)酸性高锰酸钾溶液或溴水
(4)VSO2%=22.4CVa/(22.4CVa+Vb)×100%(其它合理答案也给分)
(5)b、c、e、g或b、e、g或c、e、g。
 工业上测量SO2、N2、O2混合气体中SO2含量的装置如图所示.反应管中装有碘的淀粉溶液.SO2和I2发生的反应为(N2、O2不与I2反应):SO2+I2+2H2O═H2SO4+2HI.
工业上测量SO2、N2、O2混合气体中SO2含量的装置如图所示.反应管中装有碘的淀粉溶液.SO2和I2发生的反应为(N2、O2不与I2反应):SO2+I2+2H2O═H2SO4+2HI.(1)混合气体进入反应管后,量气管内增加的水的体积等于
(2)反应管内溶液蓝色消失后,没有及时停止通气,则测得SO2含量
(3)反应管内的碘的淀粉溶液也可以用
(4)将上述装置改为简易实验装置,除导管外,还需选用的仪器为
a.烧杯 b.试管 c.广口瓶 d.容量瓶 e.量筒 f.单孔塞 g.双孔塞.
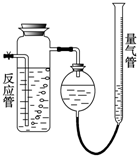 工业上测量SO2、N2、O2混合气体中SO2含量的装置如图所示.反应管中装有碘的淀粉溶液.SO2和I2发生的反应为(N2、O2不与I2反应):SO2+I2+2H2O=H2SO4+2HI
工业上测量SO2、N2、O2混合气体中SO2含量的装置如图所示.反应管中装有碘的淀粉溶液.SO2和I2发生的反应为(N2、O2不与I2反应):SO2+I2+2H2O=H2SO4+2HI(1)混合气体进入反应管后,量气管内增加的水的体积等于
(2)反应管内溶液蓝色消失后,没有及时停止通气,则测得的SO2含量
(3)反应管内的碘的淀粉溶液也可以用
(4)若碘溶液体积为Va mL,浓度为c mol?L-1.N2与O2的体积为Vb mL(已折算为标准状况下的体积).用c、Va、Vb表示SO2的百分含量为

(1)混合气体进入反应管后,量气管中增加的水的体积等于_________的体积(填写气体的分子式)。
(2)反应管内溶液蓝色消失后,没有及时停止通气,则测得的SO2含量_________(填:“偏高”“偏低”或“不受影响”)。
(3)反应管内的碘的淀粉溶液也可以用_________代替(填写物质名称)。
(4)若碘溶液体积为Va mL,浓度为c mol·L-1。N2与O2的体积为Vb mL(已折算为标准状况下的体积)。用c、Va、Vb表示SO2的体积百分含量为:_________。
(5)将上述装置改为简易实验装置,除导管外还需要选用的仪器为_________(填下列仪器的编号)。
a.烧杯 b.试管 c.广口瓶 d.容量瓶e.量筒 f.单孔塞 g.双孔塞
查看习题详情和答案>>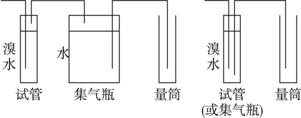
(1)混合气体进入反应管后,量气管内增加的水的体积等于____________的体积(填写气体的化学式)。?
(2)反应管内溶液蓝色消失后,没有及时停止通气,则测得的SO2含量____________(选填“偏高”“偏低”“不受影响”)。?
(3)反应管内的碘的淀粉溶液也可以用____________代替(填写物质名称)。?
(4)若碘溶液体积为VamL,浓度为c mol·L-1,N2与O2的体积为Vb mL(已折算为标准状况下的体积)。用c、Va、Vb表示SO2的体积百分含量为:_____________。?
(5)将上述装置改为简易实验装置,除导管外,还需选用的仪器为_____________(选下列仪器的编号)。
a.烧杯 b.试管 c.广口瓶 d.容量瓶? e.量筒 f.单孔塞 g.双孔塞?
查看习题详情和答案>>(1)混合气体进入反应管后,量气管内增加的水的体积等于的_____________________体积(填写气体的化学式)。
(2)反应管内溶液蓝色消失后,没有及时停止通气,则测得的SO2含量_____________(选填:“偏高”“偏低”或“不受影响”)。
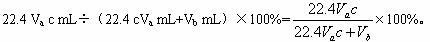
图15-17
(3)反应管内的碘的淀粉溶液也可以用_______________________代替(填写物质名称)。
(4)若碘溶液体积为Va mL,浓度为c mol·L-1。N2与O2的体积为Vb mL(已折算为标准状况下的体积)。用c、Va、Vb?表示SO2的体积百分含量为_______________。
(5)将上述装置改为简易实验装置,除导管外,还需选用的仪器为_____________(选下列仪器的编号)。
a.烧杯 b.试管 c.广口瓶 d.容量瓶 e.量筒 f.单孔塞 g.双孔塞
查看习题详情和答案>>