21. 某实验小组利用如下装置(部分固定装置略)制备氮化钙(Ca3N2),并探究其实验式。
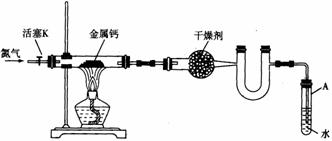
(1)按图连接好实验装置。检查装置的气密性,方法是 .
(2)反应过程中末端导管必须始终插入试管A的水中,目的是 .
(3)制备氮化钙的操作步骤是:①打开活塞K并通入N2;②点燃酒精灯,进行反应;③反应结束后, ;④拆除装置,取出产物。
(4)数据记录如下:
|
空瓷舟质量m0/g |
瓷舟与钙的质量m1/g |
瓷舟与产物的质量m2/g |
|
14.80 |
15.08 |
15.15 |
计算得到实验式CaxN2,其中x= .

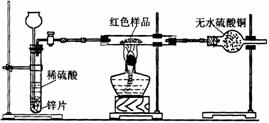 Ⅲ.另一小组设计了新的探究方案,拟通过干燥管中CuSO4是否变蓝来判断样品中是否含有Cu2O,装置如右图所示。
Ⅲ.另一小组设计了新的探究方案,拟通过干燥管中CuSO4是否变蓝来判断样品中是否含有Cu2O,装置如右图所示。