17、(1)常温下,0.1mol·L-1的醋酸和0.1mol·L-1的盐酸各100mL分别与足量的锌粒反应,
产生的气体体积前者____________后者。(填“大于”“等于”“小于”)
(2)常温下0.1mol·L-1的醋酸和pH=1的醋酸各100mL分别与足量的锌粒反应,产生的气
体前者比后者 。
(3)在25℃条件下将pH=5的氯化铵溶液稀释100倍,稀释后溶液的pH为(填选项字母,
下同)
A、5 B、7 C、3 - 5之间 D、5 - 7之间
(4)25℃时,向0.1mol·L-1的醋酸溶液中加入少量醋酸钠晶体,当晶体溶解后测得溶液pH将 。
A、增大 B、减小 C、不变 D、无法确定
(5)室温下,向0.1mol·L-1的H2SO4中加入足量的锌粒,若想减慢制取H2的速率,但又不
影响H2的体积,可以向硫酸溶液中加入 试剂。
A、碳酸钠晶体 B、醋酸钠晶体 C、滴加少量的硫酸铜溶液 D、水
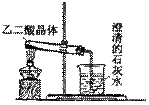 18、课本实验设计得简要明了,但也常存在一些不足,在学习过程中对其进行分析与改进是研究性学习的一个重要课题。
18、课本实验设计得简要明了,但也常存在一些不足,在学习过程中对其进行分析与改进是研究性学习的一个重要课题。
Ⅰ.草酸晶体(H2C2O4·2H2O)受热易分解(分解
温度为175℃),产生CO和CO2。关于草酸晶体
受热分解及验证部分分解产物的实验装置如右图。
(1)写出草酸晶体受热分解的化学方程式:
__________。
(2)设计该装置欲验证的分解产物是 。
(3)草酸晶体的某些物理性质如下表:
|
|
分子式 |
颜色、状态 |
水溶性 |
熔点/℃ |
密度/g·cm-3 |
|
草酸晶体 |
H2C2O4·2H2O |
无色晶体 |
易溶于水 |
101.5 |
1.650 |
有同学认为,用该装置进行实验,存在着不合理因素,请分析指出(任答两点):
①
②
Ⅱ.下图甲是 “铜丝在氯气中燃烧”的演示实验,铜丝在氯气中燃烧的主要现象是 。有人对该实验提出了如下改进方案:
①按下图乙所示连接好装置,并检查气密性;

②取下注射器并集满Cl2;
③点燃酒精灯加热1~2min后,再移开酒精灯。迅速将注射针插入石英玻璃管内,并将Cl2缓缓推入玻璃管中;
④拔出针头,再用同样方法快速向玻璃管中推入空气。请回答:
(1)步骤③中,移开酒精灯、推入Cl2时,观察到铜丝继续保持红热状态,由此可判断,该反应为 反应(填“放热”或“吸热”)。
 (2)步骤④完成后,发现乙试管中的蒸馏水变为蓝绿色。此时缓缓拉动活塞,使少量NaOH溶液吸入乙试管中,看到试管中有
色的沉淀产生,该反应的离方程式为
。
(2)步骤④完成后,发现乙试管中的蒸馏水变为蓝绿色。此时缓缓拉动活塞,使少量NaOH溶液吸入乙试管中,看到试管中有
色的沉淀产生,该反应的离方程式为
。
(3)改进后的实验与课本实验相比较,其优点为
______________。
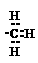 A.
A.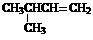 2-甲基-3-丁烯 B.乙炔的结构简式:CHCH
2-甲基-3-丁烯 B.乙炔的结构简式:CHCH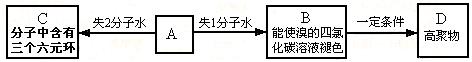
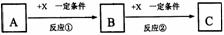 20、 A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。
20、 A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。