26.蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成。由蛇纹石制取碱式碳酸镁的实验步骤如下
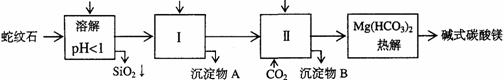
(1)蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是___________(多填少填均不得分)。
|
氢氧化物 |
Fe(OH)3 |
Al(OH)3 |
Mg(OH)2 |
|
开始沉淀pH |
1.5 |
3.3 |
9.4 |
(2)进行Ⅰ操作时,控制溶液pH=7-8
(有关氢氧化物沉淀的pH见右表)
Ca(OH)2不能过量,若Ca(OH)2过量
可能会导致_________溶解、_________沉淀。
(3)从沉淀混合物A中提取红色Fe2O3作颜料,先向沉淀物A中加入足量NaOH溶液,目的是除去沉淀物中可能存在的______________________(填化学式),然后_________、_________、__________、冷却 (依次填写实验操作名称)。
(4)18.2g产品aMgCO3·bMg(OH)2·cH2O完全分解后,产生6.6g CO2和8.0g MgO,由此可知,产品的化学式中:a∶b=__________,由此可推算c=_________。
25.硫酸亚铁是一种可用于治疗缺铁性贫血的药剂,硫酸亚铁药片外表包有一层特制的糖衣,以保护硫酸亚铁不被空气中的氧气氧化成硫酸铁(硫酸铁无治疗贫血的药效)。试设计一个方法,验证某硫酸亚铁药片是否已被氧化(主要步骤、现象、结论)。完成表格中的空白后回答问题。
|
主要步骤 |
现象 |
结论 |
|
1、将硫酸亚铁药片________(填操作名称) |
|
|
|
2、加入_______________溶液 |
|
|
(1)步骤1中常需要用到稀硫酸,主要目的是__________________________________。
(2)步骤2中若_______________现象,说明硫酸亚铁药片已被氧化;若_____________现象,说明硫酸亚铁药片未被氧化。
22.下列五个图中,横坐标表示加入的物质的量,纵坐标表示生成沉淀的量从A--E中选择各题要求的序号填入表中
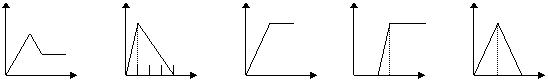
A B C D E
|
溶液 |
加入的物质 |
答案序号 |
|
饱和石灰水 |
通CO2至过量 |
|
|
AlCl3溶液 |
通过量的NH3 |
|
|
含少量NaOH的NaAlO2溶液 |
通过量的CO2 |
|
|
NaAlO2溶液 |
滴加稀HCl至过量 |
|
|
MgCl2 AlCl3的混和液 |
滴加NaOH至过量 |
|
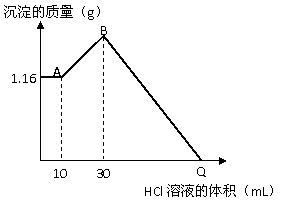 把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量的水后,有1.16 g白色沉淀产生。在所得的悬浊液中逐滴加入1 mol/L HCl溶液,沉淀的总质量与加入HCl的体积的关系如右图所示。试计算回答:
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量的水后,有1.16 g白色沉淀产生。在所得的悬浊液中逐滴加入1 mol/L HCl溶液,沉淀的总质量与加入HCl的体积的关系如右图所示。试计算回答: CO2+ K2SO4+ Cr2(SO4)3+
CO2+ K2SO4+ Cr2(SO4)3+ 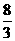 价来计算)··············· ( )
价来计算)··············· ( )