22.(12分) 实验室常利用甲醛(HCHO)法测定(NH4)2SO4样品中氮元素的质量分数,其反应原理为:4NH4++6HCHO=3H++6H2O+(CH2)6N4H+,然后用NaOH标准溶液滴定反应生成的酸[滴定时,1mol (CH2)6N4H+与1mol H+相当]。某兴趣小组用甲醛法进行了如下实验:
步骤I:准确称取样品1.4 g。
步骤Ⅱ:将样品溶解后,完全转移到250
mL容量瓶中,定容,充分摇匀。
步骤Ⅲ:移取25.00 mL样品溶液于250 mL锥形瓶中,加入10 mL 20%的中性甲醛溶液(足量)并摇匀,静置5
min后加入1-2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
实验室常利用甲醛(HCHO)法测定(NH4)2SO4样品中氮元素的质量分数,其反应原理为:4NH4++6HCHO=3H++6H2O+(CH2)6N4H+,然后用NaOH标准溶液滴定反应生成的酸[滴定时,1mol (CH2)6N4H+与1mol H+相当]。某兴趣小组用甲醛法进行了如下实验:
步骤I:准确称取样品1.4 g。
步骤Ⅱ:将样品溶解后,完全转移到250
mL容量瓶中,定容,充分摇匀。
步骤Ⅲ:移取25.00 mL样品溶液于250 mL锥形瓶中,加入10 mL 20%的中性甲醛溶液(足量)并摇匀,静置5
min后加入1-2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
根据步骤Ⅲ填空:
(1)NaOH标准溶液应装在 (填“酸式”或“碱式”)滴定管。当滴定达到终点时,锥形瓶中溶液的颜色是 色。
(2)若所用滴定管的量程是25.00 mL,当管内凹液面最低处位于4.00 mL时,管内所装溶液的体积为 。
A.等于4.00 mL B.大于4.00 mL C.等于21.00 mL D.大于21.00 mL
(3)在滴定过程中应边滴边摇动锥形瓶,眼睛应注视 。 A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化 C.锥形瓶内溶液体积的变化 D.液体的滴速
(4)滴定结果如下表所示:
|
滴定次数 |
待测溶液的体积/mL |
标准溶液的体积 |
|
|
滴定前刻度/mL |
滴定后刻度/mL |
||
|
1 |
25.00 |
1.02 |
21.03 |
|
2 |
25.00 |
2.00 |
21.99 |
|
3 |
25.00 |
0.20 |
20.20 |
若NaOH标准溶液的浓度为0.1 mol/L,则该样品中氮元素的质量分数为 。
(5)下列操作可能会使测得的结果偏高的是 。
A.碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定 B.锥形瓶用蒸馏水洗涤后,未用待装溶液润洗
C.滴定前碱式滴定管的尖嘴处有气泡,滴定后消失
D.滴定完成后仰视读数
E.终点时颜色发生变化后立即读数
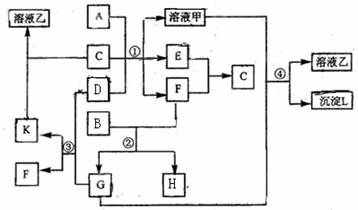
 2009年重庆一中高2011级月考
2009年重庆一中高2011级月考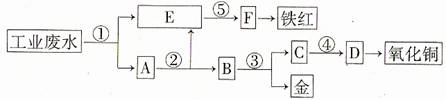
 8SO2+2Fe2O3,该反应的氧化产物是
,当生成8 mol SO2时转移电子的物质的量为 。
8SO2+2Fe2O3,该反应的氧化产物是
,当生成8 mol SO2时转移电子的物质的量为 。 2SO3。某科技小组的同学在一个恒温恒容的容器中模拟该反应,他们分两次进行实验,第一次向容器中加入2 mol SO2、1 mol O2,反应达平衡后测得SO2的转化率为α1,第二次向容器中加入3 mol SO2、1.5 mol O2,
反应达平衡后测得SO2的转化率为α2,则α1 α2(填“大于”、“等于”或“小于”)。
2SO3。某科技小组的同学在一个恒温恒容的容器中模拟该反应,他们分两次进行实验,第一次向容器中加入2 mol SO2、1 mol O2,反应达平衡后测得SO2的转化率为α1,第二次向容器中加入3 mol SO2、1.5 mol O2,
反应达平衡后测得SO2的转化率为α2,则α1 α2(填“大于”、“等于”或“小于”)。