0 26678 26686 26692 26696 26702 26704 26708 26714 26716 26722 26728 26732 26734 26738 26744 26746 26752 26756 26758 26762 26764 26768 26770 26772 26773 26774 26776 26777 26778 26780 26782 26786 26788 26792 26794 26798 26804 26806 26812 26816 26818 26822 26828 26834 26836 26842 26846 26848 26854 26858 26864 26872 447348
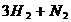

 。A.
。A.  B.
B. 
 C(g)+D(g)已达平衡的是
C(g)+D(g)已达平衡的是 =
= 
 若 aA(g) + bB(g)
cC(g)
若 aA(g) + bB(g)
cC(g)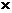
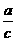 = a 和 y + z
= a 和 y + z = b
= b 再用滴管滴入5ml盐酸于试管中。试回答下列问题:
再用滴管滴入5ml盐酸于试管中。试回答下列问题: 可以在一定条件下和
可以在一定条件下和 反应生成无毒物,其反应式可表示为
反应生成无毒物,其反应式可表示为 ,该反应的氧化剂是________,还原剂是________,每有1mol
,该反应的氧化剂是________,还原剂是________,每有1mol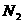 生成,反应中转移的电子为_____mol.
生成,反应中转移的电子为_____mol. Si+2CO↑,在该反应中氧化剂是________ __________ ___________,
Si+2CO↑,在该反应中氧化剂是________ __________ ___________,