26.(8分)合成氨原料可以由天然气制取。其主要反应为:CH4(g)+H2O(g)→CO(g)+3H2(g)
(1)1m3(标准状况)CH4按上式完全反应,产生H2 mol。
(2)CH4和O2的反应为:2CH4(g)+O2(g)→2CO(g)+4H2(g)
设CH4同时和H2O(g)及O2(g)反应。1m3(标准状况)CH4按上述两式完全反应,产物气体的体积V(标准状况)为 。
(3)CH4和H2O(g)及富氧空气(O2含量较高,不同富氧空气氧气含量不同)混合反应,产物气体组成如下表:
|
气体 |
CO |
H2 |
N2 |
O2 |
|
体积(L) |
25 |
60 |
15 |
2.5 |
计算该富氧空气中O2和N2的体积比V(O2)/V(N2)。
(4)若CH4和H2O(g)及富氧空气混合反应的产物中,V(H2)/V(N2)=3︰1 (合成氨反应的最佳比),则反应中的H2O(g)和富氧空气的体积比为何值?
20.(6分)有NO2和N2O4常温常压下A.B.C.D均为气态。A与B可发生可逆反应:
A +
B 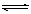 C +nD。若将2 mol A和2 mol B混合充入体积可变的密闭容器中,在
C +nD。若将2 mol A和2 mol B混合充入体积可变的密闭容器中,在
不同条件下达到平衡时C的浓度如下
|
温度 |
压强(kPa) |
C平衡浓度mol•L-1 |
|
25℃ |
100 |
1.0 |
|
25℃ |
200 |
1.8 |
|
25℃ |
300 |
3.2 |
|
25℃ |
400 |
6.0 |
(1)可逆反应中系数n的取值范围为______________理由 ________________________
(2)在500kPa时,D的状态可能为__________________________
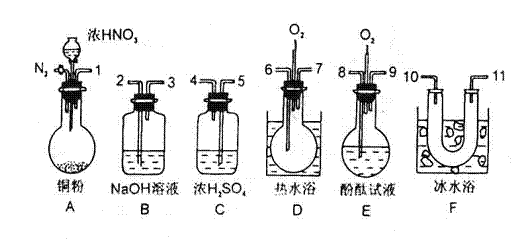
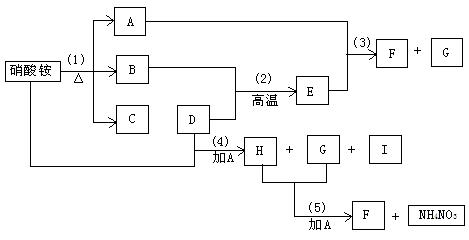 23.(5分)如图表示
23.(5分)如图表示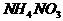 和D物质为起始反应物发生的一系列变化,其中在常温下A 为液体,F为不溶于水和碱溶液的白色固体,B.G、I为无色气体,其中G能使湿润的红色石蕊试纸变蓝。
和D物质为起始反应物发生的一系列变化,其中在常温下A 为液体,F为不溶于水和碱溶液的白色固体,B.G、I为无色气体,其中G能使湿润的红色石蕊试纸变蓝。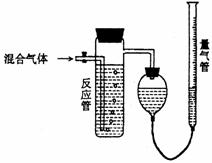 工业上测量SO2、N2、O2混合气体中
工业上测量SO2、N2、O2混合气体中