23.(本小题6分)电石中的碳化钙和水能完全反应:
CaC2+2H2O=C2H2↑+Ca(OH)2
 使反应产生的气体排水,测量排出水的体积,可计算出标准状况乙炔的体积,从而可测定电石中碳化钙的含量。
使反应产生的气体排水,测量排出水的体积,可计算出标准状况乙炔的体积,从而可测定电石中碳化钙的含量。
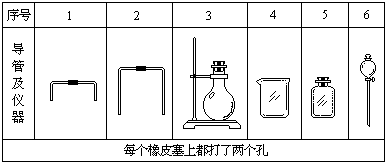
(1)若用下列仪器和导管组装实验装置:
如果所制气体流向从左向右时,上述仪器和导管从左到右直接连接的顺序(填各仪器、导管的序号)是( )接( )接( )接( )接( )接( )。(2分)
(2)仪器连接好后,进行实验时,有下列操作(每项操作只进行一次):
①称取一定量电石,置于仪器3中,塞紧橡皮塞。
②检查装置的气密性。.
③在仪器6和5中注入适量水。
④待仪器3恢复到室温时,量取仪器4中水的体积(导管2中的水忽略不计)。
⑤慢慢开启仪器6的活塞,使水逐滴滴下,至不发生气体时,关闭活塞。
正确的操作顺序(用操作编号填写)是 。(2分)
(3)若实验产生的气体有难闻的气味,且测定结果偏大,这是因为电石中含
有 杂质。(1分)
(4)若实验时称取的电石1.60克,测量排出水的体积后,折算成标准状况乙炔的体积为448毫升,此电石中碳化钙的百分含量是 %。(1分)
|
|
季碳原子,数目分别用n1、n2、n3、n4表示。例如 分子中n1=6,
n2=1,n3=2,n4=1。试根据不同烷烃的组成和结构,分析出烷烃(除甲烷外)中各原子数的关系。
(1)烷烃分子中氢原子个数为n0。n0与n1、n2、n3、n4的关系是:n0= 或
n0= 。
(2)四种碳原子数之间的关系为n1= 。
(3)若某分子中 n2=n3=n4=1,则该分子的结构简式可能是(写其中一种) 。
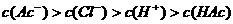
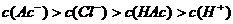
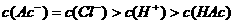
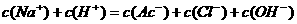
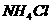 晶体,则溶液颜色( )
晶体,则溶液颜色( )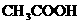 B.
B.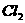 C.
C.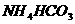 D.
D.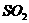
 ,在不同温度下其离子积常数为
,在不同温度下其离子积常数为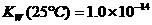 ,
,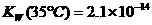 .则下列叙述正确的是( )
.则下列叙述正确的是( )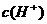 随着温度的升高而降低 B.在35℃时,水中的
随着温度的升高而降低 B.在35℃时,水中的