17 (6分)(1)1mol/L的CaCl2 溶液0.5L,Cl- 离子的物质的量浓度为___________mol/L
(2)标准状况下,33.6L的NH3所具有的物质的量为_________mol,将其溶解于水配成1L的溶液,则溶液的物质的量浓度为__________mol/L
18 (4分)就有关物质的分离回答下面的问题
(1)现有一瓶A和B的混合液,已知它们的性质如下表。
|
物质 |
熔点/oC |
沸点/oC |
密度/g·cm-3 |
溶解性 |
|
A |
-11.5 |
198 |
1.11 |
A、B互溶,且均易溶于水 |
|
B |
17.9 |
290 |
1.26 |
据此分析,将A和B相互分离的常用方法是:
(2)在分液漏斗中用一种有机溶剂萃取水溶液里的某物质时,静置分层后,如果不知道哪一层液体是“水层”,试设计一种简便的判断方法。答:
19(10分)下表是某地市场上销售的一种“加碘盐”包装上的部分文字说明。請根据此表,结合中学学过的化学知识,回答下列问题:
|
配料表 |
精制海盐、碘酸钾(KIO3) |
|
含碘量 |
20―40mg/kg |
|
储藏方法 |
密封避光、防潮 |
|
食用方法 |
烹调时待食品熟后加入碘盐 |
(1)据物质分类中的树状分类法有关知识,在①HIO3 ②碘酸钠 ③KOH ④I2O5 ⑤NaCl五种 (填“混合物”或“化合物”或“盐”或“氧化物”)中与碘酸钾(KIO3)属于同类物质的有 。(填序号)
(2)推测出碘酸钾(KIO3)的物理性质:碘酸钾(KIO3) 溶于水(填“能”或“不能”),化学性质:碘酸钾(KIO3)在受热时 。
20 (9分)实验室制配0.5 mol/L的NaOH溶液500 mL,有以下仪器:①烧杯
②100 mL量筒 ③1000 mL容量瓶 ④500 mL容量瓶 ⑤玻璃棒
⑥托盘天平(带砝码) ⑦滴定管
(1)配制时,必须使用的仪器有____________(填代号),还缺少的仪器是___ 。
(2)实验两次用到玻璃棒,其作用分别是:______________、______________。
(3)配制时,一般可分为以下几个步骤:①称量 ②计算 ③溶解 ④摇匀 ⑤转移⑥洗涤⑦定容⑧冷却。其正确的操作顺序为_______________ 。
21 (13分)四只试剂瓶中分别盛装有NaNO3溶液、Na2CO3溶液、Na2SO4溶液和NaCl溶液,就如何检验这四种溶液分别解答下列各题。
在四支试管中分别取四种溶液各1mL,做下列实验。
(1)在四支试管中分别滴入 ,现象是
离子方程式是 。
(2)在剩余三支试管中分别滴入 ,现象是
离子方程式是 。
(3)在剩余两支试管中分别滴入 ,现象是
离子方程式是 。
三次实验中都没有明显现象的是 。
三 计算题(本题包括1小题,共10分)
22 (10分)将6.50 g锌投入200 mL某浓度的盐酸中,锌和盐酸恰好完全反应。求:(Zn:65)
(1)6.50 g锌的物质的量
(2)所用盐酸中HCl中的物质的量浓度
(3)反应中生成的H2在标准状况下的体积高一化学(必修1)期中考试试题答案
第Ⅰ卷 选择题(共48分)
一 选择题(每题只有一个选项符合题意,每小题3分,共48分)
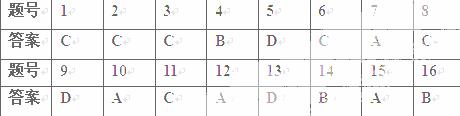
第Ⅱ卷 (非选择题 共52分)
22、(1)、NaHSO4在溶液中的电离方程式为:
(2)、向NaHSO4溶液中滴入Ba(OH)2溶液至中性,其离子方程式为
(3)、向NaHCO3溶液中滴加过量的Ba(OH)2溶液 ,其离子方程式为

 L B.
L B.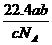 L C.
L C.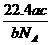 L D.
L D.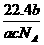 L
L 和
和 的混合气体共5.04L(STP),点燃恰好可以完全反应,通过计算回答:
的混合气体共5.04L(STP),点燃恰好可以完全反应,通过计算回答:
 溶液中充分反应,则消耗该
溶液中充分反应,则消耗该
 3Fe+4CO2的反应中, 是氧化剂, 是还原剂,__________元素被氧化,________元素被还原。
3Fe+4CO2的反应中, 是氧化剂, 是还原剂,__________元素被氧化,________元素被还原。