27.(10分)氢氧化钠与盐酸发生中和反应的化学方程式为 ▲ ,
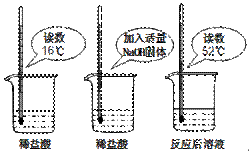 (1)为证明中和反应是放热反应,某小组进行了如图所示的
(1)为证明中和反应是放热反应,某小组进行了如图所示的
实验操作:根据下图实验,甲同学认为:NaOH与稀盐酸发生的中和反应是放热反应。乙同学认为:甲同学得出这个结论的依据不科学,理由是 ▲ ;丙同学认为:通过多个实验才能得出一个普遍的结论。请你再举出一个酸碱中和反应的实例,写出反应物的化学式 ▲ 。
(2)为探究影响中和反应放出热量多少的因素,他们又进行了如下实验:在编号为A、B、C、D、E的五只烧杯中各装入36.5g 溶质质量分数为5%、10%、15%、20%、25%的盐酸,再向上述五只烧杯中分别加入40g20% 的氢氧化钠溶液,最后测量其温度,数据记录如下:
|
烧杯编号 |
A |
B |
C |
D |
E |
|
盐酸的溶质质量分数 |
5% |
10% |
15% |
20% |
25% |
|
反应后溶液温度(℃) |
24℃ |
34℃ |
46℃ |
54℃ |
54℃ |
[实验结论]影响中和反应放出热量多少的因素是 ▲ 。
[交流反思]反应后,烧杯内溶液pH最小的是 ▲ (填烧杯编号);
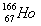 可有效地治疗肝癌。该同位素原子核内的中子数为
可有效地治疗肝癌。该同位素原子核内的中子数为
 表示氢原子,用
表示氢原子,用 表示氧原子,则
表示氧原子,则 表示 ▲ (填化学符号);
表示 ▲ (填化学符号);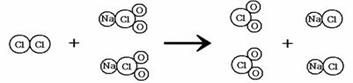 的微观过程如图所示。
的微观过程如图所示。