19.(10分)将洁净的金属片Fe、Zn 、A、B 分别与Cu用导线连结浸在合适的电解质溶液里。实验并记录电压指针的移动方向和电压表的读数如下表所示:
|
金属 |
电子流动方向 |
电压/V |
|
Fe |
Fe
→ Cu |
+0.78 |
|
Zn |
Zn
→ Cu |
+1.10 |
|
A |
Cu
→ A |
-0.15 |
|
B |
B
→ Cu |
+0.3 |
根据以上实验记录,完成以下填空:
(1)构成两电极的金属活动性相差越大,电压表的读数越___________(填“大”、“小”)。
Zn、A、B三种金属活动性由强到弱的顺序是__________________________。
(2)Cu与A组成的原电池,_____为负极,此电极反应式为___________________。
(3)A、B形成合金,露置在潮湿空气中,_______先被腐蚀。
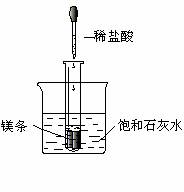
 20.(8分)在50mLH2O2水溶液中加入2g二氧化锰,在
20.(8分)在50mLH2O2水溶液中加入2g二氧化锰,在
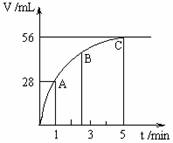
标准状况下放出气体的体积与时间的关系如图所示:
(1)该反应还可用______________代替二氧化锰做催
化剂加快反应速率。
(2)A、B、C各点所表示的反应速率由快到慢的顺序
为______________。
试解释反应速率变化的原因是_________________
__________________________________________。
 (3)该H2O2水溶液的物质的量浓度为_____________________________。
(3)该H2O2水溶液的物质的量浓度为_____________________________。
 2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。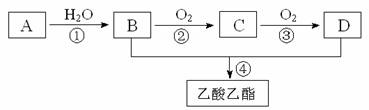
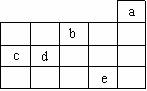 A.b元素除0价外,只有一种化合价
A.b元素除0价外,只有一种化合价