0 205948 205956 205962 205966 205972 205974 205978 205984 205986 205992 205998 206002 206004 206008 206014 206016 206022 206026 206028 206032 206034 206038 206040 206042 206043 206044 206046 206047 206048 206050 206052 206056 206058 206062 206064 206068 206074 206076 206082 206086 206088 206092 206098 206104 206106 206112 206116 206118 206124 206128 206134 206142 447348
 等份。现用它测量金属丝的直径,如图甲所示,则此金属丝的直径是_________mm
等份。现用它测量金属丝的直径,如图甲所示,则此金属丝的直径是_________mm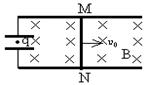 直导轨放有一导体棒MN.导轨左端接有极板水平的平行板电容器,其两极间
直导轨放有一导体棒MN.导轨左端接有极板水平的平行板电容器,其两极间 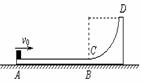 (1)小物块与水平轨道的动摩擦因数
(1)小物块与水平轨道的动摩擦因数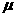 。
。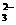 、NO3-、Cl-中的一种或几种。取该种溶液少许,加入NaOH溶液并加热,观察到白色沉淀生成并伴有刺激性气味的气体产生。沉淀过滤后,在沉淀中继续加入过量NaOH溶液,白色沉淀部分溶解,试回答下列问题:
、NO3-、Cl-中的一种或几种。取该种溶液少许,加入NaOH溶液并加热,观察到白色沉淀生成并伴有刺激性气味的气体产生。沉淀过滤后,在沉淀中继续加入过量NaOH溶液,白色沉淀部分溶解,试回答下列问题: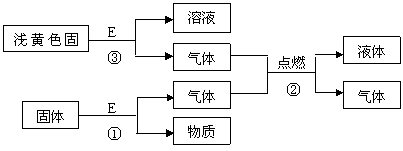
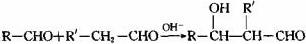 ,有机物G属于酯类,其分式为C20H18O4,合成G的路线如下图,其中C的分子式为C9H8O2
,有机物G属于酯类,其分式为C20H18O4,合成G的路线如下图,其中C的分子式为C9H8O2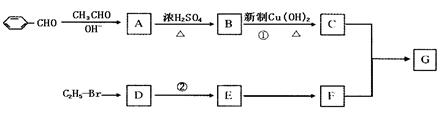
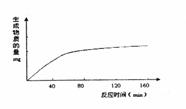 (1)该酶作用后的产物是 。如将溶液的PH
(1)该酶作用后的产物是 。如将溶液的PH 缘刚进入磁场和刚穿出磁场时刻的速度都是v0,则在整个线圈穿过磁场的全过程中 (从下边缘进入磁场到
缘刚进入磁场和刚穿出磁场时刻的速度都是v0,则在整个线圈穿过磁场的全过程中 (从下边缘进入磁场到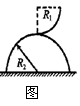 D.线圈的最小速度一定是
D.线圈的最小速度一定是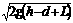
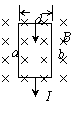 金属导体板宽为d,通以如图所示方向的电流,其中自由电子定 向运动的速度为v,整个导体板置于磁感
金属导体板宽为d,通以如图所示方向的电流,其中自由电子定 向运动的速度为v,整个导体板置于磁感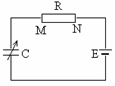 D.它们振动过程中的任意1s内通过路程均为2.0cm
D.它们振动过程中的任意1s内通过路程均为2.0cm 如图5所示,放在粗糙水平桌面上的木块,质量m = 2.0kg,同时受到F1 =8.0N、F2 =3.0N的水平推力作用处于静止状态。若只撤去F1,则木块
如图5所示,放在粗糙水平桌面上的木块,质量m = 2.0kg,同时受到F1 =8.0N、F2 =3.0N的水平推力作用处于静止状态。若只撤去F1,则木块 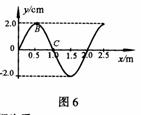 D.以a = 1.5m/s2的加速度向左做匀加速运动
D.以a = 1.5m/s2的加速度向左做匀加速运动