28.(7分)小明设计了如下图所示的实验装置来证明氧化铜能加快过氧化氢溶液的分解,并与相同条件下MnO2的催化效果做比较,实验时间均以生成30 mL气体为准(即比较反应速率)。用图示装置测量产生气体的体积,其它可能影响实验因素均已忽略,相关数据如下:
|
实验序号 |
过氧化氢溶液体积 |
催化剂 |
待测数据 |
|
① |
15mL |
无 |
|
|
② |
15mL |
CuO(0.5g) |
|
|
③ |
15mL |
MnO2(0.5g) |
|
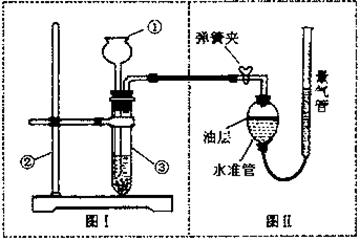
(1) 检查图(I)装置气密性的方法是: ;
(2) 图(Ⅱ)装置中油层的作用是 。
(3)从设计原理看,实验中的“待测数据”可以是指 。
(4)为了较准确地测量气体体积,在读取反应前后量气管中液面的读数的过程中,应注意 (填字母编号) 。
a.视线与凹液面最低处相平 b.读数前不能移动量气管和水准管
c.保持水准管静止,待水准管中液面不再上升时,立刻读数
d.读数前应上下移动水准管,待两管液面相平再读数
(5)如果要进一步探究CuO是否是该反应的催化剂,请完成下列实验。
|
实验步骤和现象 |
设计这一步骤的目的 |
|
(1)取15mL过氧化氢溶液,加入0.5g CuO后,产生O2的速率比未加入时快得多 |
证明CuO能加快过氧化氢溶液的分解的速率 |
|
(2)将反应后的溶液过滤,烘干并称量CuO质量,质量为0.5g |
。 |
|
(3)
。 |
。 |
26.(8分)结合下列各图装置,回答有关问题。
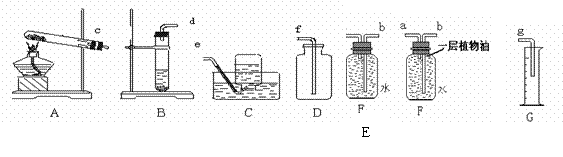
(1)实验室中,用加热高锰酸钾的方法制取氧气,发生装置可选用 (填序号),该反应的化学方程式为 。
(2)氢气是最清洁的燃料,密度比空气小,难溶于水,实验室常用锌粒与稀硫酸反应来制得。其制备氢气发生装置和收集装置可选用 。(填序号)。
(3) 实验室用石灰石与稀盐酸反应制备二氧化碳,并测定所收集的二氧化碳的体积,应选用的装置是(填序号) 。该反应的化学方程式为 。

|
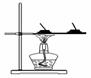
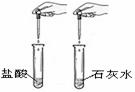 (4)用下列实验装置完成对应实验(部分仪器已省略),操作正确并能达到实验目的的是
。
(4)用下列实验装置完成对应实验(部分仪器已省略),操作正确并能达到实验目的的是
。


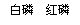 |
|||
|


22. A、B、C三种物质各15g,它们化合时只能生成30g新物质D。若增加10gA,则反应停止后,原反应物中只剩余C。根据上述条件推断,下列说法正确的是
A. 第一次反应停止后,B剩余9g B. 第二次反应后,D的质量为60g
C. 反应中A和B的质量比是3 :2 D. 反应中A和C的质量比是5 :2
2010年名山二中 理化“中考二诊”试题
化学第II卷(非选择题,共36分)
班级 姓名 成绩
第I卷选择题答案:
|
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
21 |
22 |
|
|
|
|
|
|
|
|
|
|
|
|
|

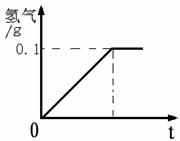 某地震科研小组取用了一包氧化亚铁样品10克(杂质不参与反应)与高温下的水蒸气进行反应,其反应图象如下所示。
某地震科研小组取用了一包氧化亚铁样品10克(杂质不参与反应)与高温下的水蒸气进行反应,其反应图象如下所示。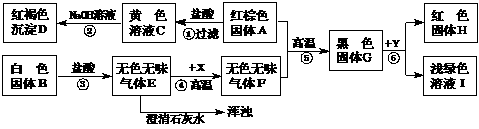
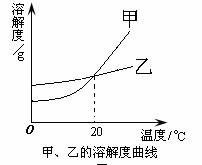 A.甲的溶解度比乙的溶解度大
A.甲的溶解度比乙的溶解度大