0 18350 18358 18364 18368 18374 18376 18380 18386 18388 18394 18400 18404 18406 18410 18416 18418 18424 18428 18430 18434 18436 18440 18442 18444 18445 18446 18448 18449 18450 18452 18454 18458 18460 18464 18466 18470 18476 18478 18484 18488 18490 18494 18500 18506 18508 18514 18518 18520 18526 18530 18536 18544 447348
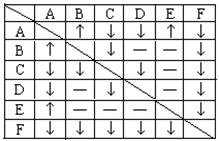 有A、B、C、D、E、F六瓶未知溶液。它们
有A、B、C、D、E、F六瓶未知溶液。它们 验,结果如右表。表中“¯”表示有沉淀或生成微溶
验,结果如右表。表中“¯”表示有沉淀或生成微溶