2.下列说法不正确的是 [ ]
A.钙、铁是人体必需的微量元素
B.人体中的酶是一种重要的蛋白质
C.维生素有二十多种,它们多数在人体内不能合成
D.葡萄糖在人体中酶的作用下,缓慢氧化生成二氧化碳和水
23.(10分)“过氧化钠(Na2O2)”是一种淡黄色固体,能与水或二氧化碳反应放出氧气。实验室有一份放置了较长时间的过氧化钠粉末,已发生了部分变质,小明想知道当中的成分,决定开展科学探究。
[提出问题]变质的过氧化钠粉末中有哪些成分?
[收集资料]2Na2O2+2H2O====4NaOH+O2↑,2Na2O2+2CO2====2Na2CO3+O2。
[猜 想]
猜测一:变质的过氧化钠粉末是Na2O2和NaOH的混合物;
猜测二:变质的过氧化钠粉末是 的混合物;
猜测三:变质的过氧化钠粉末是Na2O2、NaOH和Na2CO3的混合物。
[实验探究]
|
实验操作 |
实验现象 |
实验结论 |
|
①取3.00g变质的过氧化钠粉末于一支大试管里,加入适量的水,共收集到0.32g气体,用
检验该生成的气体。 |
|
证明粉末中有Na2O2。 |
|
②在①的反应液中加入足量的Ba(NO3)2溶液,充分反应。 |
白色沉淀 |
证明粉末中有
。 |
|
③将②反应液过滤、洗涤、干燥和称量,得固体1.97g。 |
|
[数据处理及结论]
通过对上面实验数据的综合计算,证明猜测 (选填“一”、“二”、“三”)成立。
[反 思]
(1)H2O2、Na2O2是一类特殊的氧化物,与H2O、CO2、Na2O等常见的氧化物相比较,氧元素的化合价不同。试推断H2O2与Na2O2中氧元素的化合价均为 。
 (2)小明想改变[实验探究]的实验设计,在第②步反应后的反应液中加入硫酸铜溶液,得到了蓝色沉淀,于是证明变质的过氧化钠粉末中有NaOH。老师对小明的设计提出了质疑,原因是
。
(2)小明想改变[实验探究]的实验设计,在第②步反应后的反应液中加入硫酸铜溶液,得到了蓝色沉淀,于是证明变质的过氧化钠粉末中有NaOH。老师对小明的设计提出了质疑,原因是
。
 (10分)有一瓶因保存不当而部分变质的氢氧化钠固体(假设杂质只有碳酸钠),为测定其组成,称取一定质量固体样品,向其中滴加溶质质量分数为7.3%的稀盐酸,放出二氧化碳气体质量与加入稀盐酸的质量关系如下图所示。试求:
(10分)有一瓶因保存不当而部分变质的氢氧化钠固体(假设杂质只有碳酸钠),为测定其组成,称取一定质量固体样品,向其中滴加溶质质量分数为7.3%的稀盐酸,放出二氧化碳气体质量与加入稀盐酸的质量关系如下图所示。试求: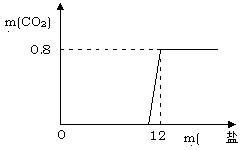 (2)样品总质量是多少克?
(2)样品总质量是多少克?
 (12分)A、B可发生中和反应,D是生活中最常见的液体。通常情况下,F、G、I为气体,且F是一种清洁能源。x是目前应用最广泛的金属,y常用作食品干燥剂。各物质间的转化关系如图所示(个别产物略去)。
(12分)A、B可发生中和反应,D是生活中最常见的液体。通常情况下,F、G、I为气体,且F是一种清洁能源。x是目前应用最广泛的金属,y常用作食品干燥剂。各物质间的转化关系如图所示(个别产物略去)。