30. (7分) 某课外活动小组为测定当地石灰石中含碳酸钙的质量分数,取来了一些矿石,并取稀盐酸200g,平均分成4份,进行实验,结果如下:
|
实验 |
1 |
2 |
3 |
4 |
|
加入样品的质量/g |
5 |
10 |
15 |
20 |
|
生成CO2的质量/g |
1.54 |
3.08 |
4.4 |
m |
⑴哪几项反应中盐酸有剩余______________;⑵ m= __________________;
⑶试计算这种石灰石矿中碳酸钙的质量分数。
31 (6分)中国是一个人口众多的发展中国家,人们注意到:西方国家的发展模式不完全适用于中国,例如:
(1)设想中国每家都有轿车,则每天需供应8000万桶石油(目前全世界每天的产油量约为6700万桶),如果每7桶石油为1吨,每吨石油能提炼出70%(质量分数)的燃料油,以燃料油中平均含C、H原子比例为10∶22(燃烧产物为二氧化碳、水)计算,到那时,中国由于轿车燃油将可能每天排放温室气体多少万吨?
(2)设想以植物性食物为主的中国人,平均食用牛肉的水平若与美国人相当,则每年需增加粮食3.4亿吨(这相当于美国一年的粮食产量),如果每吨粮食生产需提供0.1吨氮元素,则:
①中国每年将需要多供应多少吨尿素[CO(NH2)2]?
②尿素生产原理为: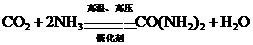 ,据此计算:为增产尿素,需再建年产20万吨合成氨的工厂几座?
,据此计算:为增产尿素,需再建年产20万吨合成氨的工厂几座?
25.(3分)在化学反应中,物质所含元素的化合价发生变化的反应就是氧化还原反应。例如: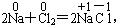 反应前后,Na、Cl的化合价发生了变化,该反应是氧化还原反应。
反应前后,Na、Cl的化合价发生了变化,该反应是氧化还原反应。
(1)根据化合价是否变化分析下列反应属于氧化还原反应的是(填序号) 。
A.2Mg+O2 2MgO B.CaO+H2O=Ca(OH)2
C.2KClO3
2MgO B.CaO+H2O=Ca(OH)2
C.2KClO3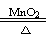 2KCl+3O2↑ D.CaCO3
2KCl+3O2↑ D.CaCO3 CaO+CO2↑
E.H2+CuO
CaO+CO2↑
E.H2+CuO Cu+H2O F.HCl+NaOH=NaCl+H2O (2)根据上面的分析推理,对下列两种基本反应类型是否属于氧化还原反应,作出恰当的概括。
化合反应: 。
分解反应: 。
26.(4分)(9分)一氧化氮是大气的主要污染物之一。近几年来,又发现在生物体内存在少量的一氧化氮,它有扩张血管和增强记忆力的功能,成为当前生命科学研究的热点。
Cu+H2O F.HCl+NaOH=NaCl+H2O (2)根据上面的分析推理,对下列两种基本反应类型是否属于氧化还原反应,作出恰当的概括。
化合反应: 。
分解反应: 。
26.(4分)(9分)一氧化氮是大气的主要污染物之一。近几年来,又发现在生物体内存在少量的一氧化氮,它有扩张血管和增强记忆力的功能,成为当前生命科学研究的热点。
|
4X+5O2 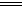 4NO+6H2O,根据质量守恒定律推断,X的化学式为
。
4NO+6H2O,根据质量守恒定律推断,X的化学式为
。
⑵汽车尾气中含有一氧化氮、一氧化碳等有毒气体,治理的方法是在汽车尾气的排风管上装一个催化转换器,在催化剂的作用下,一氧化氮与一氧化碳反应可生成二氧化碳和氮气,该反应的化学方程式为: 。
⑶某同学希望了解尾气中一氧化碳的含量,于是在环保科研人员的帮助下,采集了一定量的汽车尾气,并把它转化为二氧化碳和氮气。下面该同学该怎样将二氧化碳和氮气分开呢?并设法计算出一氧化碳的含量 。

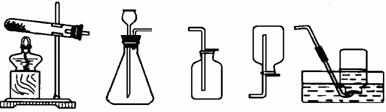
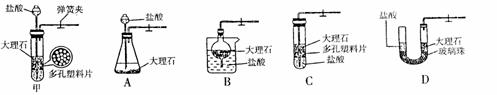
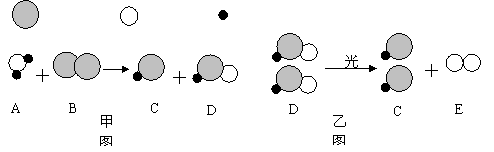 (6分)自来水消毒过程中通常会发生如下化学反应,其反应的微观过程可用下图表示:
(6分)自来水消毒过程中通常会发生如下化学反应,其反应的微观过程可用下图表示:
