摘要:空气的组成测定中的化学反应方程式:
网址:http://m.1010jiajiao.com/timu3_id_92893[举报]
化学兴趣小组的同学在报纸上看到这样一则新闻报道:《杭州一大货车载电石狂奔燃烧 火龙震撼 仿佛好莱坞大片》某日凌晨2点50分左右,一辆满载20吨电石的挂车,在杭州滨江区江南大道信诚路口燃起熊熊大火,黑烟如蘑菇升空,不时发出“嘭嘭”爆炸声.让电石起火的是雨水,电石遇水燃烧爆炸.而雨一直下,燃烧现场一直无法处理.从火灾发生到初步控制住,一共用掉4吨干粉.电石,学名碳化钙(CaC2),是由生石灰和焦炭在电炉中加热到2000℃生成.电石的化学性质非常活泼,遇水就会发生剧烈化学反应,生成一种可燃气体乙炔和一白色固体物质,并放出大量的热.所以,水不能灭这个火,水在其中的角色是助燃!电石起火在正常情况下,可以用磷酸盐干粉、干黄沙和水泥进行覆盖、隔离扑灭.但因为现场雨下得很大,这三种物质无法完全发挥作用,只能就近让它烧光.
针对以上新闻内容,大家展开了热烈的讨论:
【讨论交流】
(1)关于电石引起的燃烧,需要满足燃烧的三个条件分别为:①需要可燃物②可燃物与氧气接触③ .文中画线处灭火方法所对应的原理为:
(2)根据元素守恒思想对电石与水反应后生成的白色固体物质进行了三种猜想,猜想A:氧化钙;猜想B:氢氧化钙;猜想C:是碳酸钙,同学们经过分析将猜想排除,并设计了如下实验来验证该固体物质:
(3)同学们对于可燃气体乙炔很感兴趣,想通过设计实验来得出乙炔的化学式
查阅资料:
已知乙炔是一可燃性气体,由碳氢元素组成,一个乙炔分子中共有四个原子构成.
实验设计:
将一定量的乙炔气体与足量氧气混合在一密闭容器内将其引燃.生成的混合气体缓缓通过以下吸收装置.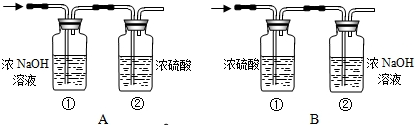
交流讨论:
由于涉及了两套吸收装置,实验小组的两位同学对于上述实验装置A和装置B的选用发生了争执,你认为应该选择 .
实验测定:
经讨论后,他们选定了实验装置,进行实验. 记录数据于下表中
Ⅰ.试通过计算,判断乙炔的化学式 写出计算过程;
Ⅱ.请写出电石与水反应的化学方程式 .
查看习题详情和答案>>
针对以上新闻内容,大家展开了热烈的讨论:
【讨论交流】
(1)关于电石引起的燃烧,需要满足燃烧的三个条件分别为:①需要可燃物②可燃物与氧气接触③
(2)根据元素守恒思想对电石与水反应后生成的白色固体物质进行了三种猜想,猜想A:氧化钙;猜想B:氢氧化钙;猜想C:是碳酸钙,同学们经过分析将猜想排除,并设计了如下实验来验证该固体物质:
| 方法 | 现象 | 结论 |
| 往样品中滴加稀盐酸 | 猜想 | |
| 猜想B正确 |
查阅资料:
已知乙炔是一可燃性气体,由碳氢元素组成,一个乙炔分子中共有四个原子构成.
实验设计:
将一定量的乙炔气体与足量氧气混合在一密闭容器内将其引燃.生成的混合气体缓缓通过以下吸收装置.

交流讨论:
由于涉及了两套吸收装置,实验小组的两位同学对于上述实验装置A和装置B的选用发生了争执,你认为应该选择
实验测定:
经讨论后,他们选定了实验装置,进行实验. 记录数据于下表中
| 反应前质量/g | 反应后质量/g | |
| 装置① | 125.3 | 127.1 |
| 装置② | 78.2 | 87.0 |
Ⅱ.请写出电石与水反应的化学方程式
化学是一门以实验为基础的科学,通过实验可以学习科学探究的方法.现有一份由碳酸钠和氯化钠组成的固体样品,质量为m1g.小明设计了图中的装置,请你参与探究.
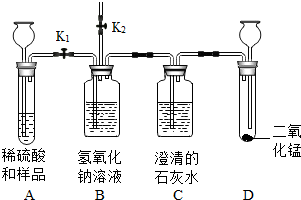
【实验目的】探究碳酸钠的化学性质并测定样品中碳酸钠的质量分数.
【查阅资料】碳酸钠能与稀硫酸发生反应,生成硫酸钠、二氧化碳和水.
【实验步骤】
①关闭止水夹K2,打开止水夹K1.向装有样品的A装置内加入适量的稀硫酸,充分反应后,B装置的质量增重m2g,C装置中的澄清石灰水不变浑浊.
②关闭止水夹K1,打开止水夹K2,使B装置与空气连通.向D装置内加入适量的过氧化氢溶液充分反应(确保溶液浸没长颈漏斗下端管口).请回答:
(1)实验前需检查装置的 .
(2)判断样品中含有碳酸钠的实验现象为 .
(3)样品中碳酸钠的质量分数的表达式为 .
(4)在整个反应过程中,B装置内发生反应的化学方程式为 .
【实验拓展】反应结束后,B装置溶液中溶质的组成有多种情况,其中的一种是只含有氢氧化钠,还有的情况是: .你怎样验证溶质只含有氢氧化钠的这种情况: .
查看习题详情和答案>>

【实验目的】探究碳酸钠的化学性质并测定样品中碳酸钠的质量分数.
【查阅资料】碳酸钠能与稀硫酸发生反应,生成硫酸钠、二氧化碳和水.
【实验步骤】
①关闭止水夹K2,打开止水夹K1.向装有样品的A装置内加入适量的稀硫酸,充分反应后,B装置的质量增重m2g,C装置中的澄清石灰水不变浑浊.
②关闭止水夹K1,打开止水夹K2,使B装置与空气连通.向D装置内加入适量的过氧化氢溶液充分反应(确保溶液浸没长颈漏斗下端管口).请回答:
(1)实验前需检查装置的
(2)判断样品中含有碳酸钠的实验现象为
(3)样品中碳酸钠的质量分数的表达式为
(4)在整个反应过程中,B装置内发生反应的化学方程式为
【实验拓展】反应结束后,B装置溶液中溶质的组成有多种情况,其中的一种是只含有氢氧化钠,还有的情况是:
 空气是多种气体组成的混合物,氧气约占21%,氮气约占78%.测定空气中氧气含量的基本思路是:取一定体积的混合气体
空气是多种气体组成的混合物,氧气约占21%,氮气约占78%.测定空气中氧气含量的基本思路是:取一定体积的混合气体方法一:除去氧气测氮气的体积
方法二:除去氮气测氧气的体积
根据所学知识,你认为应除去的气体是
氧气
氧气
,原因是氮气化学性质比较稳定(或化学性质不活泼,不易和其它物质发生反应)
氮气化学性质比较稳定(或化学性质不活泼,不易和其它物质发生反应)
.化学兴趣小组的同学查找资料知:白磷是一种易自燃的物质,其着火点为40℃,在空气中燃烧生成白色固体五氧化二磷.他们设计了如图所示实验:实验现象是
白磷燃烧产生大量白烟,放出热量
白磷燃烧产生大量白烟,放出热量
,化学方程式为4P+5O2
2P2O5
| ||
4P+5O2
2P2O5
.
| ||
等冷却到室温,他们发现气体减少了大约1.5个空格,所测结果比空气中氧气含量低了许多,其原因可能是
白磷量不足或装置气密性不好.(其他合理答案均可)
白磷量不足或装置气密性不好.(其他合理答案均可)
(只写一条)中考化学实验考查其中的一个内容是:用大理石和稀盐酸制取、收集CO2并检验,下列仪器组装成发生装置应选用
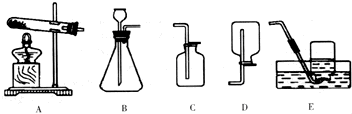
实验结束后同学们将试管中的“废液”倒入废液缸.几位同学对此产生了兴趣:
(1)天天看到大理石留在了漏斗中,液体流入了试剂瓶,此操作是利用了
(2)强强用
(3)月月将一颗生锈的铁钉放入少量废液中,开始看到铁锈消失,溶液变黄.化学方程式为
(4)艺艺想对废液先处理,然后回收氯化钙.她忽然想到,如果把检验CO2后集气瓶内变浑浊的“石灰水”与废液按一定比例混合就能达到预期效果.
①首先用实验确认集气瓶内变浑浊的“石灰水”的成分:
②如何确认集气瓶内变浑浊的“石灰水”与废液恰好完全反应呢?
她取少量集气瓶内变浑浊的“石灰水”于试管中,滴加几滴无色酚酞试液后变红,逐滴加入废液,看到
③从反应后的溶液中获取氯化钙晶体可采用
查看习题详情和答案>>
B
B
(填序号).收集装置只能选择C
C
(填序号),依据是二氧化碳的密度比空气的密度大,能溶于水,因此只能用向上排空气法收集
二氧化碳的密度比空气的密度大,能溶于水,因此只能用向上排空气法收集
.不改变收集和发生装置还可制取并收集氧气
氧气
气体,化学方程式为2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.
| ||

实验结束后同学们将试管中的“废液”倒入废液缸.几位同学对此产生了兴趣:
(1)天天看到大理石留在了漏斗中,液体流入了试剂瓶,此操作是利用了
过滤
过滤
法对混合物分离的.(2)强强用
PH试纸
PH试纸
测得试剂瓶中液体的PH为1,由此推断液体中一定含有溶于水的氯化钙、水和盐酸
盐酸
三种物质.(3)月月将一颗生锈的铁钉放入少量废液中,开始看到铁锈消失,溶液变黄.化学方程式为
Fe2O3+6HCl=2FeCl3+3H2O
Fe2O3+6HCl=2FeCl3+3H2O
,一段时间后还能看到有气泡冒出
有气泡冒出
.(4)艺艺想对废液先处理,然后回收氯化钙.她忽然想到,如果把检验CO2后集气瓶内变浑浊的“石灰水”与废液按一定比例混合就能达到预期效果.
①首先用实验确认集气瓶内变浑浊的“石灰水”的成分:
| 操 作 | 现 象 | 结 论 |
先向集气瓶内变浑浊的“石灰水”中,滴加无色酚酞试液, 先向集气瓶内变浑浊的“石灰水”中,滴加无色酚酞试液, |
发现无色变红色,仍浑浊 发现无色变红色,仍浑浊 |
(1)仍有没反应的氢氧化钙 (2)还含有生成的碳酸钙 |
她取少量集气瓶内变浑浊的“石灰水”于试管中,滴加几滴无色酚酞试液后变红,逐滴加入废液,看到
无气泡生成,溶液变为无色
无气泡生成,溶液变为无色
现象时说明恰好反应,其中氢氧化钙与废液发生反应的方程式Ca(OH)2+2HCl=CaCl2+2H2O
Ca(OH)2+2HCl=CaCl2+2H2O
.③从反应后的溶液中获取氯化钙晶体可采用
蒸发结晶的
蒸发结晶的
方法.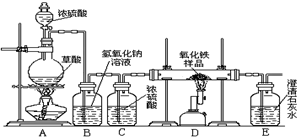 化学小组的同学在研究性学习课上展示了一套如图所示的实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不参加反应,且杂质中不含铁).查阅资料:草酸在浓硫酸存在时加热发生如下反应:
化学小组的同学在研究性学习课上展示了一套如图所示的实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不参加反应,且杂质中不含铁).查阅资料:草酸在浓硫酸存在时加热发生如下反应:H2C2O4
| ||
| △ |
通过讨论,同学们对这套装置有了多种认识.
(1)第一小组同学说:从实验安全和实验操作程序看,首先要检查装置的气密性,实验开始先加热
A
A
(填A或D)处,实验结束时,应先
先
(填先或后)停止D处的加热;从环保的角度讲,在E装置后还应对尾气进行处理,要处理尾气的原因是.(2)第二小组的同学说:用该实验装置可以检验一氧化碳与氧化铁反应的产物,其中B装置的作用
吸收A中反应生成的二氧化碳
吸收A中反应生成的二氧化碳
;E装置的作用检验并吸收D中反应生成的二氧化碳
检验并吸收D中反应生成的二氧化碳
;CO与Fe2O3反应的化学方程式为3CO+Fe2O3
3CO2+2Fe
| ||
3CO+Fe2O3
3CO2+2Fe
,该反应
| ||
否
否
(填是、否)置换反应.你证明D中有铁产生的2个方法是:;.
(3)第三小组的同学说:利用这套装置还可以测定氧化铁样品中氧化铁的质量分数.他们的测定方
法是:称量氧化铁样品的质量10.0g,样品与玻璃管的总质量为60.0g,完全反应并冷却后再称量玻璃管与剩余固体的总质量为57.6g.则实验测得氧化铁样品中氧化铁的质量分数为
80%
80%
%.(4)第四小组同学说:利用这套装置还有另外测定样品中氧化铁的质量分数的方法:先称量氧化铁样品的质量,再分别称量E装置在反应前后的总质量,即可计算求得样品中氧化铁的质量分数.但按此方法实际实验测定结果却偏大,分析造成偏大的原因可能是
B装置吸收CO2不充分(或E吸收了装置里空气中的CO2或者外界CO2进入的干扰)
B装置吸收CO2不充分(或E吸收了装置里空气中的CO2或者外界CO2进入的干扰)
.(5)反思:要验证草酸分解有CO2生成,可以在装置A与B之间增加一个形如B内盛
澄清石灰水
澄清石灰水
的洗气瓶;如果没有装置C,则测得氧化铁的质量分数将不变
不变
(填偏大、偏小、不变).