题目内容
化学兴趣小组的同学在报纸上看到这样一则新闻报道:《杭州一大货车载电石狂奔燃烧 火龙震撼 仿佛好莱坞大片》某日凌晨2点50分左右,一辆满载20吨电石的挂车,在杭州滨江区江南大道信诚路口燃起熊熊大火,黑烟如蘑菇升空,不时发出“嘭嘭”爆炸声.让电石起火的是雨水,电石遇水燃烧爆炸.而雨一直下,燃烧现场一直无法处理.从火灾发生到初步控制住,一共用掉4吨干粉.电石,学名碳化钙(CaC2),是由生石灰和焦炭在电炉中加热到2000℃生成.电石的化学性质非常活泼,遇水就会发生剧烈化学反应,生成一种可燃气体乙炔和一白色固体物质,并放出大量的热.所以,水不能灭这个火,水在其中的角色是助燃!电石起火在正常情况下,可以用磷酸盐干粉、干黄沙和水泥进行覆盖、隔离扑灭.但因为现场雨下得很大,这三种物质无法完全发挥作用,只能就近让它烧光.针对以上新闻内容,大家展开了热烈的讨论:
【讨论交流】
(1)关于电石引起的燃烧,需要满足燃烧的三个条件分别为:①需要可燃物②可燃物与氧气接触③
(2)根据元素守恒思想对电石与水反应后生成的白色固体物质进行了三种猜想,猜想A:氧化钙;猜想B:氢氧化钙;猜想C:是碳酸钙,同学们经过分析将猜想排除,并设计了如下实验来验证该固体物质:
| 方法 | 现象 | 结论 |
| 往样品中滴加稀盐酸 | 猜想 | |
| 猜想B正确 |
查阅资料:
已知乙炔是一可燃性气体,由碳氢元素组成,一个乙炔分子中共有四个原子构成.
实验设计:
将一定量的乙炔气体与足量氧气混合在一密闭容器内将其引燃.生成的混合气体缓缓通过以下吸收装置.
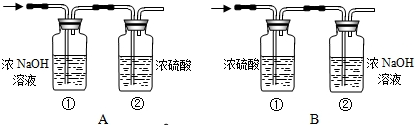
交流讨论:
由于涉及了两套吸收装置,实验小组的两位同学对于上述实验装置A和装置B的选用发生了争执,你认为应该选择
实验测定:
经讨论后,他们选定了实验装置,进行实验. 记录数据于下表中
| 反应前质量/g | 反应后质量/g | |
| 装置① | 125.3 | 127.1 |
| 装置② | 78.2 | 87.0 |
Ⅱ.请写出电石与水反应的化学方程式
分析:(1)根据燃烧的三个条件可知,从画线部分的信息(磷酸盐干粉、干黄沙和水泥进行覆盖、隔离扑灭)可知,灭火原理是隔绝可燃物和外界的接触.
(2)根据物质的性质即可判断,比如碱遇酚酞变红.
(3)根据氢氧化钠吸收二氧化碳和浓硫酸吸收水可知.
(2)根据物质的性质即可判断,比如碱遇酚酞变红.
(3)根据氢氧化钠吸收二氧化碳和浓硫酸吸收水可知.
解答:解;
(1)③温度达到着火点;根据题干信息(用磷酸盐干粉、干黄沙和水泥进行覆盖、隔离扑灭)可知,这样做的目的就是把可燃物和外界隔离,故答案为:原理为隔绝可燃物与氧气(及水)的接触.
(2)根据生活常识可知,猜想A:氧化钙是不可能的,因为氧化钙和水可以迅速反应生成氢氧化钙;根据题目信息可知猜想C:碳酸钙也错误,碳酸钙与盐酸反应的现象是有气体生成;氢氧化钙是碱性的,与酚酞颜色变红.故答案为:
(3)如果选A,混合气体通过氢氧化钠,氢氧化钠增重的质量就是二氧化碳;但是也会带一部分水进入浓硫酸,所以浓硫酸增重的质量就不再全部是燃烧的产物水.故答案为:B
水的质量:127.1-125.3═1.8;∴氢元素的质量:1.8×
═0.2
二氧化碳的质量:87-78.2═8.8;∴碳元素的质量:8.8×
═2.4
氢元素的质量分数是
×100%═
×100%
设化学式中氢原子个数是X,则碳原子个数是4-X;
则氢元素的质量分数:
×100%=
×100%;解得:X=2
故答案为:乙炔的化学式 C2H2
Ⅱ.由题目信息知反应物和生成物可知,电石与水反应的化学方程式:CaC2+2H2O═Ca(OH)2+C2H2↑
(1)③温度达到着火点;根据题干信息(用磷酸盐干粉、干黄沙和水泥进行覆盖、隔离扑灭)可知,这样做的目的就是把可燃物和外界隔离,故答案为:原理为隔绝可燃物与氧气(及水)的接触.
(2)根据生活常识可知,猜想A:氧化钙是不可能的,因为氧化钙和水可以迅速反应生成氢氧化钙;根据题目信息可知猜想C:碳酸钙也错误,碳酸钙与盐酸反应的现象是有气体生成;氢氧化钙是碱性的,与酚酞颜色变红.故答案为:
| 方法 | 现象 | 结论 |
| 往样品中滴加稀盐酸 | 无气泡产生 | 猜想C不正确 |
| 往样品中加入酚酞 | 溶液颜色变红 | 猜想B正确 |
水的质量:127.1-125.3═1.8;∴氢元素的质量:1.8×
| 2 |
| 18 |
二氧化碳的质量:87-78.2═8.8;∴碳元素的质量:8.8×
| 12 |
| 44 |
氢元素的质量分数是
| 0.2 |
| 0.2+2.4 |
| 1 |
| 13 |
设化学式中氢原子个数是X,则碳原子个数是4-X;
则氢元素的质量分数:
| X |
| X+48-12X |
| 1 |
| 13 |
故答案为:乙炔的化学式 C2H2
Ⅱ.由题目信息知反应物和生成物可知,电石与水反应的化学方程式:CaC2+2H2O═Ca(OH)2+C2H2↑
点评:培养学生通过题目搜索做题信息的能力,学会计算化学式的方法.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
 20、某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如下图所示的装置进行探究.
20、某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如下图所示的装置进行探究.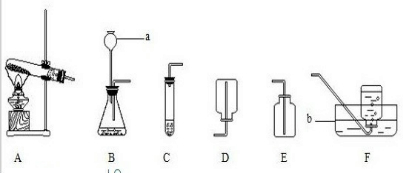
 (2012?太原)某化学兴趣小组的同学在探究Mg、Cu、Fe三种金属的有关性质时进行了如下实验:
(2012?太原)某化学兴趣小组的同学在探究Mg、Cu、Fe三种金属的有关性质时进行了如下实验: