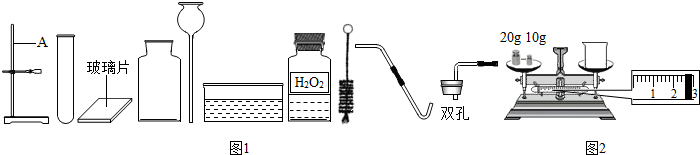
题目内容
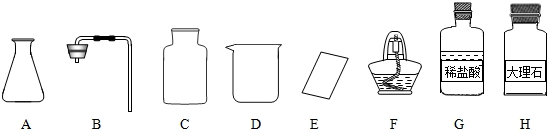
中考化学实验考查其中的一个内容是:用大理石和稀盐酸制取、收集CO2并检验,下列仪器组装成发生装置应选用
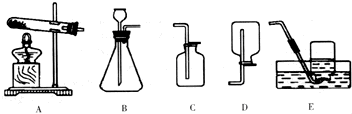
实验结束后同学们将试管中的“废液”倒入废液缸.几位同学对此产生了兴趣:
(1)天天看到大理石留在了漏斗中,液体流入了试剂瓶,此操作是利用了
(2)强强用
(3)月月将一颗生锈的铁钉放入少量废液中,开始看到铁锈消失,溶液变黄.化学方程式为
(4)艺艺想对废液先处理,然后回收氯化钙.她忽然想到,如果把检验CO2后集气瓶内变浑浊的“石灰水”与废液按一定比例混合就能达到预期效果.
①首先用实验确认集气瓶内变浑浊的“石灰水”的成分:
②如何确认集气瓶内变浑浊的“石灰水”与废液恰好完全反应呢?
她取少量集气瓶内变浑浊的“石灰水”于试管中,滴加几滴无色酚酞试液后变红,逐滴加入废液,看到
③从反应后的溶液中获取氯化钙晶体可采用
B
B
(填序号).收集装置只能选择C
C
(填序号),依据是二氧化碳的密度比空气的密度大,能溶于水,因此只能用向上排空气法收集
二氧化碳的密度比空气的密度大,能溶于水,因此只能用向上排空气法收集
.不改变收集和发生装置还可制取并收集氧气
氧气
气体,化学方程式为2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.
| ||

实验结束后同学们将试管中的“废液”倒入废液缸.几位同学对此产生了兴趣:
(1)天天看到大理石留在了漏斗中,液体流入了试剂瓶,此操作是利用了
过滤
过滤
法对混合物分离的.(2)强强用
PH试纸
PH试纸
测得试剂瓶中液体的PH为1,由此推断液体中一定含有溶于水的氯化钙、水和盐酸
盐酸
三种物质.(3)月月将一颗生锈的铁钉放入少量废液中,开始看到铁锈消失,溶液变黄.化学方程式为
Fe2O3+6HCl=2FeCl3+3H2O
Fe2O3+6HCl=2FeCl3+3H2O
,一段时间后还能看到有气泡冒出
有气泡冒出
.(4)艺艺想对废液先处理,然后回收氯化钙.她忽然想到,如果把检验CO2后集气瓶内变浑浊的“石灰水”与废液按一定比例混合就能达到预期效果.
①首先用实验确认集气瓶内变浑浊的“石灰水”的成分:
| 操 作 | 现 象 | 结 论 |
先向集气瓶内变浑浊的“石灰水”中,滴加无色酚酞试液, 先向集气瓶内变浑浊的“石灰水”中,滴加无色酚酞试液, |
发现无色变红色,仍浑浊 发现无色变红色,仍浑浊 |
(1)仍有没反应的氢氧化钙 (2)还含有生成的碳酸钙 |
她取少量集气瓶内变浑浊的“石灰水”于试管中,滴加几滴无色酚酞试液后变红,逐滴加入废液,看到
无气泡生成,溶液变为无色
无气泡生成,溶液变为无色
现象时说明恰好反应,其中氢氧化钙与废液发生反应的方程式Ca(OH)2+2HCl=CaCl2+2H2O
Ca(OH)2+2HCl=CaCl2+2H2O
.③从反应后的溶液中获取氯化钙晶体可采用
蒸发结晶的
蒸发结晶的
方法.分析:制取装置包括加热和不需加热两种,实验室是用石灰石和稀盐酸在常温下来制取二氧化碳的,因此不需要加热;二氧化碳的密度比空气的密度大,能溶于水,因此只能用向上排空气法收集.如果用过氧化氢和二氧化锰制氧气,就不需要加热;如果用高锰酸钾或氯酸钾就需要加热.氧气不易溶于水,密度比空气的密度大,因此可以用排水法和向上排空气法收集.固体和液体分开就需要过滤,可溶性固体与水分开,可以用蒸发的方法;用PH试纸测定溶液的PH值;生锈的铁钉与盐酸能发生化学反应;酸和碱会发生中和反应;用酸碱指示剂可以检验溶液的酸碱性.书写化学方程式时,要注意配平.
解答:解:Ⅰ实验室是用石灰石和稀盐酸在常温下来制取二氧化碳的,因此不需要加热;二氧化碳的密度比空气的密度大,能溶于水,因此只能用向上排空气法收集.如果用过氧化氢和二氧化锰制氧气,就不需要加热;故答案为:B;C;二氧化碳的密度比空气的密度大,能溶于水,因此只能用向上排空气法收集;氧气;2H2O2
2H2O+O2↑
Ⅱ(1)固体和液体分开就需要过滤,故答案为:过滤;
(2)用PH试纸测定溶液的PH值,测得试剂瓶中液体的PH为1,因此滤液中有盐酸.故答案为:PH试纸;盐酸
(3)铁锈的主要成分是氧化铁,氧化铁和盐酸反应生成氯化铁和水,配平即可;铁锈除去后,铁与盐酸反应有气泡冒出.故答案为:Fe2O3+6HCl=2FeCl3+3H2O;有气泡冒出
(4)用实验确认集气瓶内变浑浊的“石灰水”成分的实验方法是:先向集气瓶内变浑浊的“石灰水”中,滴加无色酚酞试液;发现无色变红色,仍浑浊;要确认集气瓶内变浑浊的“石灰水”与废液恰好完全反应,只要观察到:无气泡生成,溶液变为无色即可;氢氧化钙和盐酸反应生成氯化钙和水,配平即可;从反应后的溶液中获取氯化钙晶体可采用蒸发结晶的方法.故答案为:①先向集气瓶内变浑浊的“石灰水”中,滴加无色酚酞试液;发现无色变红色,仍浑浊;②无气泡生成,溶液变为无色;Ca(OH)2+2HCl=CaCl2+2H2O;③蒸发结晶的
| ||
Ⅱ(1)固体和液体分开就需要过滤,故答案为:过滤;
(2)用PH试纸测定溶液的PH值,测得试剂瓶中液体的PH为1,因此滤液中有盐酸.故答案为:PH试纸;盐酸
(3)铁锈的主要成分是氧化铁,氧化铁和盐酸反应生成氯化铁和水,配平即可;铁锈除去后,铁与盐酸反应有气泡冒出.故答案为:Fe2O3+6HCl=2FeCl3+3H2O;有气泡冒出
(4)用实验确认集气瓶内变浑浊的“石灰水”成分的实验方法是:先向集气瓶内变浑浊的“石灰水”中,滴加无色酚酞试液;发现无色变红色,仍浑浊;要确认集气瓶内变浑浊的“石灰水”与废液恰好完全反应,只要观察到:无气泡生成,溶液变为无色即可;氢氧化钙和盐酸反应生成氯化钙和水,配平即可;从反应后的溶液中获取氯化钙晶体可采用蒸发结晶的方法.故答案为:①先向集气瓶内变浑浊的“石灰水”中,滴加无色酚酞试液;发现无色变红色,仍浑浊;②无气泡生成,溶液变为无色;Ca(OH)2+2HCl=CaCl2+2H2O;③蒸发结晶的
点评:本考点主要考查气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和实验方案的设计,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.设计实验方案时,要注意实验操作、现象和结论的叙述,本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
中考化学实验考查其中的一个内容是:用大理石和稀盐酸制取、收集CO2并检验,下列仪器组装成发生装置应选用________(填序号).收集装置只能选择________(填序号),依据是________.不改变收集和发生装置还可制取并收集________气体,化学方程式为________.

实验结束后同学们将试管中的“废液”倒入废液缸.几位同学对此产生了兴趣:
(1)天天看到大理石留在了漏斗中,液体流入了试剂瓶,此操作是利用了________法对混合物分离的.
(2)强强用________测得试剂瓶中液体的PH为1,由此推断液体中一定含有溶于水的氯化钙、水和________三种物质.
(3)月月将一颗生锈的铁钉放入少量废液中,开始看到铁锈消失,溶液变黄.化学方程式为________,一段时间后还能看到________.
(4)艺艺想对废液先处理,然后回收氯化钙.她忽然想到,如果把检验CO2后集气瓶内变浑浊的“石灰水”与废液按一定比例混合就能达到预期效果.
①首先用实验确认集气瓶内变浑浊的“石灰水”的成分:
| 操 作 | 现 象 | 结 论 |
| ________ | ________ | (1)仍有没反应的氢氧化钙 (2)还含有生成的碳酸钙 |
她取少量集气瓶内变浑浊的“石灰水”于试管中,滴加几滴无色酚酞试液后变红,逐滴加入废液,看到________现象时说明恰好反应,其中氢氧化钙与废液发生反应的方程式________.
③从反应后的溶液中获取氯化钙晶体可采用________方法.