摘要:7.X.Y.Z.L.M五种元素的原子序数依次增大.X.Y.Z.L是组成蛋白质的基础元素.M是地壳中含量最高的金属元素. 回答下列问题: ⑴ L的元素符号为 ,M在元素周期表中的位置为 ,五种元素的原子半径从大到小的顺序是 . ⑵ Z.X两元素按原子数目比l∶3和2∶4构成分子A和B.A的电子式为 .B的结构式为 . ⑶ 硒(se)是人体必需的微量元素.与L同一主族.Se原子比L原子多两个电子层.则Se的原子序数为 .其最高价氧化物对应的水化物化学式为 .该族2 ~ 5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下.表示生成1 mol硒化氢反应热的是 . a.+99.7 mol·L-1 b.+29.7 mol·L-1 c.-20.6 mol·L-1 d.-241.8 kJ·mol-1 ⑷ 用M单质作阳极.石墨作阴极.NaHCO3溶液作电解液进行电解.生成难溶物R.R受热分解生成化合物Q .写出阳极生成R的电极反应式: ,由R生成Q的化学方程式: . 解析:(1)X.Y.Z.L是组成蛋白质的四种元素且原子序数依次增大.故分别为:H.C.N.O元素,M是地壳中含量最高的元素.为Al.其在周期表的位置为第3周第ⅢA族,再根据五种元素在周期表的位置.可知半径由大到小的顺序是:Al>C>N>O>H. (2) N和H 1:3构成的分子为NH3.电子式为,2:4构成的分子为N2H4.其结构式为. (3)Se比O多两个电子层.共4个电子层.1→4电子层上的电子数分别为:2.8 .18.6.故其原子序数为34,其最高价氧化物对应的水化物的化学式类似H2SO4.为H2SeO4. 非金属性越强.与氢气反应放出的热量越多.故2→5周期放出的热量依次是:d.c.b.a.则第四周期的Se对应的是b. (4)Al作阳极失去电子生成Al3+.Al3++3HCO3-==Al(OH)3+3CO2.2Al(OH)3Al2O3+3H2O. 答案: (1)O 第三周第ⅢA族 Al>C>N>O>H (2) (3) 34 H2SeO4 b (4) Al-3e-Al3+ Al3++3HCO3-==Al(OH)3+3CO2 2Al(OH)3Al2O3+3H2O. 命题立意:本题以元素的推断为背景.综合考查了元素符号的书写.元素位置的判断和原子半径大小的比较,考查了电子式.结构式的书写.元素周期律.和电极反应式.化学方程式的书写.是典型的学科内综合试题.
网址:http://m.1010jiajiao.com/timu3_id_88441[举报]
X、Y、Z、L、M五种元索的原子序数依次增大。X、Y、Z、L,是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。 回答下列问题:
(1)L的元素符号为______;M在元素周期表中的位置为____;五种元素的原子半径从大到小的顺序是_________(用元素符号表示)。
(2)Z、X两元素按原子数目比1:3和2:4构成分子A和B,A的电子式为______, B的结构式为_____。
(3)硒( Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子 层,则Se的原子序数为____,其最高价氧化物对应的水化物化学式为____ 该族2-5周期元素单质分别与H2反应生成1mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是____(填字母代号)。
a.+99.7 kJ·mol-1
b.+29.7 kJ·mol-1
c.- 20.6 kJ·mol-1
d.-241.8 kJ·mol-1
(4)用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R,R受热分解生成化合物Q。写出阳极生成R的电极反应式:________; 由R生成Q的化学方程式:__________
查看习题详情和答案>>
(1)L的元素符号为______;M在元素周期表中的位置为____;五种元素的原子半径从大到小的顺序是_________(用元素符号表示)。
(2)Z、X两元素按原子数目比1:3和2:4构成分子A和B,A的电子式为______, B的结构式为_____。
(3)硒( Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子 层,则Se的原子序数为____,其最高价氧化物对应的水化物化学式为____ 该族2-5周期元素单质分别与H2反应生成1mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是____(填字母代号)。
a.+99.7 kJ·mol-1
b.+29.7 kJ·mol-1
c.- 20.6 kJ·mol-1
d.-241.8 kJ·mol-1
(4)用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R,R受热分解生成化合物Q。写出阳极生成R的电极反应式:________; 由R生成Q的化学方程式:__________
 (2013?江西模拟)(一)X、Y、Z、L、M五种元素的原子序数依次增大,X的阴离子与Y的内层电子数相等,Y原子的最外层电子数是次外层电子数的两倍,Z、L是空气中含量最多的二种元素,M是地壳中含量最高的金属元素.回答下列问题:
(2013?江西模拟)(一)X、Y、Z、L、M五种元素的原子序数依次增大,X的阴离子与Y的内层电子数相等,Y原子的最外层电子数是次外层电子数的两倍,Z、L是空气中含量最多的二种元素,M是地壳中含量最高的金属元素.回答下列问题:(1)L的元素名称为
氧
氧
;五种元素的原子半径从小到大的顺序是(用元素符号表示)H<O<N<C<Al
H<O<N<C<Al
.(2)Z、X两元素按原子数目比1:3和2:4构成分子A和B,用电子式表示A的形成过程
3H?+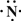 →
→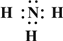
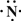 →
→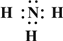
3H?+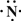 →
→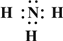
,B的结构式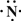 →
→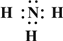
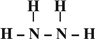
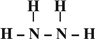
(3)硒(Se)是人体必须的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为
34
34
,其最高价氧化物对应的水化物化学式为H2SeO4
H2SeO4
.该族2~5周期元素单质分别与H2反应生成1mol气态氢化物的反应热如下,表示生成1mol硒化氢反应热的是b
b
(填字母代号).a.+99.7kJ?mol-1 b.+29.7kJ?mol-1c.-20.6kJ?mol-1 d.-241.8kJ?mol-1(4)一定条件下,M与TiO2、C(石墨)反应只生成乙和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分.已知.该反应生成lmol乙时放出536kJ热量,其热化学方程式为
4Al(s)+3TiO2(s)+3C(s,石墨)=2Al2O3(s)+3TiC(s)△M=-1072g/mol
4Al(s)+3TiO2(s)+3C(s,石墨)=2Al2O3(s)+3TiC(s)△M=-1072g/mol
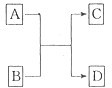
.(二)已知A、B、C、D分别是由短周期元素原子组成的四种微粒,它们之间有如图所示的转变关系,且A是种含有18电子的微粒,C是一种含有10电子的微粒.请完成下列各题:
(1)若A、D分别是两种气态单质分子,写出A与B反应的化学方程式
2F2+2H2O=4HF+O2
2F2+2H2O=4HF+O2
.(2)若B、D属同主族的单质分子,写出C的化学式
H2O
H2O
.(3)若B是一种含四核l8电子的分子,如果D是一种气态单质分子,B的结构简式为
H-O-O-H
H-O-O-H
.(4)若A、B均是含2个原子核的微粒,其中B中含有10个电子,D中含有18个电子,则A、B之间发生的离子反应方程式为
HS-+OH-=S2-+H2O
HS-+OH-=S2-+H2O
.(5)若D是一种含有22电子的分子,则符合如图关系的A的物质有
CH3OH、CH3-CH3
CH3OH、CH3-CH3
(写出物质的化学式,如果是有机物则写相应的结构简式).X、Y、Z、L、M五种元素的原子序数依次增大.X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素.请回答下列问题:
(1)M在元素周期表中的位置为
(2)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为
a.+99.7kJ?mol-1 b.+29.7kJ?mol-1
c.-20.6 1kJ?mol-1 d.-241.8kJ?mol-1
(3)用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R,R受热可分解.写出生成R的反应式:
查看习题详情和答案>>
(1)M在元素周期表中的位置为
第三周期第ⅢA族
第三周期第ⅢA族
;五种元素的原子半径从大到小的顺序是Al>C>N>O>H
Al>C>N>O>H
(用元素符号表示).(2)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为
34
34
,其最高价氧化物对应的水化物化学式为H2SeO4
H2SeO4
.该族2~5周期元素单质分别与H2反应生成lmol气态氢化物的焓变如下,表示生成1mol硒化氢焓变的是b
b
(填字母代号).a.+99.7kJ?mol-1 b.+29.7kJ?mol-1
c.-20.6 1kJ?mol-1 d.-241.8kJ?mol-1
(3)用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R,R受热可分解.写出生成R的反应式:
Al-3e-=Al3+、Al3++3HCO3-=Al(OH)3↓+3CO2↑
Al-3e-=Al3+、Al3++3HCO3-=Al(OH)3↓+3CO2↑
.X、Y、Z、L、M五种元素的原子序数依次增大.X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素.
回答下列问题:
(1)L的元素符号为
(2)Z、X两元素按原子数目比1:3和2:4构成分子A和B,已知:气态的B在L常见的单质中燃烧生成Z单质和水蒸气时放出534KJ能量,试写出该反应热化学方程式
(3)硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的最高价氧化物对应的水化物化学式为
a.+99.7mol?L-1 b.+29.7mol?L-1
c.-20.6mol?L-1 d.-241.8kJ?mol-1
(4)用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R和某气体,已知R受热分解生成化合物Q.写出阳极生成R的电极反应式:
查看习题详情和答案>>
回答下列问题:
(1)L的元素符号为
O
O
;M在元素周期表中的位置为第三周期第ⅢA族
第三周期第ⅢA族
;五种元素的原子半径从大到小的顺序是Al>C>N>O>H
Al>C>N>O>H
(用元素符号表示).(2)Z、X两元素按原子数目比1:3和2:4构成分子A和B,已知:气态的B在L常见的单质中燃烧生成Z单质和水蒸气时放出534KJ能量,试写出该反应热化学方程式
N2H4(g)+O2(g)═N2(g)+2H2O(g)?△H=-534kJ/mol
N2H4(g)+O2(g)═N2(g)+2H2O(g)?△H=-534kJ/mol
(3)硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的最高价氧化物对应的水化物化学式为
H2SeO4
H2SeO4
,该族2~5周期元素单质分别与H2反应生成1 mol气态氢化物的反应热如下,表示生成1mol硒化氢反应热的是b
b
(填字母代号).a.+99.7mol?L-1 b.+29.7mol?L-1
c.-20.6mol?L-1 d.-241.8kJ?mol-1
(4)用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R和某气体,已知R受热分解生成化合物Q.写出阳极生成R的电极反应式:
Al-3e-=Al3+、Al3++3HCO3-=Al(OH)3↓+CO2↑
Al-3e-=Al3+、Al3++3HCO3-=Al(OH)3↓+CO2↑
;由R生成Q的化学方程式:2Al(OH)3
Al2O3+2H2O
| ||
2Al(OH)3
Al2O3+2H2O
.
| ||
X、Y、Z、L、M五种元素的原子序数依次增大.X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素.回答下列问题:
(1)五种元素的原子半径从大到小的顺序是 (用元素符号表示).
(2)X与Z形成的3:1的化合物A,它与Z的最高价氧化物对应的水化物B反应的化学方程式 ,该水溶液显 性,用离子方程式解释原因 .
(3)硒是人体必需的微量元素,与L同一主族,其最高价氧化物对应的水化物化学式为 .该元素固体单质与H2反应生成0.5mol气态氢化物时吸收了14.87kJ的热量,请写出1mol该物质与氢气化合的热化学方程式: .
(4)用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R,R受热分解生成化合物Q.写出阳极生成R的电极反应式: ;由R生成Q的化学方程式: .
查看习题详情和答案>>
(1)五种元素的原子半径从大到小的顺序是
(2)X与Z形成的3:1的化合物A,它与Z的最高价氧化物对应的水化物B反应的化学方程式
(3)硒是人体必需的微量元素,与L同一主族,其最高价氧化物对应的水化物化学式为
(4)用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R,R受热分解生成化合物Q.写出阳极生成R的电极反应式: