摘要:12.由Fe2O3.Fe.CuO.C.Al中的几种物质组成的混合粉末.取样品进行下列实验: (1)取少量溶液X.加入过量的NaOH溶液.有沉淀生成.取上层清液.通入CO2.无明显变化.说明样品中不含有的物质是 . (2)Z为一种或两种气体: ①若Z只为一种气体.试剂a为饱和NaHCO3溶液.则反应Ⅰ中能同时生成两种气体的化学方程式是 . ②若Z为两种气体的混合物.试剂a为适量水.则Z中两种气体的化学式是 . (3)向Y中通入过量氯气.并不断搅拌.充分反应后.溶液中的阳离子是 . (4)取Y中的溶液.调pH约为7.加入淀粉KI溶液和H2O2.溶液呈蓝色并有红褐色沉淀生成.当消耗2 mol I-时.共转移3 mol电子.该反应的离子方程式是 . (5)另取原样品.加入足量稀硫酸充分反应.若溶液中一定不会产生Y中的红色固体.则原样品中所有可能存在的物质组合是(各组合中的物质用化学式表示) . [解析] 首先要注意框图中量的描述“过量 .然后做大致的推断.再根据具体的设问提供的信息具体分析. 大致猜想:“浓酸 和“两种气体 可推知“浓酸 可能为浓硫酸或浓硝酸.金属元素只有Fe.Cu.则溶液X可能为Fe2(SO4)3.CuSO4.Al2(SO4)3或Fe(NO3)3.Cu(NO3)2.Al(NO3)3.两种气体可能为SO2.CO2或NO2.CO2.不可能为NO2.NO.因浓酸过量.Y中溶液定有Fe2+.还可能有Al3+.Y中固体定有Fe.Cu. (1)若有Al.则应有2AlO+CO2+3H2O===2Al(OH)3↓+CO.或AlO+CO2+2H2O===Al(OH)3↓+HCO.有白色沉淀产生.“无明显变化 说明原混合物中无Al. (2)①“若Z只为一种气体.试剂a为饱和NaHCO3溶液 .则Z为CO2.两种气体中一种与NaHCO3溶液反应生成CO2.应为SO2:SO2+2NaHCO3===Na2SO3+2CO2+H2O.则浓酸为浓硫酸. ②若Z为两种气体的混合物.a为适量水.则其中一种为NO2:3NO2+H2O===2HNO3+NO.气体Z为NO与CO2的混合气体.则浓酸为浓硝酸. (3)Y中溶液中有大量的Fe2+.少量H+.固体为Fe.Cu.通入过量Cl2.并不断搅拌.则发生的反应有:Cl2+2Fe2+===2Fe3++2Cl-.Cl2+H2O===H++Cl-+HClO,2H++Fe===Fe2++H2↑.HClO+H++Cu===Cu2++Cl-+H2O,2Fe3++Cu===2Fe2++Cu2+.所以溶液中的阳离子有Fe3+.Cu2+.H+. (4)当消耗2 mol I-时.共转移3 mol电子.且有红褐色沉淀[Fe(OH)3]生成.则I-与Fe2+共同还原H2O2:4I-+2Fe2++3H2O2===2I2+2Fe(OH)3↓.(这是一个新动向.氧化剂或还原剂不止一种的氧化还原反应离子方程式的书写!) (5)通过前面的分析已知原样品中一定有CuO和C.一定无Al.Fe2O3.Fe是否存在不能确定.“另取原样品.加入足量稀硫酸充分反应.若溶液中一定不会产生Cu .则一定不会发生Fe+Cu2+===Fe2++Cu.则原样品中无Fe.可能的组合有:CuO.C,CuO.C.Fe2O3. [答案] (1)Al (2)①C+2H2SO4(浓)CO2↑+2SO2↑+2H2O ②NO.CO2 (3)Cu2+.Fe3+.H+ (4)2Fe2++3H2O2+4I-===2Fe(OH)3↓+2I2 (5)CuO.C CuO.C.Fe2O3
网址:http://m.1010jiajiao.com/timu3_id_88113[举报]
(2008?北京)由Fe2O3、Fe、CuO、C、Al中的几种物质组成的混合粉末,取样品进行下列实验(部分产物略去)
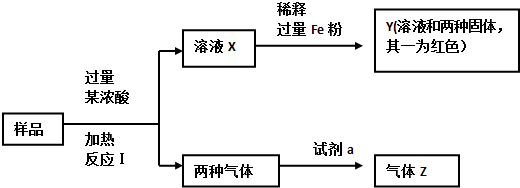
(1)取少量溶液X,加入过量的NaOH溶液,有沉淀生成.取上层清液,通入CO2,无明显变化,说明样品中不含有的物质是(填写化学式)
(2)Z为一种或两种气体:
①若Z只为一种气体,试剂a为饱和NaHCO3溶液,则反应I中能同时生成两种气体的化学方程式是
②若Z为两种气体的混合物,试剂a为适量水,则Z中两种气体的化学式是
(3)向Y中通入过量氯气,并不断搅拌,充分反应后,溶液中的阳离子是(填写离子符号)
(4)取Y中的溶液,调pH约为7,加入淀粉KI溶液和H2O2,溶液呈蓝色并有红褐色沉淀生成.当消耗2mol I-时,共转移3mol电子,该反应的离子方程式是
(5)另取原样品,加入足量稀硫酸充分反应.若溶液中一定不会产生Y中的红色固体,则原样品中所有可能存在的物质组合是(各组合中的物质用化学式表示)
查看习题详情和答案>>

(1)取少量溶液X,加入过量的NaOH溶液,有沉淀生成.取上层清液,通入CO2,无明显变化,说明样品中不含有的物质是(填写化学式)
Al
Al
.(2)Z为一种或两种气体:
①若Z只为一种气体,试剂a为饱和NaHCO3溶液,则反应I中能同时生成两种气体的化学方程式是
C+2H2SO4(浓) CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
 CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2OC+2H2SO4(浓) CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
. CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O②若Z为两种气体的混合物,试剂a为适量水,则Z中两种气体的化学式是
NO、CO2
NO、CO2
.(3)向Y中通入过量氯气,并不断搅拌,充分反应后,溶液中的阳离子是(填写离子符号)
Cu2+、Fe3+、H+
Cu2+、Fe3+、H+
.(4)取Y中的溶液,调pH约为7,加入淀粉KI溶液和H2O2,溶液呈蓝色并有红褐色沉淀生成.当消耗2mol I-时,共转移3mol电子,该反应的离子方程式是
2Fe2++3H2O2+4I-=2Fe(OH)3↓+2I2
2Fe2++3H2O2+4I-=2Fe(OH)3↓+2I2
.(5)另取原样品,加入足量稀硫酸充分反应.若溶液中一定不会产生Y中的红色固体,则原样品中所有可能存在的物质组合是(各组合中的物质用化学式表示)
CuO、C;CuO、C、Fe2O3
CuO、C;CuO、C、Fe2O3
.( I)由Zn、Fe、Cu、Ag四种金属按下表中装置进行实验,根据实验现象填表:
( II)碘是人体必须的元素之一,海洋植物如海带、海藻中含有丰富的以碘离子形式存在的碘元素.海带中含有丰富的碘.为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
请填写下列空白:
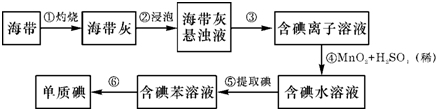
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器及用品是
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.玻璃棒 G.石棉网
(2)步骤③的实验操作名称是
(3)步骤④也可以用
(4)步骤⑤中,除选择用苯来提取碘,还可选择的试剂是
A.酒精 B.醋酸 C.四氯化碳 D.甘油 E.己烷 F.直馏汽油
(5)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:
查看习题详情和答案>>
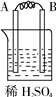
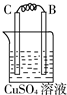
装 置 |
 |
 |
 |
| 现 象 | 金属A不断溶解 | C的质量增加 | A上有气体产生 |
| 正极反应式 |
请填写下列空白:

(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器及用品是
BDE
BDE
(填字母编号).A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.玻璃棒 G.石棉网
(2)步骤③的实验操作名称是
过滤
过滤
;步骤⑤实验操作名称是萃取分液
萃取分液
.(3)步骤④也可以用
Cl2
Cl2
填试剂名称)来起相同作用,写出该反应的离子方程式2I-+Cl2=I2+2Cl-
2I-+Cl2=I2+2Cl-
.(4)步骤⑤中,除选择用苯来提取碘,还可选择的试剂是
CEF
CEF
.A.酒精 B.醋酸 C.四氯化碳 D.甘油 E.己烷 F.直馏汽油
(5)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:
取少量提取碘后的水溶液于试管中,加入几滴淀粉试液;观察是否出现蓝色(如果变蓝,说明还有单质碘)
取少量提取碘后的水溶液于试管中,加入几滴淀粉试液;观察是否出现蓝色(如果变蓝,说明还有单质碘)
.(2011?枣庄模拟)由Fe2O3、Fe、CuO、C、Al中的几种物质组成的混合粉末,取样进行下列实验(部分产物略去):
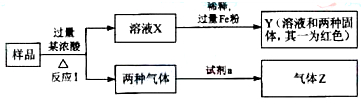
(1)取少量溶液X,加入过量的NaOH溶液,有沉淀生成.取上层清液,通入CO2,无明显变化,说明样品中不含有的物质是
(2)如何检验Y中的金属阳离子
(3)Z为一种或两种气体:
①若Z只为一种气体,试剂a为饱和NaHCO3溶液,则反应Ⅰ中能同时生成两种气体的化学方程式是
②若Z为两种气体的混合物,试剂a为适量的水,则Z中两种气体的化学式是
(4)向Y中通入过量的Cl2,并不断搅拌,充分反应后,溶液中的阳离子是
(5)取Y中的溶液,调节pH约为7,加入淀粉KI和H2O2,溶液呈蓝色并有红褐色沉淀生成.当消耗2molI-时,共转移3mol电子,该反应的离子方程式
查看习题详情和答案>>

(1)取少量溶液X,加入过量的NaOH溶液,有沉淀生成.取上层清液,通入CO2,无明显变化,说明样品中不含有的物质是
Al
Al
.(填化学式)(2)如何检验Y中的金属阳离子
取少量Y中的溶液加入适量KSCN溶液,无明显现象,再滴入适量氯水,溶液呈血红色,则说明溶液中含有Fe2+
取少量Y中的溶液加入适量KSCN溶液,无明显现象,再滴入适量氯水,溶液呈血红色,则说明溶液中含有Fe2+
.(3)Z为一种或两种气体:
①若Z只为一种气体,试剂a为饱和NaHCO3溶液,则反应Ⅰ中能同时生成两种气体的化学方程式是
C+2H2SO4(浓)═CO2↑+2SO2↑+2H2O
C+2H2SO4(浓)═CO2↑+2SO2↑+2H2O
.②若Z为两种气体的混合物,试剂a为适量的水,则Z中两种气体的化学式是
NO、CO2
NO、CO2
.(4)向Y中通入过量的Cl2,并不断搅拌,充分反应后,溶液中的阳离子是
Cu2+、Fe3+、H+
Cu2+、Fe3+、H+
_.(填写离子符号)(5)取Y中的溶液,调节pH约为7,加入淀粉KI和H2O2,溶液呈蓝色并有红褐色沉淀生成.当消耗2molI-时,共转移3mol电子,该反应的离子方程式
2Fe2++4I-+3H2O2=2Fe(OH)3↓+2I2
2Fe2++4I-+3H2O2=2Fe(OH)3↓+2I2
.
由Fe2O3、Fe、CuO、C、Al中的几种物质组成的混合粉末,取样进行下列实验(部分产物略去)以初步确定其成分.
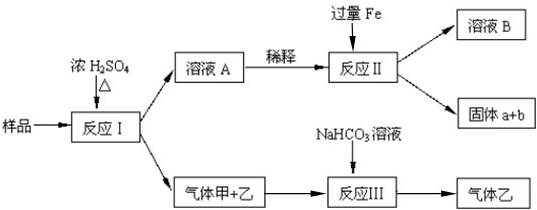
(1)取少量溶液A,加入过量氨水,有沉淀生成.过滤后向沉淀物中加入NaOH溶液,沉淀物的量无明显变化,说明样品中不含有的物质是 (填化学式).
(2)写出反应Ⅰ中同时生成两种气体甲和乙的化学方程式 .
(3)写出反应Ⅱ中生成红色固体b的离子方程式 .
(4)气体甲和乙经过反应Ⅲ,反应后溶液中增加的一种离子是 (用离子符号表示).
查看习题详情和答案>>

(1)取少量溶液A,加入过量氨水,有沉淀生成.过滤后向沉淀物中加入NaOH溶液,沉淀物的量无明显变化,说明样品中不含有的物质是
(2)写出反应Ⅰ中同时生成两种气体甲和乙的化学方程式
(3)写出反应Ⅱ中生成红色固体b的离子方程式
(4)气体甲和乙经过反应Ⅲ,反应后溶液中增加的一种离子是
(08年北京卷)(14分)由Fe2O3、Fe、CuO、C、Al中的几种物质组成的混合粉末,取样品进行下列实验(部分产物略去)

(1)取少量溶液X,加入过量的NaOH溶液,有沉淀生成。取上层清液,通入CO2,无明显变化,说明样品中不含有的物质是(填写化学式)______________。
(2)Z为一种或两种气体:
①若Z只为一种气体,试剂a为饱和NaHCO3溶液,则反应I中能同时生成两种气体的化学方程式是_______。
②若Z为两种气体的混合物,试剂a为适量水,则Z中两种气体的化学式是______。
(3)向Y中通入过量氯气,并不断搅拌,充分反应后,溶液中的阳离子是(填写离子符号)___________________________。
(4)取Y中的溶液,调pH约为7,加入淀粉KI溶液和H2O2,溶液呈蓝色并有红褐色沉淀生成。当消耗2 mol I-时,共转移3 mol电子,该反应的离子方程式是__________。
(5)另取原样品,加入足量稀硫酸充分反应。若溶液中一定不会产生Y中的红色固体,则原样品中所有可能存在的物质组合是(各组合中的物质用化学式表示)__________。
查看习题详情和答案>>