网址:http://m.1010jiajiao.com/timu3_id_87968[举报]

请完成以下问题:
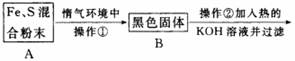
(1)混合粉末A中硫粉过量的原因是_____________________________________________。
(2)反应在“惰气环境”中进行的原因是__________________________________________。
(3)操作①是用烧热的玻璃棒点触混合粉末,反应即可持续进行,说明_________________。
(4)操作②的作用是_____________________,反应方程式是__________________________,也可改用加入________________。
(5)操作③稀H2SO4煮沸的目的是___________________________________________。
(6)为证明产物中铁的价态,对D溶液的实验操作最好是____________________________。
查看习题详情和答案>>为了证明铁和硫反应产物中铁的化合价,下面是某同学设计的实验过程的一部分:

请回答以下问题:
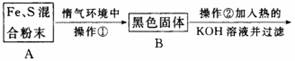
(1)混合粉末A中硫粉过量的原因是 ;
(2)反应在“惰气环境”中进行的原因是 ;
(3)操作①是用烧热的玻璃棒点触混合粉末,反应即可持续进行,说明__________;
(4)操作②的作用是__________。反应方程式是 。也可改用加入__________
(5)操作③稀H2SO4煮沸的目的是 ;
(6)为证明产物中铁的价态,对D溶液的实验操作最好是 。
查看习题详情和答案>>为了证明铁和硫反应产物中铁的化合价,下面是某同学设计的实验过程的一部分:
请完成以下问题:
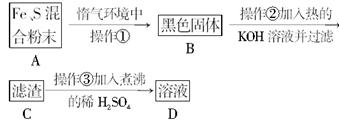
(1)混合粉末A中硫粉过量的原因是__________________。
(2)反应在“惰气环境”中进行的原因是__________________。
(3)操作①是用烧热的玻璃棒点触混合粉末,反应即可持续进行,说明__________________。
(4)操作②的作用是,反应方程式是__________________,也可改用加入__________________。
(5)操作③稀H2SO4煮沸的目的是__________________。
(6)为证明产物中铁的价态,对D溶液的实验操作最好是__________________。
查看习题详情和答案>>